Przeczytaj
Organizm ludzki do syntezy białek potrzebuje dwudziestu rodzajów aminokwasów. Część z nich musimy dostarczyć wraz z pożywieniem – są to aminokwasy egzogenneaminokwasy egzogenne. Część może być syntetyzowana w komórkach. To aminokwasy endogenneaminokwasy endogenne, do których syntezy niezbędne są odpowiednie prekursory oraz związki zawierające azot.
Aminokwasy endogenne i egzogenne
Aminokwasy endogenne | Aminokwasy egzogenne |
|---|---|
alanina (Ala) | arginina (Arg) |
asparagina (Asn) | fenyloalanina (Phe) |
cysteina (Cys) | histydyna (His) |
glicyna (Gly) | izoleucyna (Ile) |
glutamina (Gln) | leucyna (Leu) |
kwas asparaginowy (Asp) | lizyna (Lys) |
kwas glutaminowy (Glu) | metionina (Met) |
prolina (Pro) | treonina (Thr) |
seryna (Ser) | tryptofan (Trp) |
tyrozyna (Tyr) | walina (Val) |
Aminokwasy endogenne
Aminokwasy egzogenne
Synteza aminokwasów endogennych
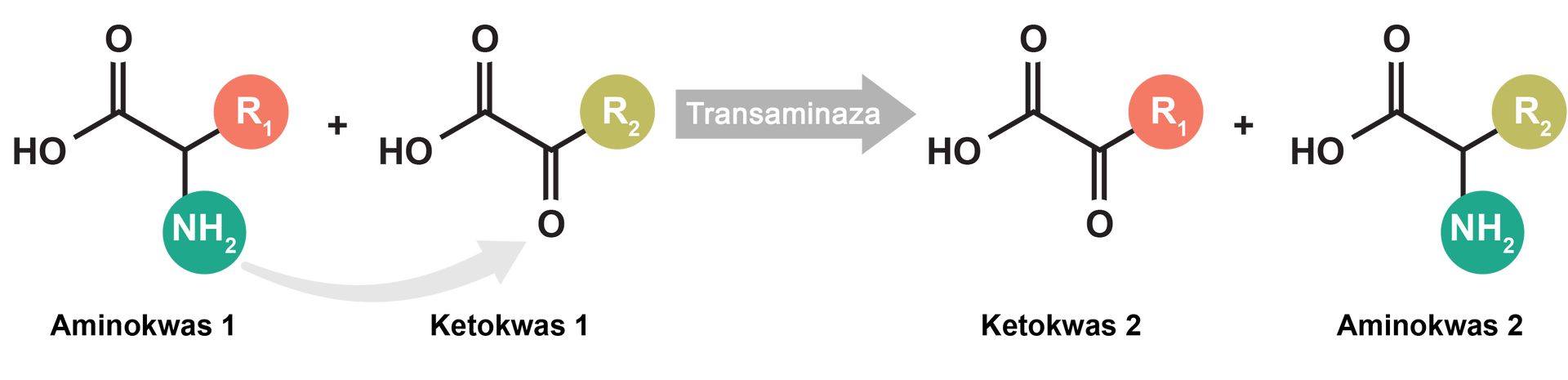
Aminokwasy to cząsteczki, które mimo wspólnych cech budowy znacząco różnią się między sobą. Dlatego są syntetyzowane podczas różnych szlaków biochemicznych z odpowiednich prekursorów. Są nimi ketokwasyketokwasy, do których zaliczamy pirogronian, szczawiooctan i -ketoglutaran. Na cząsteczki te przenoszone są grupy aminowe z innych aminokwasów, w reakcji zwanej transaminacjątransaminacją, która jest katalizowana przez enzymy należące do grupy transaminaztransaminaz (aminotransferaz).
Synteza glutaminianu
Większość aminokwasów endogennych można zsyntetyzować przy użyciu innego aminokwasu – glutaminianu, który jest wykorzystywany jako dawca grup aminowych. Glutaminian powstaje z -ketoglutaranu i jonów amonowych z wykorzystaniem , według reakcji:
W kolejnej reakcji grupa aminowa z glutaminianu przenoszona jest w reakcji transaminacji na ketokwas, co skutkuje wytworzeniem drugiego aminokwasu
i -ketoglutaranu. Wzór ogólny transaminacji:
glutaminian ketokwas ‑ketoglutaran aminokwas
Przykłady reakcji transaminacji:
glutaminian pirogronian -ketoglutaran alanina
glutaminian szczawiooctan -ketoglutaran asparaginian
Alanina i asparaginian powstają w wyniku transaminacji odpowiednio pirogronianu i szczawiootanu. Glutamina i asparaganina są syntetyzowane odpowiednio z glutaminianu i asparaginianu w połączeniu z jonami amonowymi. Prolina i arginina powstają również z glutaminianu. Seryna, będąca prekursorem glicyny i cysteiny, powstaje z kwasu--fosfoglicerynowego przy jednoczesnym wykorzystaniu glutaminianu.
Tyrozyna jest również aminokwasem endogennym. Powstaje jednak w inny sposób, niż pozostałe. Jej synteza polega na hydroksylacji egzogennego aminokwasu, fenyloalaniny.
Słownik
aminokwasy białkowe syntetyzowane przez organizm ludzki i organizmy zwierzęce oraz przez rośliny
aminokwasy białkowe, które nie są syntetyzowane przez organizmy. Muszą być dostarczone z zewnątrz
oksokwasy, związki organiczne, których cząsteczki zawierają grupę karboksylową i karbonylową
biochemiczna reakcja katalizowana przez enzymy aminotransferazy, podczas której grupa -aminowa () zostaje przeniesiona z aminokwasu (donor) na atom węgla ketokwasu (akceptor)
aminotransferazy, enzymy z klasy transferaz – katalizują reakcję przeniesienia grupy aminowej () aminokwasu na jeden z trzech ketokwasów: pirogronian, -ketoglutaran lub szczawiooctan. Reakcja przebiega według schematu:
aminokwas ketokwas ketokwas aminokwas