Przeczytaj
Alkany o krótkich łańcuchach węglowych stanowią potencjalne prekursory (związki wyjściowe) wielu podstawowych organicznych chemikaliów. Jednak przekształcenie alkanów do cennych chemikaliów często obejmuje pośrednie lub wieloetapowe drogi reakcji. Opracowanie bezpośrednich sposobów uzyskiwania kluczowych chemikaliów organicznych (np. alkenówalkenów) z niższych alkanów to marzenie wielu technologów chemicznych. Jedną ze skutecznych metod otrzymywania alkenów jest wdrożenie procesów katalitycznego odwodornienia odpowiednich alkanów. Na czym polega ten proces? Poniżej przedstawiono wybrane metody otrzymywania alkenów z alkanów.
Metody otrzymywania alkenów z alkanów
Reakcje eliminacji
1. Halogenowanie alkanów w obecności światła lub w podwyższonej temperaturze i eliminacja cząsteczki typu HX z halogenoalkanu
Alkeny można otrzymać w wyniku ciągu przemian zaprezentowanych na schemacie poniżej.
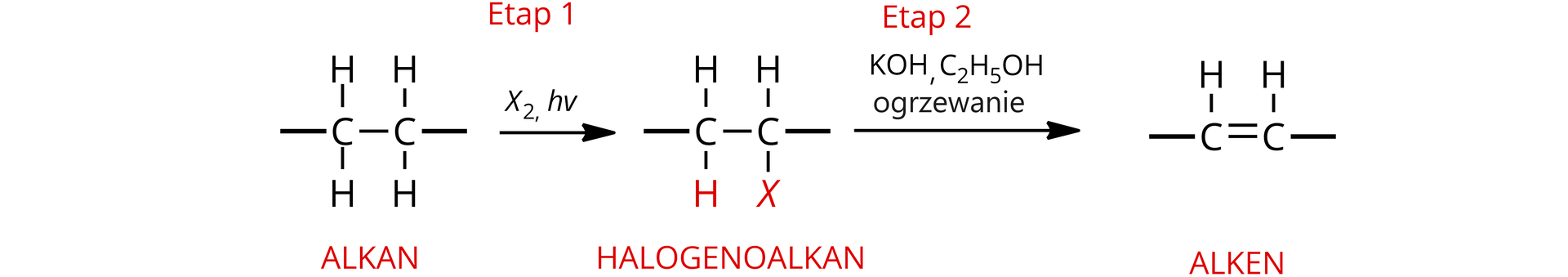
Otrzymywanie etenu
Etap 1. Halogenowanie alkanów w obecności światła (hnu) lub w podwyższonej temperaturze.
W pierwszym etapie, jako związek startowy, wykorzystywany jest etan, który w reakcji z lub , w obecności światła, daje odpowiedni halogenoalkan. Reakcja przebiega zgodnie z mechanizmem łańcuchowej substytucji rodnikowej.

Etap 2. Reakcja eliminacji cząsteczki typu HX z halogenoalkanu
Reakcja eliminacji przebiega w obecności silnej zasady w środowisku alkoholu (najczęściej etanolu) w podwyższonej temperaturze. W przedstawionym równaniu reakcji cząsteczka chloroetanu traci chlorowodór (), w efekcie czego powstaje alken. Chlorowodór reaguje z zasadą tworząc sól - chlorek potasu ().

Ta sama reakcja prowadzona w temperaturze pokojowej, w środowisku wodnym bez obecności alkoholu prowadzi do otrzymania etanolu.
2. Odwodornienie alkanów
Proces ten znany jest jako dehydrogenacja. Jest to proces odwrotny do uwodornienia. Reakcja ta polega na usunięciu cząsteczki wodoru z alkanu (lub innej cząsteczki organicznej). Jest to bardzo przydatny sposób przekształcania alkanów w alkeny.
Reakcja odwodornienia prowadzona jest w wysokiej temperaturze (400‑600°C) i pod obniżonym ciśnieniem. Katalizatory tej reakcji to między innymi: , , . Z uwagi na ciągły rozwój tej metody otrzymywania alkenów oraz udoskonalanie procesu technologicznego, liczba nowych katalizatorów nieustannie wzrasta.
Reakcja odwodornienia to reakcja równowagowa, dlatego równanie reakcji zapisujemy z dwiema pełnymi strzałkami skierowanymi w przeciwne strony. Sugeruje to, że reakcja w zależności od warunków może przebiegać w obu kierunkach. Z uwagi na fakt, że liczba moli produktów jest większa niż substratów, niskie ciśnienie zapewnia przesuwanie stanu równowagi chemicznej w kierunku produktów.
Przykłady reakcji odwodornienia
Odwodornienie butanu
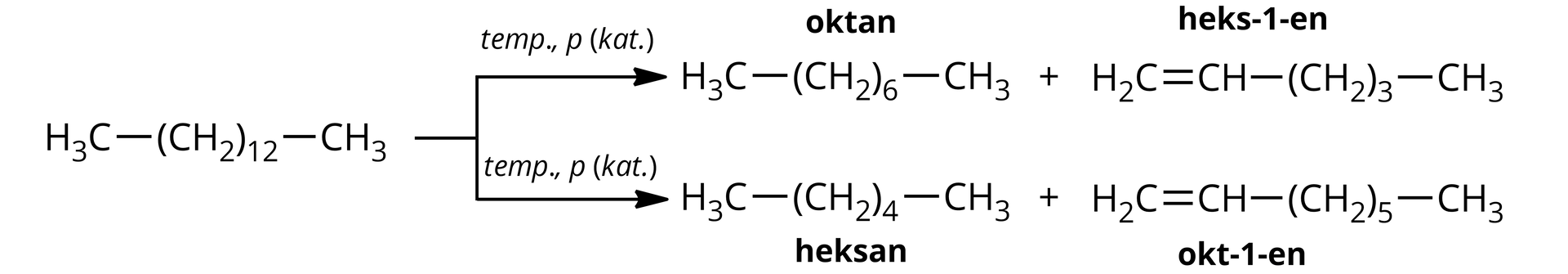
Odwodornienie alkanów o łańcuchach prostych, zawierających w cząsteczkach od 6 do 18 atomów węgla do odpowiednich terminalnych alkenów
Odwodornienie w obecności tlenku węgla(IV)
Na podstawie dostępnych danych literaturowych, otrzymywanie węglowodorów nienasyconych na drodze odwodornienia alkanów w obecności CO2, może przebiegać zgodnie ze schematem:
Przykład. Otrzymywanie but-1-enu
Alkany o łańcuchach węglowych dłuższych niż butan, w obecności ulegają przede wszystkim reakcjom krakingu.
Kraking
Podczas krakingukrakingu następuje rozerwanie wiązania węgiel - węgiel, wskutek czego z cząsteczki alkanu (łańcuch zawierający co najmniej 4 atomy węgla) powstają dwie cząsteczki - alkanu oraz alkenu. Rozerwanie wiązania może zachodzić w różnym miejscu, stąd otrzymywane są mieszaniny węglowodorów. Główny produkt wyodrębniany jest z mieszaniny produktów na drodze destylacji w obniżonej temperaturze i zwiększonym ciśnieniu.
1. Kraking termiczny
Jest to metoda przemysłowa otrzymywania wielu alkenów, m.in etenu. W procesie tym następuje rozkład termiczny alkanów, stąd nazwa kraking termiczny. Krakingowi termicznemu poddaje się oleje ciężkie, a reakcja przebiega pod zwiększonym ciśnieniem (2‑7 MPa) i w temperaturze 500 - 550°C.
Źródłem węglowodorów poddawanych krakingowi termicznemu jest często frakcja nafty lub frakcja oleju napędowego z destylacji frakcyjnej ropy naftowej.
Otrzymywanie etenu
3. Kraking katalityczny
W metodzie tej stosowane są katalizatory (np. , , glinokrzemiany, zeolity), a reakcja prowadzona jest w wysokiej temperaturze (450 - 510°C) i pod zmniejszonym ciśnieniem . W wyniku krakingu katalitycznego alkanów powstają zarówno alkany, jak i alkeny. Na przebieg i kierunek zachodzących reakcji zasadniczy wpływ ma temperatura i rodzaj użytego katalizatora. Stąd możliwe są dwie różne drogi zajścia procesu i otrzymanie różnych mieszanin węglowodorów.
Słownik
(łac. eliminare „usuwać”) proces polegający na oderwaniu od sąsiadujących atomów węgla dwóch atomów lub grup atomów bez zastąpienia ich innymi podstawnikami, w wyniku czego rośnie krotność wiązania lub powstaje związek cykliczny
grupa związków zbudowanych wyłącznie z atomów węgla i atomów wodoru, w cząsteczkach których między atomami węgla występuje jedno lub kilka wiązań wielokrotnych (podwójnych lub potrójnych)
(łac. substitutio „podstawianie”) (inaczej reakcja podstawiania, podstawienie) reakcja chemiczna, w której następuje podstawienie atomu lub grupy atomów innym atomem lub inną grupą atomów
nienasycone związki organiczne zbudowane z atomów węgla i atomów wodoru, o wzorze ogólnym ; posiadają w swojej strukturze wiązanie podwójne (w dowolnym miejscu łańcucha)
(z ang. crack „pękać”, „łamać”) to proces, podczas którego na skutek działania wysokiej temperatury (lub w obecności katalizatora) następuje rozerwanie wiązania węgiel - węgiel, wskutek czego z cząsteczki alkanu (łańcuch zawierający co najmniej 4 atomy węgla) powstają dwie cząsteczki - alkanu oraz alkenu; rozerwanie wiązania może zachodzić w różnym miejscu, stąd otrzymywane są mieszaniny węglowodorów
Bibliografia
Bhasin M. M., McCain J. H., Vora B. V., Imai T., Pujado P. R., Dehydrogenation and oxydehydrogenation of paraffins to olefins, Applied Catalysis A: General 221 (2001) 397- 419
https://chem.libretexts.org/ data dostępu 20.02.2020
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Encyklopedia PWN
Grzywa E., Molenda J., Technologia podstawowych syntez organicznych. Tom I. Surowce do syntez, Warszawa 1995.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1, Warszawa 2010.
McMurry J., Chemia organiczna, cz. 2, Warszawa 2010.
Skrzyńska E., Badanie aktywności katalizatorów wanadowych w reakcji odwodornienia izobutanu do izobutenu w obecności ditlenku węgla, praca doktorska, dostęp: https://repozytorium.biblos.pk.edu.pl/redo/resources/26579/file/suwFiles/SkrzynskaE_BadanieAktywnosci.pdf