Przeczytaj
Stereoizomery
Mamy dwie nieidentyczne cząsteczki. W jaki sposób ocenić, czy i jakim rodzajem izomerów są te cząsteczki? Dowiesz się klikając na poniższe odpowiedzi.
Spora liczba związków chemicznych posiada jeden atom asymetrycznyatom asymetryczny (chiralny), czyli jedno centrum chiralności. Gdy związek posiada dwa i więcej centrów chiralności, sytuacja staje się bardziej skomplikowana, ponieważ związek będzie posiadał więcej stereoizomerówstereoizomerów.
Czy można przewidzieć liczbę stereoizomerów na podstawie budowy związku?
W celu wyznaczenia liczby możliwych stereoizomerów, należy skorzystać z poniższej reguły:
Maksymalna liczba stereoizomerów wynosi 2Indeks górny nn, gdzie n to liczba centrów chiralności.
Kiedy n = 1, liczba stereoizomerów wynosi 2Indeks górny 1 Indeks górny koniec1 = 2.
Gdy cząsteczka posiada jeden atom chiralny, utworzone stereoizomery są enancjomeramienancjomerami.
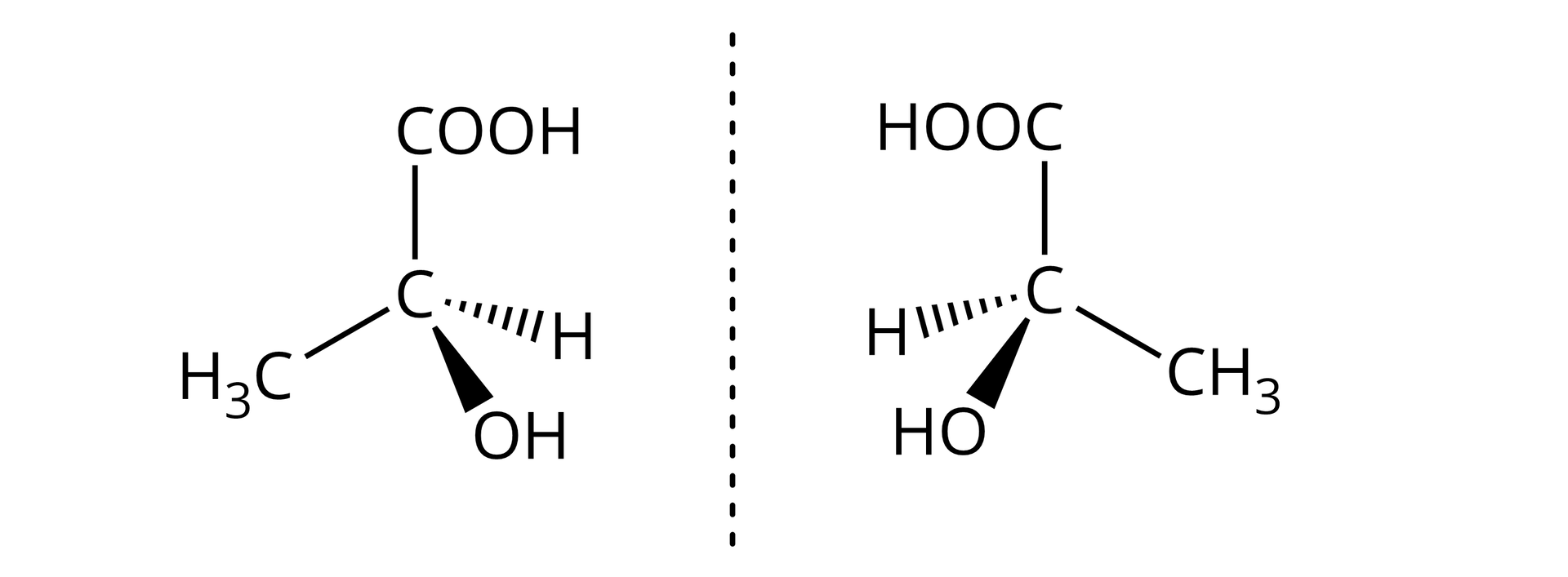
Kiedy n = 2, liczba stereoizomerów wynosi 2Indeks górny 2 Indeks górny koniec2 = 4.
Gdy cząsteczka posiada dwa atomy chiralne, liczba możliwych stereoizomerów wynosi cztery lub mniej. W przypadku, gdy związek tworzy mniej stereoizomerów niż cztery, to obok pary enancjomerów tworzy także diastereoizomerdiastereoizomer - czyli w sumie trzy stereoizomery.
Diastereoizomery a enancjomery – różnice
Poniżej przedstawiono właściwości fizyczne trzech stereoizomerów kwasu 2,3‑dihydroksybutanodiowego (kwasu winowego). Na podstawie danych w tabeli sformułuj wnioski, które dotyczą różnic między enancjomerami a diasteroizomerami. Spróbuj wyjaśnić, z czego one wynikają, a następnie sprawdź poprawną odpowiedź.
Przedstawiono właściwości fizyczne trzech stereoizomerów kwasu 2,3‑dihydroksybutanodiowego (kwasu winowego). Zapoznaj się z opisem. Na podstawie danych w tabeli sformułuj wnioski, które dotyczą różnic między enancjomerami a diasteroizomerami. Spróbuj wyjaśnić, z czego one wynikają, a następnie sprawdź poprawną odpowiedź.
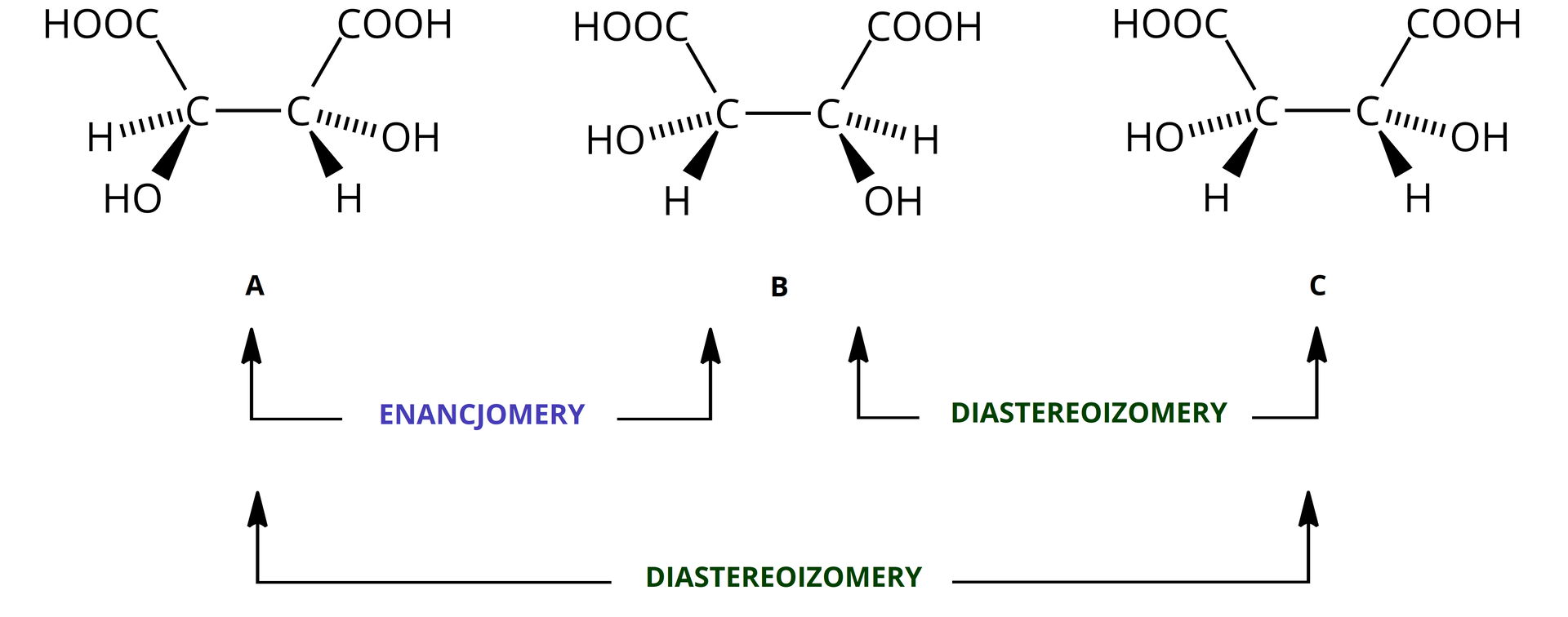
Właściwość | A | B | C |
|---|---|---|---|
Temperatura topnienia [°C] | 171 | 171 | 146 |
Rozpuszczalność w wodzie [] | 139 | 139 | 125 |
Skręcalność właściwaSkręcalność właściwa [°] | + 13 | - 13 | 0 |
Konfiguracja absolutnaKonfiguracja absolutna R,S | R,R | S,S | R,S |
Z uwagi na fakt, że enancjomery posiadają identyczne właściwości fizyczne, nie można ich rozdzielić przy użyciu takich technik, jak np. destylacja. Z kolei diastereoizomery różnią się właściwościami fizycznymi, takimi jak temperatura topnienia i wrzenia oraz można je rozdzielać używając metody destylacji prostej.
Co ciekawe, enancjomery mogą się różnić także właściwościami biologicznymi. Wynika to z ich chiralnościchiralności. W procesach przebiegających w organizmach żywych biorą udział chiralne cząsteczki białek (enzymy), które reagują z odpowiednimi substratami, gdy te posiadają określoną budowę przestrzenną. Przykładem są receptory smaku i zapachu, które rozróżniają chiralne enancjomery, np. enanncjomery aminokwasów. Smak większości aminokwasów białkowych określany jest jako słodki lub gorzki. W przypadku enancjomerów aminokwasów (jak np. fenyloalanina, tryptofan, leucyna) jeden enancjomer jest słodki, a drugi gorzki.
W poniższej tabeli przedstawiono enancjomery wybranych aminokwasów oraz odpowiadający im smak.
D- aminokwas | L‑aminokwas | |
|---|---|---|
fenyloalanina | słodki | gorzki |
tryptofan | słodki | gorzki |
leucyna | słodki | gorzki |
Indeks górny /źródło: Schiffman S. S., Sennewald K., Gagnon J., Comparison of taste qualities and thresholds of D- and L‑amino acids, Physiology & Behavior, Volume 27, Issue 1, 1981, Pages 51‑59,/ Indeks górny koniec/źródło: Schiffman S. S., Sennewald K., Gagnon J., Comparison of taste qualities and thresholds of D- and L‑amino acids, Physiology & Behavior, Volume 27, Issue 1, 1981, Pages 51‑59,/
Zarówno pojęcie enancjomerii, jak i diastereoizomerii odnosi się do pary związków i określa wzajemną relację jednego związku do drugiego. Należy pamiętać, że ten sam związek może być i enancjomerem, i diastereoizomerem. Istotne jest jednak to, względem jakiego innego związku jest porównywany.
Słownik
(gr. cheír „ręka”) cecha obiektów chemicznych polegająca na tym, że cząsteczka wyjściowa nie pokrywa się ze swoim odbiciem w płaskim zwierciadle – nie można obu cząsteczek nałożyć na siebie na drodze obrotu ani przesunięcia
tzw. atom chiralny; atom pierwiastka, połączony z czterema różnymi podstawnikami, oznaczany symbolem gwiazdki (*)
izomery przestrzenne, które różnią się ułożeniem atomów w przestrzeni; klasyfikuje się je na kilka sposobów; mogą to być: konformery (cząsteczki przechodzące wzajemnie w siebie przez obrót wokół pojedynczych wiązań), izomery konfiguracyjne (cząsteczki nie przechodzące wzajemnie w siebie przez obrót, ale przez zerwanie i odtworzenie wiązań ), izomery optyczne (należą do nich enancjomery i diastereoziomery)
(gr. enantios „przeciwne, odwrotne”, meros „fragment”) izomery, które mają się do siebie tak, jak przedmiot do swego odbicia w zwierciadle płaskim i tworzą parę nienakładalnych na siebie cząsteczek chemicznych; posiadają te same właściwości fizyczne; skręcają płaszczyznę światła spolaryzowanego o tę samą wartość kąta, ale w przeciwnym kierunku
stereoizomery, które nie są własnymi odbiciami lustrzanymi
związek chiralny (posiadający atom asymetryczny), który posiada zdolność do skręcania płaszczyzny światła spolaryzowanego w prawo lub lewo
kąt skręcenia płaszczyzny płaszczyzny światła spolaryzowanego, wyrażony w stopniach, gdy długość rurki polarymetrycznej z roztworem substancji optycznie czynnej wynosi 1 dm, a stężenie roztworu c=1 ; skęcalność właściwa często oznaczana jest symbolem , jeżeli pomiar był prowadzony przy użyciu lampy sodowej (światło o długości fali 589 nm, to tak zwana linia D widma par sodu, czyli światło żółte emitowane przez lampy sodowe); wartość skręcalności właściwej przy określonej długości fali jest zależna od temperatury, dlatego nad literą D wstawia się liczbę, która oznacza temperaturę, np.
(łac. configuratio „ukształtowanie”, „porównanie”) sposób rozróżniania i nazewnictwa izomerów optycznych na podstawie rozmieszczania podstawników wokół asymetrycznego atomu węgla
Sposób przejścia po podstawnikach wokół asymetrycznego atomu określa się, przemieszczając się od podstawnika o najwyższym pierwszeństwie do podstawnika o najniższym pierwszeństwie, gdy:
przejście odbywa się zgodnie z ruchem wskazówek zegara, to konfiguracja absolutna jest oznaczana literą R (od łac. rectus – prawy);
przejście odbywa się przeciwnie do ruchu wskazówek zegara, to konfiguracja absolutna oznaczana jest literą S (od łac. sinister – lewy)
Bibliografia
Encyklopedia PWN
Hejwowska S., Marcinkowski R., Staluszka J., Chemia 2. Zakres rozszerzony, Gdynia 2011.
Kołodziejczyk A., Naturalne związki organiczne, Warszawa 2013.
Litwin M., Styka‑Wlazło Sz., Szmońska J., Chemia organiczna 2, Warszawa 2005.
Gorzynski Smith J., Organic Chemistry, Third Edition, New York 2011.