Przeczytaj
Ogólna budowa nazwy związku chemicznego
Gdy tworzymy nazwę związku chemicznego, należy:
znaleźć główną grupę funkcyjną i odpowiadający jej przyrostek użyć w nazwie;
ponumerować i nazwać układ podstawowy (z grupą główną), uwzględniając przy tym ewentualne końcówki odpowiednie dla wiązań wielokrotnych;
określić lokalizację (lokanty) podstawników i podać je w nazwie z najniższymi możliwymi lokatami w porządku alfabetycznym.
Układając nazwę związku organicznego, należy zachować następujący układ: przedrostki‑nazwa podstawowa‑końcówki‑przyrostki.
Przedrostek informuje o położeniu podstawników, końcówki o obecności lub braku wiązań wielokrotnych, a z kolei przyrostki oznaczają podstawową (najwyższą w hierarchii regułę pierwszeństwa grup) grupę funkcyjną związku chemicznego.
W przypadku wystąpienia więcej niż jednego takiego samego podstawnikapodstawnika, stosujemy przedrostek, który oznacza wielokrotność atomów węgla (mnożnik), pochodzących od nazw liczebników greckich lub łacińskich. Mnożniki nie zmieniają ustalonego porządku wymieniania podstawników.
liczba podstawników | przedrostek |
|---|---|
mono | |
di | |
tri | |
tetra | |
penta | |
heksa | |
hepta | |
okta | |
nona | |
deka | |
undeka | |
dodeka |
Budowa fenoli
FenoleFenole to związki chemiczne o wzorze ogólnym: .
gdzie:
– grupa arylowa;
– grupa hydroksylowa.
Grupa arylowa to jednowartościowa grupa, utworzona przez oderwanie atomu wodoru od pierścienia aromatycznego.


Podczas wojny światowej, w obozach koncentracyjnych prowadzono eliminację więźniów. Używano do tego m.in. właściwości toksycznych fenolufenolu. Za pomocą długiej igły wstrzykiwano ofierze śmiertelną dawkę roztworu fenolu w pierś. Jeśli iniekcja wykonana była w sposób prawidłowy (bezpośrednio do komory serca), to śmierć następowała po upływie około pół minuty. W ten sposób sierpnia roku w bunkrze głodowym zginął również Maksymilian Kolbe. Franciszkanin zgłosił się w celu dobrowolnego oddania życia za współwięźnia Franciszka Gajowniczka, jednego z dziesięciu skazanych na śmierć głodową, w odwecie za jego ucieczkę.
Fenole to związki chemiczne, które posiadają przynajmniej jedną grupę hydroksylową (), bezpośrednio połączoną z pierścieniem aromatycznym. Najprostszym przedstawicielem tych związków jest fenol o wzorze sumarycznym . Nazwą zalecaną przez IUPAC dla tego związku jest fenol. Nazwę systematycznąNazwę systematyczną tworzy się przez dodanie do nazwy węglowodoru przyrostku „-ol”, z uwzględnieniem mnożników i położenia poszczególnych grup .
Nazewnictwo fenoli i jego związków
Nazwa „fenol” używana jest nie tylko w odniesieniu do benzenolu, ale również do takich pochodzących od niego związków, które nie zawierają więcej niż jednej grupy połączonej z pierścieniem aromatycznym. Chodzi bowiem o sytuację, gdzie nie występują ugrupowania decydujące o tym, że jest to inny typ związku chemicznego (reguła pierwszeństwa grup).
Nazwę systematyczną tworzy się przez dodanie do nazwy węglowodoru przyrostku
„-ol”, z uwzględnieniem mnożników i położenia poszczególnych grup .
Fenole są grupą związków chemicznych, w których nazwach, zalecanych przez IUPAC, jest słowo fenol. Posiadają przyrostek „-ol” w nazwie.
Nazwy fenoli monohydroksylowych
Do nazwy węglowodoru aromatycznego, z którym związana jest grupa hydroksylowa, należy dodać przyrostek (końcówkę) „-ol”.
Nazwy fenoli polihydroksylowych
Do nazwy węglowodoru aromatycznego, z którym związane są grupy hydroksylowe, należy dodać przyrostek (końcówkę) „-odiol” – w przypadku dwóch grup hydroksylowych – lub „-otriol” – w przypadku trzech grup hydroksylowych itd. (-tetrol, -pentol) – wraz z lokantami, odpowiadającymi grupom hydroksylowym. Zachowuje się numerację atomów węgla układu aromatycznego, jak w przykładzie zamieszczonym poniżej.
Związki o następujących wzorach grupowych nie są fenolami, mimo obecnych w swojej strukturze atomów wodoru i tlenu. Porównaj poniższe struktury z definicją fenoli, a dowiesz się, dlaczego.
Aldehyd benzoesowy - wzór cząsteczki zbudowany jest z sześcioczłonowego pierścienia aromatycznego, w którym jeden z atomów węgla tworzących pierścień podstawiony jest grupą aldehydową , to znaczy łączy się z atomem węgla, który to związany jest za pomocą wiązania podwójnego z atomem tlenu oraz za pomocą wiązania pojedynczego z atomem wodoru.
Kwas benzoesowy - wzór cząsteczki zbudowany jest z sześcioczłonowego pierścienia aromatycznego, w którym jeden z atomów węgla tworzących pierścień, podstawiony jest grupą karboksylową , to znaczy łączy się z atomem węgla, który to związany jest za pomocą wiązania podwójnego z atomem tlenu oraz za pomocą wiązania pojedynczego z grupą hydroksylową .
Fenylometanol - wzór cząsteczki zbudowany jest z sześcioczłonowego pierścienia aromatycznego, w którym jeden z atomów węgla tworzących pierścień podstawiony jest grupą metylenową podstawioną grupa hydroksylową .
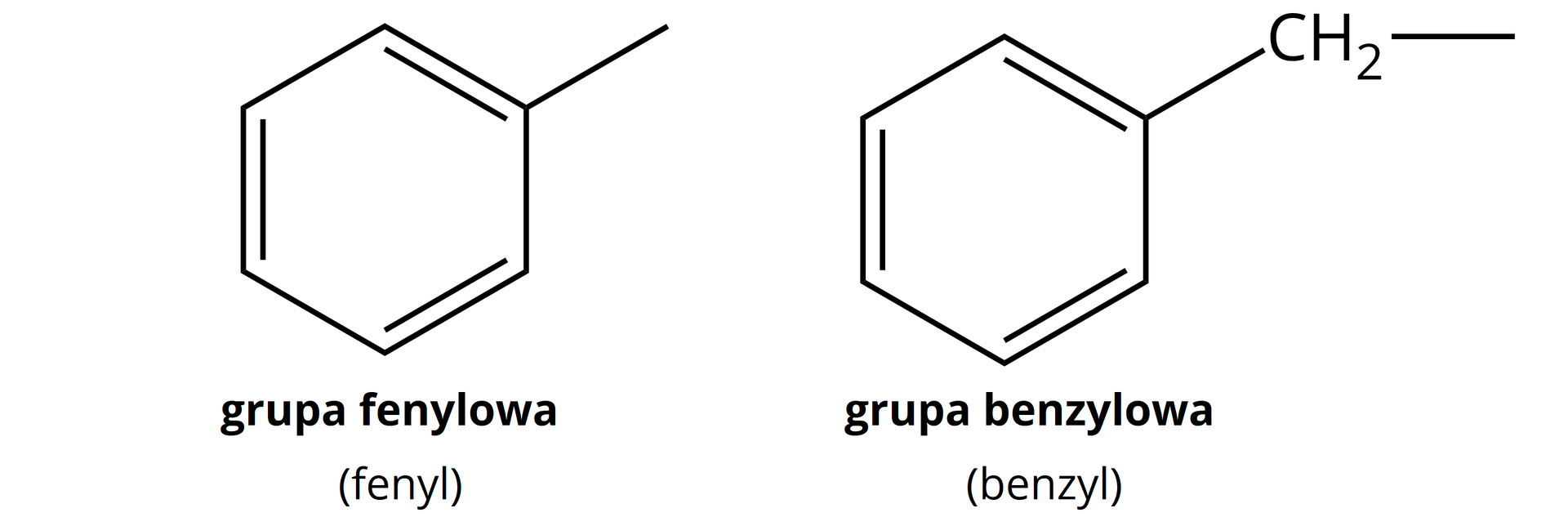
Nie należy mylić fenolu:

z grupą fenylową (fenyl) lub z grupą benzylową (benzyl):
Związki fenolu
Cząsteczka fenolu może być podstawiona dodatkowymi grupami – np. grupą metylową. Prześledźmy wzory i nazwy izomerów o wzorze sumarycznym .
Nazwa izomeru | Wzór sumaryczny | Wzór półstrukturalny i model 3D |
|---|---|---|
‑metylofenol |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |
‑metylofenol |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |
‑metylofenol | 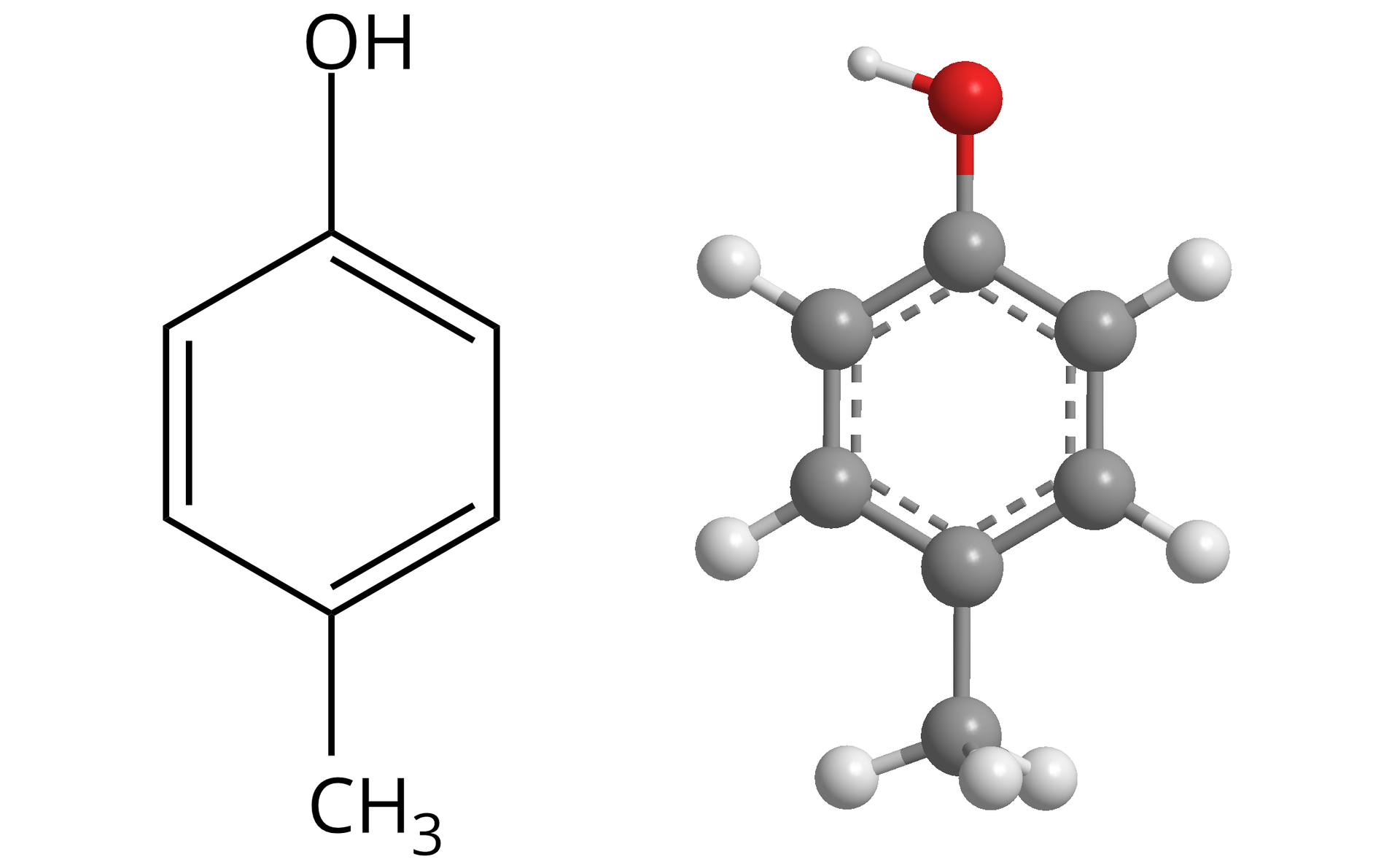 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Fenole z podstawionymi grupami to metylofenole, zwyczajowo nazywane krezolami.
Inne związki fenolu
W strukturze fenolu mogą być obecne również inne podstawniki, np.:

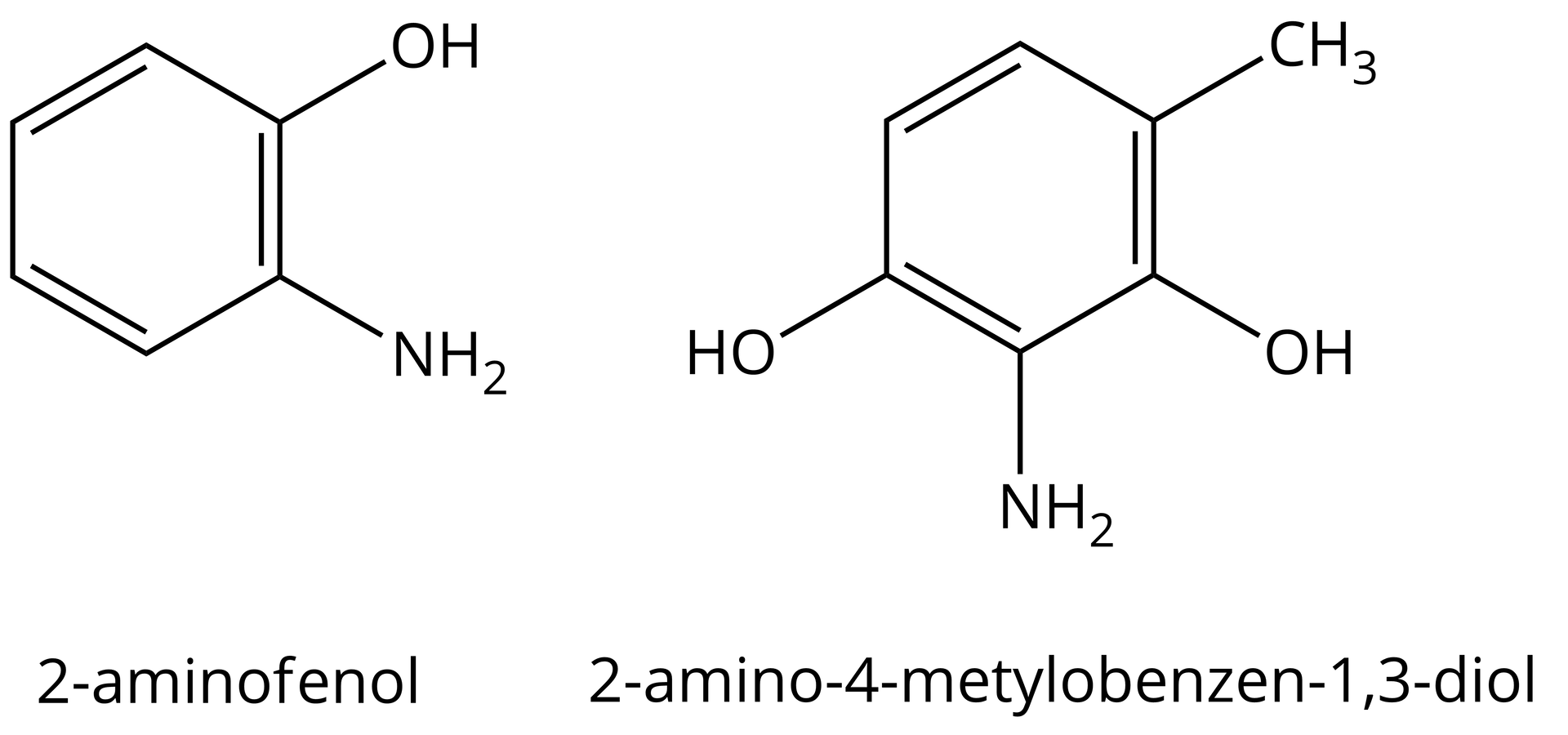
Ponieważ grupa aminowa jest mniej ważna od grupy hydroksylowej, będzie pełnić rolę podstawnika w związkach zawierających grupy hydroksylowe, np.:
Do sześcioczłonowego pierścienia aromatycznego przyłączone są następujące grupy: w pozycji pierwszej i drugiej po jednej grupie , a w pozycji piątej atom chloru . Możliwe odpowiedzi: 1. -chlorobenzeno-,-diol, 2. -chlorofenol, 3. -chlorobenzeno-,-diol, 4. -bromobenzeno-,-diol
Słownik
związki, w których występują atomy związane ze sobą tak, że tworzą jeden lub więcej zamkniętych pierścieni
związek organiczny o wzorze sumarycznym ; podstawowy węglowodór aromatyczny
benzenol, dawniej pot. kwas karbolowy, karbol, związek organiczny; najprostszy przedstawiciel grupy monohydroksylowych fenoli
związki organiczne; mono-, di- i polihydroksylowe pochodne benzenu oraz alkilobenzenów, których cząsteczki zawierają grupy hydroksylowe (), związane z atomem węgla pierścienia benzenowego
nazwa związku chemicznego, która jest złożona całkowicie ze specjalnie stworzonych sylab, liczbowych przedrostków i innych znaków, zgodna z regułami systematycznej nomenklatury zalecanej przez IUPAC, np.
-etylo-,-dimetylononan i - chloroetan--ol
atom lub ich grupa w miejscu atomu wodoru lub przy atomie węgla w związkach organicznych; podstawnikami nazywa się także grupy funkcyjne
Bibliografia
Atkins P., Jones L., Chemia ogólna. Cząsteczki, materia, reakcje, Warszawa 2004, s. 524‑525.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Encyklopedia PWN
Mastalerz P., Podręcznik chemii organicznej, Wrocław 1998.
McMurry J., Chemia organiczna, t. 1 i 2, Warszawa 2000.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1 i 2, Warszawa 1997.
Proniewicz E., Nomenklatura związków organicznych, e‑podręcznik 2019.
Wojcieszyńska D., Wilczek A., Związki fenolowe pochodzenia naturalnego, „Chemia w szkole” 2006, nr 6.