Przemiana fizyczna, reakcja chemiczna, typy reakcji chemicznych, równania reakcji
Za pomocą zmysłów rejestrujemy wiele efektów przemian zachodzących w otoczeniu. W niektórych z nich substancje zmieniają jedynie swoje właściwości fizyczne (np. stan skupienia), a w innych przekształcają się w nowe. Czy opisane przemiany można jakoś rozróżnić, nazwać, opisać?
Jaka przemiana wiąże się ze zmianą właściwości fizycznych substancji?
W swoim otoczeniu możemy zauważyć wiele przemian, w efekcie których zmieniają się właściwości fizyczne materii, ale nie ona sama. Przykładem może być zamarzanie wody. Lód, który powstaje w wyniku tego procesu, nie jest nową substancją chemiczną, lecz w dalszym ciągu wodą. W następstwie obniżenia temperatury, zmianie ulega jedynie stan skupienia (właściwość fizyczna) tej substancji. Taki proces, w wyniku którego materia zmienia jedynie swoje właściwości fizyczne, nazywamy przemianą fizyczną lub zjawiskiem fizycznym.
W poniższej galerii zamieszczono przykłady przemian fizycznych, które można zaobserwować w codziennym życiu.
Czy procesy ogrzewania, a następnie ochładzania siarki, to przemiany fizyczne czy chemiczne?
Obejrzyj zamieszczony poniżej film, który pozwoli Ci na udzielenie jednoznacznej odpowiedzi. Następnie, na podstawie przedstawionego materiału, uzupełnij dziennik laboratoryjny.

Film dostępny pod adresem /preview/resource/RkuqvoBqpJzhx
Film przedstawia doświadczenie, w którym z siarki krystalicznej otrzymywana jest inna odmiana alotropowa siarki – siarka plastyczna. Film zawiera dodatkowo porównanie właściwości siarki plastycznej oraz siarki krystalicznej.
Przeprowadzono doświadczenie, które miało na celu sprawdzenie, czy procesy ogrzewania, a następnie ochładzania siarki, to przemiany fizyczne czy chemiczne.
Co było potrzebne:
siarka (krystaliczna);
zimna woda;
żaroodporna probówka;
statyw na probówki;
palnik;
drewniana łapa do probówek;
łyżeczka;
dwa szkiełka zegarkowe;
zlewka;
bagietka;
młotek.
Przebieg doświadczenia:
Siarkę umieszczono w probówce (probówkę wypełniono siarką do ok. jej wysokości). Zawartość probówki delikatnie ogrzewano w płomieniu palnika do czasu, gdy siarka uzyskała płynną konsystencję i zmieniła barwę na brązową. Energicznym ruchem przelano ciekłą siarkę do zlewki wypełnionej do połowy zimną wodą. Gdy ostygła, wyjęto ją ze zlewki za pomocą bagietki i położono na szkiełku zegarkowym. Zbadano plastyczność otrzymanej siarki poprzez rozciąganie, zginanie. Pozostawiono ją na powietrzu przez kilka godzin, a następnie sprawdzono jej barwę, twardość oraz kruchość.
Obserwacje:
Siarka w trakcie ogrzewania topi się, zmieniając w ciecz o jasnożółtej barwie. Podczas dalszego ogrzewania, jej barwa zmienia się na ciemnobrunatną. Substancja uzyskana po przelaniu cieczy do zimnej wody ma także ciemnobrunatne zabarwienie i jest plastyczna (łatwo ją wyginać i rozciągać). Po pewnym czasie powraca do początkowej postaci – kruchej, stałej i o żółtej barwie.
Wnioski:
Procesy ogrzewania, a następnie ochłodzenia siarki, są zjawiskami fizycznymi.
Podsumowanie:
Siarka pod wpływem temperatury topi się, zmieniając się w ciecz o jasnożółtej barwie. Dalszemu ogrzewaniu jej płynnej postaci towarzyszy znaczny wzrost gęstości oraz zmiana barwy na ciemnobrunatną. Ogrzewając nadal zawartość probówki, obserwujemy ponowne zmniejszenie gęstości siarki (staje się płynna), co zachodzi już bez zmiany barwy. Produkt gwałtownego ochłodzenia ciekłej siarki o ciemnobrunatnej barwie ma cechy ciała plastycznego – łatwo go wyginać i rozciągać. Po pewnym czasie powraca on do początkowej postaci – kruchej, stałej i o żółtej barwie. Przemiany siarki podczas jej ogrzewania, a następnie ochłodzenia, są zjawiskami fizycznymi, które łączą się ze zmianami stanu skupienia oraz zmianami barwy tej substancji.
Jakie przemiany powodują, że jedne substancje przekształcają się w inne?
W naszym otoczeniu ciągle obserwuje się przemiany, podczas których substancje ulegają trwałym zmianom i przekształcają się w inne.
Wspomniane przemiany zachodzą zwykle pod wpływem różnych czynników: działania wysokiej temperatury, mikroorganizmów, wzajemnego oddziaływania różnych substancji. Mają wspólną cechę – w ich wyniku powstają nowe substancje o odmiennych właściwościach. O tego typu procesach mówi się, że są to przemiany chemiczne lub reakcje chemiczne.
W poniższej galerii zamieszczono przykłady przemian chemicznych, które można zaobserwować w codziennym życiu:
Zastanów się, jakiej przemianie ulega siarka podczas palenia. Obejrzyj zamieszczony poniżej film, który pozwoli Ci na udzielenie jednoznacznej odpowiedzi. Następnie, na podstawie materiału, uzupełnij dziennik laboratoryjny.

Film dostępny pod adresem /preview/resource/R1dOZq9nhnqnI
Film przedstawia doświadczenie, w którym przeprowadzane jest spalanie siarki. Film prezentuje potrzebny sprzęt laboratoryjny oraz sam proces spalania.
Przeprowadzono doświadczenie, które miało na celu zbadanie, jakiej przemianie ulega siarka podczas palenia.
Co było potrzebne:
siarka;
łyżka do spalań;
wysoki cylinder miarowy;
palnik;
zapałki.
Przebieg doświadczenia:
Nałożono niewielką ilość siarki na łyżkę do spalań. Umieszczono ją w płomieniu palnika i poczekano, aż znajdująca się na niej siarka ulegnie zapaleniu. Umieszczono łyżkę do spalań z płonącą siarką w wysokim cylindrze miarowym. Zanotowano zachodzące zachodzące zmiany.
Obserwacje:
Siarka umieszczona w płomieniu palnika najpierw stopiła się, a następnie zapaliła niebieskim płomieniem. W wyniku spalania siarki powstały białe dymy – wydzielił się gaz o charakterystycznym zapachu.
Wnioski:
Siarka w procesie spalania ulega przemianie chemicznej, w wyniku której powstaje nowa substancja – tlenek siarki().
Podsumowanie:
Siarka umieszczona w płomieniu palnika najpierw się topi, a następnie ulega zapaleniu. Spala się niebieskim płomieniem. W wyniku spalania siarki powstaje bezbarwna substancja o gazowym stanie skupienia – tlenek siarki(). Przemiana ta jest przykładem reakcji (przemiany) chemicznej.
Przeprowadź reakcję chemiczną, wykorzystując substancje (składniki) obecne w Twojej kuchni. Podczas wykonywania poniższego doświadczenia pamiętaj o zachowaniu wszelkich zasad bezpieczeństwa.
Co będzie potrzebne:
soda oczyszczona;
ocet;
łyżka stołowa;
lejek;
butelka o małej pojemności;
balonik.
Instrukcja wykonania:
Sodę oczyszczoną wsyp do balonika (maks. dwie duże łyżki).
Do butelki wlej octu.
Delikatnie nałóż balonik na szyjkę butelki w taki sposób, aby soda oczyszczona nie przedostała się do butelki, zanim zakończysz tę czynność.
Unieś balonik do góry i przesyp jego zawartość do butelki.
Wyjaśnienie:
W trakcie doświadczenia, między składnikami sody oczyszczonej i octu, zachodzi reakcja chemiczna, podczas której wydziela się gaz – tlenek węgla() (dwutlenek węgla) – wypełniający balon.
Przeprowadzono reakcję chemiczną, wykorzystując substancje (składniki) obecne w przeciętnej kuchni. Podczas wykonywania poniższego doświadczenia zachowano wszelkie zasady bezpieczeństwa.
Co było potrzebne:
soda oczyszczona;
ocet;
łyżka stołowa;
lejek;
butelka o małej pojemności;
balonik.
Przebieg doświadczenia:
Dwie duże łyżki sody oczyszczonej wsypano do balonika. Do butelki wlano octu. Delikatnie nałożono balonik na szyjkę butelki, w taki sposób, aby soda oczyszczona nie przedostała się do butelki. Uniesiono balonik do góry i przesypano jego zawartość do butelki.
Wyjaśnienie:
W trakcie doświadczenia, między składnikami sody oczyszczonej i octu zaszła reakcja chemiczna, podczas której wydzielił się gaz – tlenek węgla() (dwutlenek węgla) – wypełniający balon.
Czym różni się zjawisko fizyczne od reakcji chemicznej?
Zjawiska fizyczne i przemiany chemiczne towarzyszą nam każdego dnia. Nie zawsze bez trudu możemy ocenić ich rodzaj. W wielu przypadkach sama obserwacja procesu nie wystarczy, aby można było określić, czy w jego wyniku powstała nowa substancja, czy tylko zmieniły się właściwości fizyczne (np. stan skupienia) substancji ulegającej tej przemianie. Zastosowane czynniki również nie determinują rodzaju przemiany. W wyniku ogrzewania substancja może albo ulec przemianie fizycznej, albo wziąć udział w reakcji chemicznej.
W efekcie zmieszania dwóch różnych substancji może powstać ich mieszanina (zjawisko fizyczne) bądź też zajść reakcja chemiczna, w wyniku której utworzy się nowa substancja (lub substancje). Jest to uzależnione od właściwości samych substancji oraz od warunków, w jakich się znajdują (np. temperatury otoczenia). Dlatego wiedza na temat ich właściwości jest przydatna podczas przewidywania rodzaju przemian, które zachodzą pod wpływem działania różnych czynników.
Zastanów się i odpowiedz na pytanie, jakie przemiany zachodzą podczas zmieszania, a następnie ogrzania siarki i żelaza. Obejrzyj zamieszczony poniżej film, który pozwoli Ci na udzielenie jednoznacznej odpowiedzi. Następnie, na podstawie materiału, uzupełnij dziennik laboratoryjny.

Film dostępny pod adresem /preview/resource/R19ucAO2jrqTv
Film przedstawia doświadczenie chemiczne, w którym badana jest reaktywność siarki i żelaza. Porównano wpływ temperatury na zajście reakcji chemicznej.
Przeprowadzono doświadczenie w celu zbadania, jakie przemiany (fizyczne czy chemiczne) zachodzą podczas zmieszania ze sobą, a następnie ogrzania siarki i żelaza.
Co było potrzebne:
siarka krystaliczna ();
żelazo w postaci pyłu (tak zwany pył żelazny, );
moździerz z tłuczkiem;
magnes;
tygiel porcelanowy;
metalowe szczypce;
zapałki;
palnik gazowy.
Przebieg doświadczenia:
W moździerzu umieszczono siarki i żelaza i starannie wymieszano. Sprawdzono, czy w mieszaninie nadal znajduje się żelazo – zbliżono do niej magnes. Przeniesiono mieszaninę siarki i żelaza do porcelanowego tygla. Złapano go za pomocą szczypiec i ogrzewano od spodu płomieniem palnika. Proces prowadzono do momentu, aż mieszanina uległa rozżarzeniu. Po ustaniu wszelkich zmian, za pomocą magnesu sprawdzono obecność żelaza w powstałej masie.
Obserwacje:
Siarka, po zmieszaniu z żelazem, tworzy mieszaninę barwy szarej. Zbliżony do jej powierzchni magnes przyciąga pył żelaza. Po ogrzaniu, mieszanina się zapala. Żar obejmuje ją całą. Po zakończeniu tego procesu powstaje masa o czarnej barwie. Magnes z nią nie oddziałuje.
Wnioski:
Postawiona hipoteza jest prawdziwa. Mieszanie siarki z żelazem jest przemianą fizyczną, a w wyniku ogrzania mieszaniny tych substancji zachodzi reakcja chemiczna, dzięki której powstaje nowa substancja – siarczek żelaza() – o odmiennych właściwościach od substancji wyjściowych (użytych w doświadczeniu).
Podsumowanie:
Wymieszanie siarki z żelazem nie prowadzi do powstania nowej substancji, ale do utworzenia mieszaniny, którą możemy rozdzielić na składniki, wykorzystując np. magnes (żelazo, w przeciwieństwie do siarki, wykazuje właściwości magnetyczne). Po ogrzaniu do wysokiej temperatury, mieszanina zapala się, dzięki czemu powstaje czarna masa. Magnes z nią nie oddziałuje. Podczas ogrzewania, w mieszaninie zachodzi zatem reakcja chemiczna – siarka reaguje z żelazem. Powstaje nowa substancja, która – w przeciwieństwie do żelaza – nie wykazuje właściwości magnetycznych.
Jak możemy opisać reakcje chemiczne?
Chemicy znaleźli uniwersalny sposób opisywania przemian chemicznych podczas których jedne substancje przemieniają się w inne. Każdą reakcję chemiczną można opisać słownie lub za pomocą tak zwanych równań reakcji chemicznych.
Substancje, które ulegają przemianie chemicznej, nazywamy substratami, a te, które powstają w jej wyniku, określa się mianem produktów. W zapisie równania rozpatrywanej reakcji chemicznej za pomocą strzałki (→) pokazujemy kierunek przemiany – od substancji, które wzięły udział w reakcji chemicznej (od substratów), do substancji, które powstały w jej wyniku (do produktów). Poniżej znajduje się ogólny (uproszczony) schemat zapisu równania reakcji chemicznej.
W równaniu reakcji chemicznej substraty znajdują się zawsze po lewej stronie strzałki, produkty zaś po prawej. Strzałka skierowana jest od substratów do produktów.
W doświadczeniu z siarki i zawartego w powietrzu tlenu otrzymaliśmy tlenek
siarki(). Przebieg tej reakcji możemy opisać schematycznie w poniższy sposób.
Zapis ten odczytujemy następująco: siarka reaguje (łączy się) z tlenem zawartym w powietrzu i powstaje tlenek siarki(). Siarka i tlen są zatem substratami zachodzącej reakcji chemicznej, a tlenek siarki() jej produktem.
W zapisie równań reakcji, nad strzałką można zapisać warunki niezbędne do ich przebiegu. W rozpatrywanym przykładzie, aby z siarki i tlenu mógł powstać tlenek siarki(), siarkę ogrzewano w płomieniu palnika. Proces ogrzewania można uwzględnić w schematycznym zapisie:
Doświadczenie , które polega na ogrzewaniu siarki z żelazem, doprowadziło do powstania siarczku żelaza(). Tę przemianę chemiczną możemy przedstawić za pomocą następującego schematu równania reakcji:
co można odczytać w następujący sposób: siarka reaguje (łączy się) z żelazem, w wyniku czego powstaje siarczek żelaza(). Siarka i żelazo to substraty analizowanej reakcji chemicznej, a siarczek żelaza() jest jej produktem.
Nie zawsze w wyniku zachodzącej reakcji chemicznej z dwóch substratów otrzymuje się jeden produkt (jak to miało miejsce w opisanych przykładach). W zależności od przemiany, w reakcji chemicznej może wziąć udział jeden lub kilka substratów. Podobnie w przypadku produktów – może ich powstać kilka.
Przykładowo, podczas przygotowywania chleba na zakwasie lub ciasta drożdżowego, na skutek działania wytwarzanych przez drożdże enzymów, zachodzi tak zwana fermentacja alkoholowa. Jest to reakcja chemiczna, w wyniku której cukier prosty (glukoza) ulega przemianie w etanol i tlenek węgla() (dwutlenek węgla). Reakcję tę można opisać schematem:
W doświadczeniu opisanym w sekcji „dla zainteresowanych”, substancja o nazwie wodorowęglan sodu (główny składnik sody oczyszczonej), reagując z kwasem octowym (składnikiem octu), tworzy tlenek węgla() oraz substancję o nazwie octan sodu.
Wszystkie substancje uczestniczące w reakcji chemicznej (a więc zarówno substraty, jak i produkty reakcji) nazywamy reagentami.
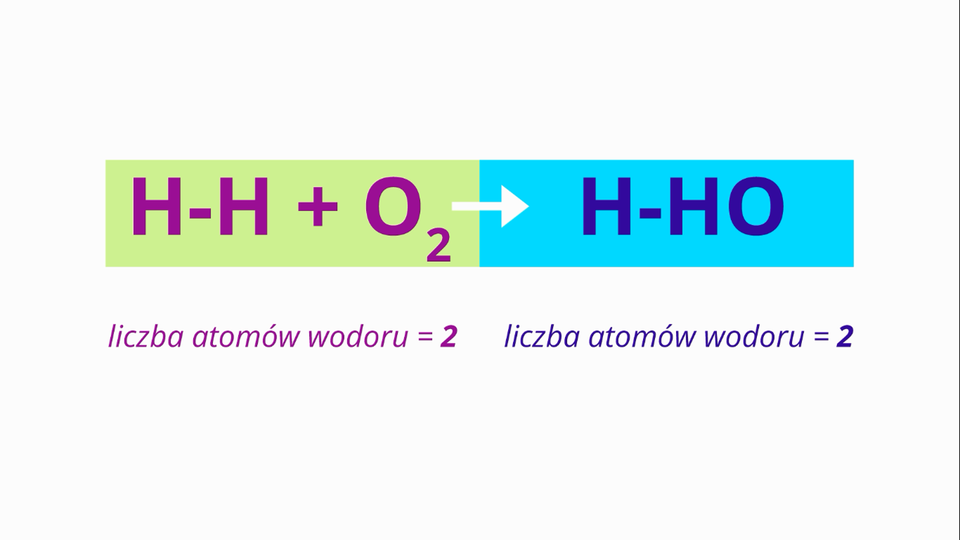
W jaki sposób zbilansować (uzgodnić) równanie reakcji otrzymywania wody z wodoru i tlenu? Zapoznaj się z poniższym filmem, a następnie rozwiąż ćwiczenie.
Film dostępny pod adresem /preview/resource/R2LHSRPgd5atn
Na filmie ukazano, w jaki sposób poprawnie uzgodnić równanie reakcji na przykładzie reakcji wodoru z tlenem.
Jak nazywamy reakcję, w wyniku której substancje łączą się ze sobą, tworząc jeden związek chemiczny?
Przyjrzyj się poniższym równaniom reakcji:
Zauważ, że w wyniku tych przemian z dwóch substratów otrzymuje się jeden produkt. Można je opisać poniższym równaniem:
O takich przemianach mówi się, że są to reakcje syntezy lub inaczej reakcje łączenia.
W poniższej galerii przedstawiono przykłady reakcji syntezy.
Jak nazywamy reakcję chemiczną, w wyniku której z jednej substancji powstaje kilka produktów?
W odpowiednich warunkach woda ulega reakcji, w wyniku której powstają pierwiastki, z jakich się składa. Przebieg tej reakcji opisuje równanie:
Zauważmy, że w omawianej reakcji z jednej substancji (wody) powstają dwie inne (tlen i wodór).
Przemiana chemiczna, podczas której z jednego substratu powstają co najmniej dwa produkty, nazywana jest reakcją rozkładu lub reakcją analizy. Można ją opisać za pomocą schematu:
Obejrzyj film, a następnie zaznacz produkty rozkładu tlenku rtęci.

Film dostępny pod adresem /preview/resource/Rih29SnQGcBoL
Na filmie ukazano reakcję analizy na przykładzie reakcji rozkładu tlenku rtęci dwa, w wyniku której powstała rtęć oraz tlen.
Tlenek rtęci ulega reakcji rozkładu zgodnie z poniższym równaniem reakcji:
Co to są reakcje wymiany?
Przyjrzyj się poniższym równaniom reakcji.
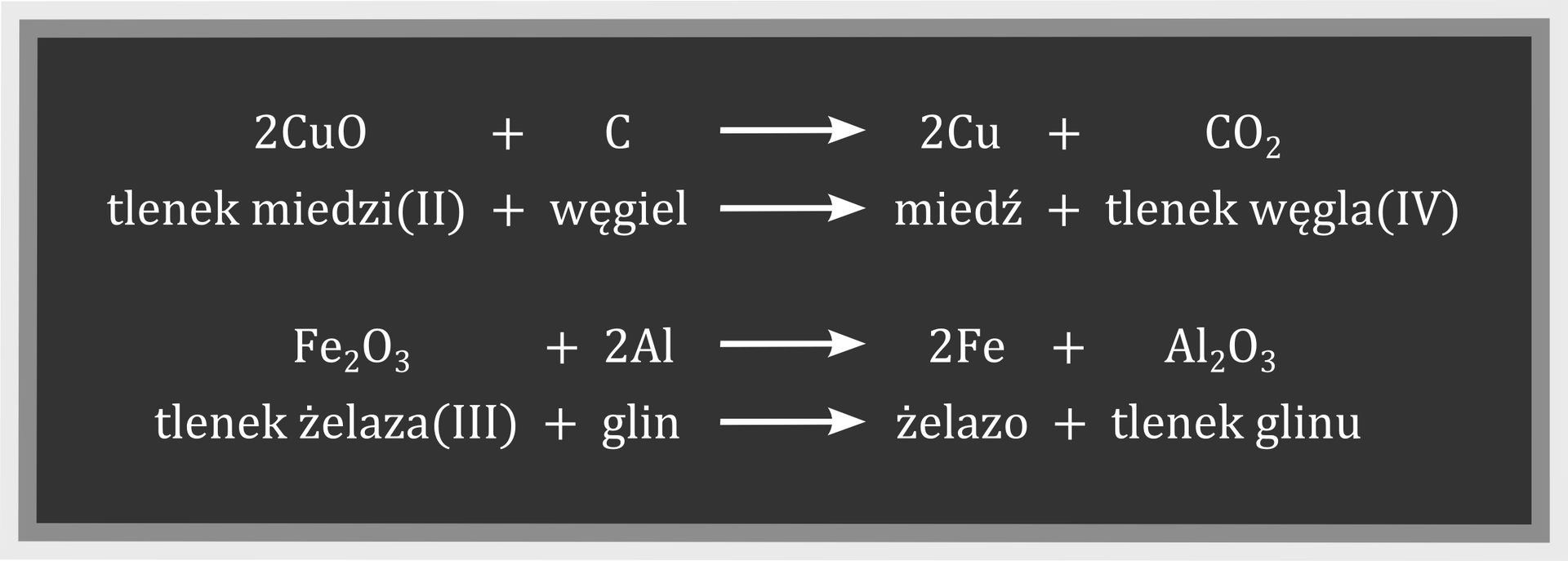
Przedstawione reakcje przebiegają według schematu:
O tego typu reakcjach mówi się, że są to reakcje wymiany.
Przeprowadź doświadczenie chemiczne polegające na sprawdzeniu, czy reakcja pomiędzy tlenkiem ołowiu a węglem jest przykładem reakcji wymiany.
Przeprowadzono doświadczenie chemiczne polegające na sprawdzeniu, czy reakcja pomiędzy tlenkiem ołowiu a węglem jest przykładem reakcji wymiany. Zapoznaj się z poniższym opisem doświadczenia, a następnie wykonaj polecenie.
Problem badawczy:
Czy reakcja tlenku węgla z węglem jest przykładem reakcji wymiany?
Hipoteza:
Reakcja tlenku węgla z węglem jest przykładem reakcji wymiany.
Co było potrzebne:
węgiel drzewny;
tlenek ołowiu;
łopatka metalowa;
palnik gazowy.
Przebieg doświadczenia:
W kawałku węgla drzewnego wykonano wgłębienie (okruchy wybrane z wgłębienia pozostawiono w celu wykorzystania w dalszej części doświadczenia). Wprowadzono do wgłębienia niewielką ilość tlenku ołowiu, tak aby wypełnił je tylko częściowo. Wymieszano tlenek ołowiu z okruchami pozostałego węgla drzewnego za pomocą łopatki. Zapalono palnik gazowy i skierowano gorący płomień na mieszaninę tlenku ołowiu z węglem. Obserwowano zachodzące zmiany.
Obserwacje:
Ogrzewany w płomieniu palnika węgiel drzewny rozżarza się. Po pewnym czasie na powierzchni mieszaniny tlenku ołowiu z węglem drzewnym pojawiają się srebrzyste kuleczki.
Wnioski:
Pod wpływem wysokiej temperatury tlenek ołowiu reaguje z węglem i powstaje ołów, który wydziela się z mieszaniny reakcyjnej w postaci srebrzystych kuleczek. Węgiel utlenia się i przekształca się w tlenek węgla. Przebieg tej reakcji opisuje równanie:
Wśród reakcji wymiany wyróżnia się reakcje wymiany pojedynczej i reakcje wymiany podwójnej. Pierwszy rodzaj, reakcja wymiany pojedynczej, jest przemianą, podczas której dwa substraty (pierwiastek i związek chemiczny) przekształcają się w dwa produkty (nową substancję prostą i złożoną). Jej przebieg można opisać za pomocą następującego schematu:
Równanie reakcji chemicznej | Zapis słowny przebiegu reakcji |
|---|---|
Druga grupa to reakcje wymiany podwójnej. Zachodzą one wtedy, gdy dwie substancje złożone przekształcają się w dwa nowe związki chemiczne. Poniższy schemat obrazuje przebieg reakcji wymiany podwójnej:
Równanie reakcji chemicznej | Zapis słowny przebiegu reakcji |
|---|---|