Tlenki – budowa, nazewnictwo i właściwości fizyczne
Zapewne nie są Ci obce takie nazwy jak korund, rubin, czy szafir..., a może też wapno palone, biel cynkowa, minia ołowiowa, glejta ołowiana, rutyl, biel tytanowa. Niektóre z tych nazw kojarzą Ci się zapewne z jubilerstwem, inne z budownictwem, spawalnictwem, zabezpieczeniami antykorozyjnymi, pigmentami do farb, a jeszcze inne z medycyną. Jest także nazwa woda, która powinna Ci sie kojarzyć z życiem. Pod tymi nazwami zwyczajowymi kryją się okresślone substancje chemiczne, które można zaliczyć do jednej, wspólnej kategorii, a mianowicie tlenków.
Związki pierwiastków z tlenem
- Nazwa kategorii: Związki pierwiastków z tlenem
- Nazwa kategorii: tlenki
- Nazwa kategorii: proste
- Nazwa kategorii: np. N a indeks dolny, dwa, koniec indeksu dolnego, O – tlenek sodu Koniec elementów należących do kategorii proste
- Nazwa kategorii: mieszane
- Nazwa kategorii: np. F e indeks dolny, trzy, koniec indeksu dolnego, O indeks dolny, cztery, koniec indeksu dolnego – tlenek żelaza(dwa, trzy), N indeks dolny, dwa, koniec indeksu dolnego, O – tlenek azotu(jeden, dwa) N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego – tlenek azotu(cztery, dwa) Koniec elementów należących do kategorii mieszane
- Nazwa kategorii: ponadtlenki
- Nazwa kategorii: np. K O indeks dolny, dwa, koniec indeksu dolnego – ponadtlenek potasu, N a O indeks dolny, dwa, koniec indeksu dolnego – ponadtlenek sodu Koniec elementów należących do kategorii ponadtlenki
- Nazwa kategorii: nadtlenki
- Nazwa kategorii: np. H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego – nadtlenek wodoru, N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego – nadtlenek sodu, B a O indeks dolny, dwa, koniec indeksu dolnego – nadtlenek baru Koniec elementów należących do kategorii nadtlenki
- Nazwa kategorii: fluorki
- Nazwa kategorii: np. O F indeks dolny, dwa, koniec indeksu dolnego Koniec elementów należących do kategorii fluorki
- Elementy należące do kategorii Związki pierwiastków z tlenem
- Elementy należące do kategorii tlenki
- Elementy należące do kategorii proste
- Elementy należące do kategorii mieszane
- Elementy należące do kategorii ponadtlenki
- Elementy należące do kategorii nadtlenki
- Elementy należące do kategorii fluorki
Tlenki
Tlenki to związki tlenu z innymi pierwiastkami, w których atomy tlenu występują na minus drugim ( ) stopniu utlenienia. Wzór ogólny tlenków prostych ma postać:
gdzie:
– oznacza symbol dowolnego pierwiastka chemicznego,
, – odpowiednie indeksy stechiometryczne.
- Nazwa kategorii: tlenki
- Nazwa kategorii: niemetali
- Nazwa kategorii: np. C O – tlenek węgla(dwa) Koniec elementów należących do kategorii niemetali
- Nazwa kategorii: metali
- Nazwa kategorii: S c indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego – tlenek skandu(trzy) Koniec elementów należących do kategorii metali
- Elementy należące do kategorii tlenki
- Elementy należące do kategorii niemetali
- Elementy należące do kategorii metali
Właściwości fizyczne wybranych tlenków
Poniżej znajdują się informacje przedstawiające wybrane właściwości fizyczne tlenków. Przeanalizuj poniższe informacje i zwróć uwagę na temperatury topnienia i wrzenia. Które z tlenków mają wysokie wartości temperatur topnienia i wrzenia, a które niskie?Zastanów się co może być przyczyną tych rozbieżności.
Tlenki stałe
Tlenki ciekłe
Z tlenkiem, występującym naturalnie w postaci cieczy, masz styczność na co dzień. Co więcej – masz go właściwie na wyciągnięcie ręki. A dokładnie: pod skórą. Tym tlenkiem jest dobrze znana woda (). Bez niej nie byłoby możliwe rozwinięcie się życia na Ziemi w takiej formie, jaką znamy obecnie. Organizm ludzki składa się z ok. 70% tego tlenku.
Tlenki gazowe
Większość niemetali tworzy tlenki, które występują w postaci gazowej. Za każdym razem, robiąc wydech powietrza z płuc, uwalniasz tlenek węgla(IV) – bezbarwny, bezwonny gaz. Bardzo niebezpiecznym jest tlenek węgla(II) , inaczej nazywany czadem. To bezwonny, bezbarwny gaz, który powstaje w wyniku niecałkowitego spalenia gazu ziemnego. Dlatego w łazienkach ogrzewanych gazem powinien być zamontowany czujnik czadu. Jego toksyczne działanie polega na nieodwracalnym łączeniu się z czerwonymi krwinkami, uniemożliwiając tym samym przenoszenie tlenu.
Tlenek azotu(I) znany jest z użycia w gazach rozweselających. To również bezbarwny, bezwonny gaz. Inny, tlenek azotu(IV), jest brunatnym gazem o nieprzyjemnym zapachu. Jest bardzo toksyczny dla organizmów żywych, ponadto powoduje opady kwaśnego deszczu.
Ustal wzór sumaryczny związku pierwiastka z tlenem na podstawie jego nazwy.
Nadtlenek baru.
Tlenek chromu().
W poniższej tabeli zaprezentowane zostały maksymalne wartości stopni utlenienia pierwiastków w ich związkach z tlenem.
Numer grupy w układzie okresowym | |||||||
|---|---|---|---|---|---|---|---|
Najwyższy stopień utlenienia atomów pierwiastka w tlenkach |
Indeks dolny Tabela 1. Maksymalne wartości stopni utlenienia pierwiastków w ich związkach z tlenem. Indeks dolny koniecTabela 1. Maksymalne wartości stopni utlenienia pierwiastków w ich związkach z tlenem.
Jak tworzy się nazwy tlenków prostych?
Nomenklatura chemiczna stanowi zbiór zasad nadawania nazw substancjom chemicznym, jest niezwykle ważna w nauce i pozwala na usystematyzowanie wszystkich związków chemicznych. Międzynarodową organizacją, która zajmuje się standaryzacją nazewnictwa i symboliki związków chemicznych, jest IUPAC (Międzynarodowa Unia Chemii Czystej i Stosowanej, ang. International Union of Pure and Applied Chemistry).
W systemie Stocka nazwy tlenków są dwuczłonowe, podaje się je poprzez połączenie ze sobą słowa „tlenek” z nazwą pierwiastka chemicznego w dopełniaczu, przykładowo:
– tlenek sodu.
Jeśli dany pierwiastek chemiczny tworzy więcej niż jeden tlenek po dwuczłonowej nazwie w nawiasie, należy podać stopień utlenienia (w postaci cyfry rzymskiej) pierwiastka w danym tlenku (bez spacji między drugim członem nazwy a nawiasem z podanym stopniem utlenienia), przykładowo:
– tlenek żelaza() oraz - tlenek żelaza()
Jak zapisać wzór tlenku na podstawie jego nazwy?
Ustal wzór sumaryczny tlenku siarki() oraz tlenku chromu() na podstawie jego nazwy.
Rozwiązanie
Zacznijmy od tlenku siarki(). Najpierw zapiszmy symbole pierwiastków budujących tlenek siarki(), a nad nimi zaznaczmy stopnie utlenienia, na których występują atomy tych pierwiastków w naszym związku.

Następnie sprawdźmy, że (6) znajdujący się nad symbolem siarki może ulec skróceniu z wartością stopnia utlenienia tlenu w tlenkach, a więc z (-2). Oczywiście po skróceniu otrzymamy i .

Teraz możemy skorzystać z reguły “na krzyż” i zapisać wzór tlenku w miejsce cyfr rzymskich stosując cyfry arabskie.
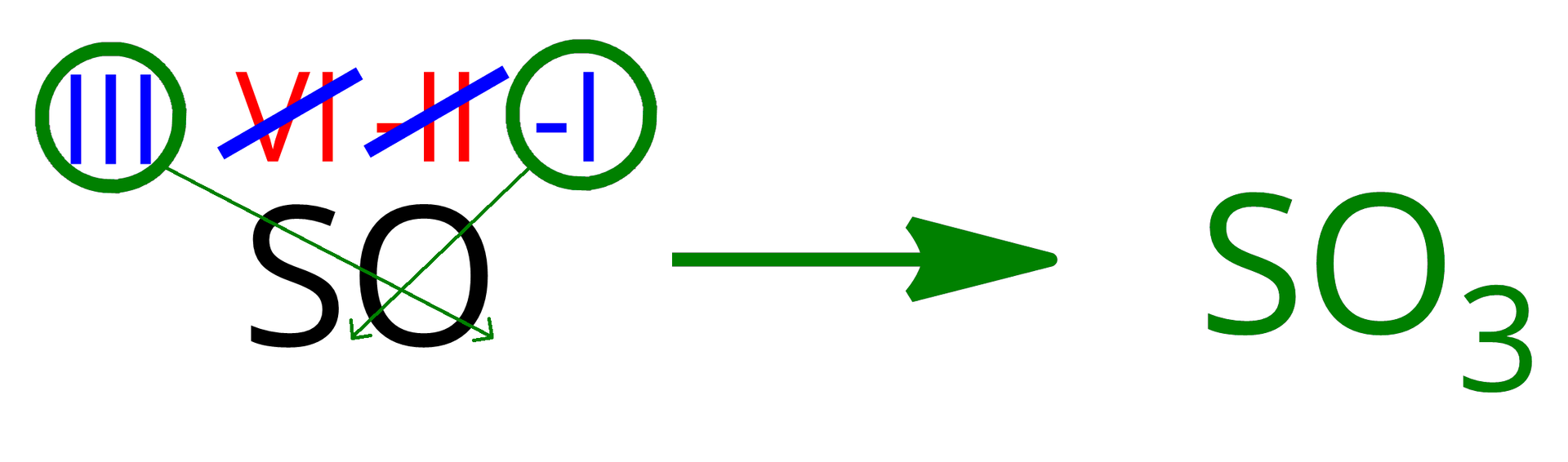
Przeprowadź samodzielnie analogiczną analizę dla tlenku chromu(). Tym razem jednak nie skraca się z , zatem operacja “na krzyż” doprowadzi nas do wzoru .
Ustal nazwę tlenku na podstawie jego wzoru sumarycznego:
Rozwiązanie:
1.
Dla metali grupy stopień utlenienia w związkach chemicznych zawsze wynosi , dlatego nie zapisujemy wartości stopnia utlenienia, pisząc nazwę tlenku. Podobnie rzecz ma się w przypadku tlenków metali grupy oraz tlenku glinu i tlenku cynku.
Zatem tlenek nosi nazwę: tlenek litu.
2.
W przypadku siarki musimy obliczyć stopień utlenienia jej atomów w związku , czynimy to wykorzystując definicje tlenków jako związków, w których atomy tlenu występują zawsze na stopniu utlenienia. Oznaczmy stopień utlenienia siarki jako „x”.
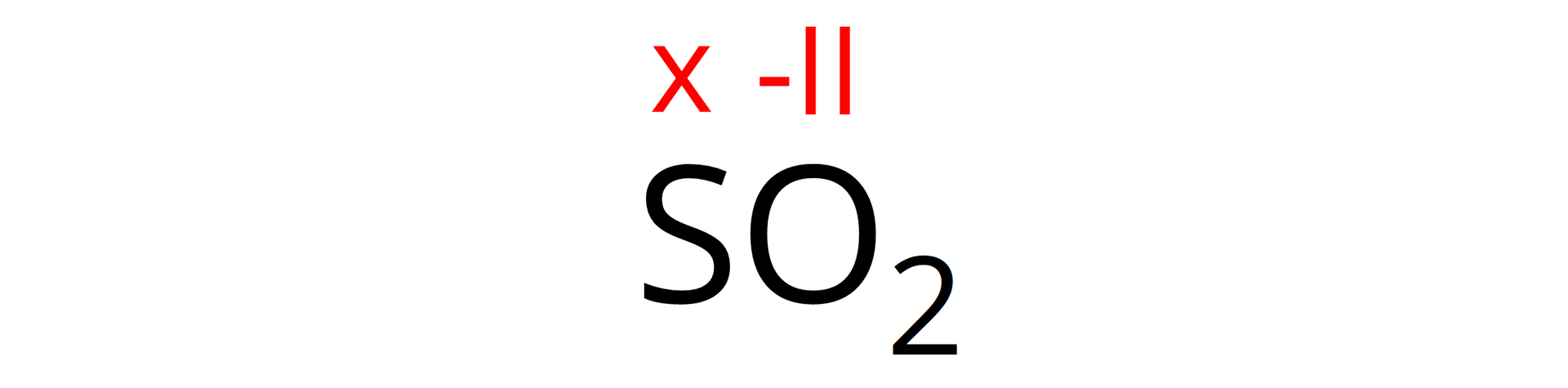
Wiemy, że suma stopni utlenienia wszystkich atomów wchodzących w skład związku obojętnego elektrycznie jest równa 0.
Możemy zatem ułożyć równanie:
Wynika z tego, że atomy siarki w cząsteczce występują na stopniu utlenienia. Nazwa tego tlenku to zatem: tlenek siarki().
3.
W analogiczny sposób przeprowadzamy analizę dla tlenku , tym razem stopień utlenienia atomów azotu oznaczmy w postaci niewiadomej „y”.
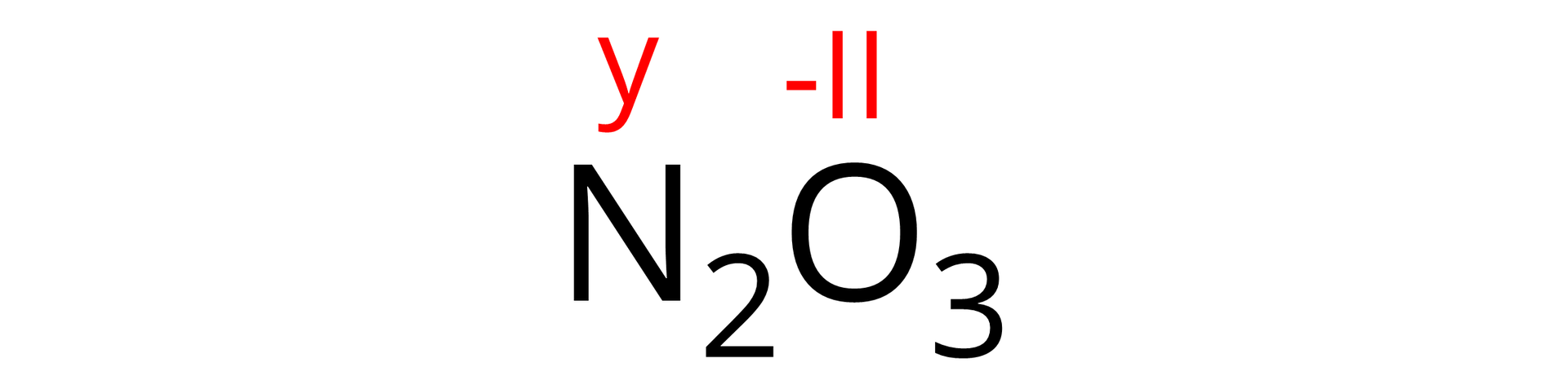
Wiemy, że suma stopni utlenienia wszystkich atomów wchodzących w skład związku obojętnego elektrycznie jest równa 0.
Możemy zatem ułożyć równanie:
Wynika z tego, że atomy azotu w cząsteczce występują na III stopniu utlenienia. Nazwa tego tlenku to zatem: tlenek azotu().
Zestawienie przykładowych nazw i wzorów tlenków znajduje się poniżej. Przeanalizuj w jaki sposób wartosć stopnia utlenienia atomów ma odzwierciedlenie w nazwie i wzorze tlenku.
Nazwa tlenku (wg Systemu Stocka) | Wzór tlenku | Stopień utlenienia atomów pierwiastka w tlenku |
|---|---|---|
tlenek sodu | ||
tlenek litu | ||
tlenek wapnia | ||
tlenek magnezu | ||
tlenek skandu() | ||
tlenek tytanu() | ||
tlenek wanadu() | ||
tlenek chromu() | ||
tlenek manganu() | ||
tlenek żelaza() | ||
tlenek kobaltu() | ||
tlenek niklu() | ||
tlenek miedzi() | ||
tlenek cynku | ||
tlenek glinu | ||
tlenek węgla() | ||
tlenek węgla() | ||
tlenek ołowiu() | ||
tlenek ołowiu() | ||
tlenek azotu() | ||
tlenek azotu() | ||
tlenek azotu() | ||
tlenek siarki() | ||
tlenek siarki() | ||
tlenek chloru() | ||
tlenek chloru() | ||
tlenek chloru() |
Czy potrafisz sprawnie posługiwać się nazwami tlenków oraz zapisywać ich wzory sumaryczne? Sprawdź się w poniższej grze!
Czy potrafisz sprawnie posługiwać się nazwami tlenków oraz zapisywać ich wzory? W grze edukacyjnej należy podać nazwy dla wybranych wzorów sumarycznych tlenków oraz wartości stopni utlenienia atomu pierwiastka tworzącego z tlenem tlenek: , , , , , , , , .
Informacja do zadania
Tlenki to związki tlenu z innymi pierwiastkami, w których atomy tlenu występują na minus drugim stopniu utlenienia (zapis cyframi rzymskimi). Wzór ogólny tlenków prostych ma postać: , gdzie X to symbol dowolnego pierwiastka chemicznego, n,m oznaczają odpowiednie indeksy stechiometryczne. W systemie Stocka nazwy tlenków są dwuczłonowe, podaje się je poprzez połączenie ze sobą słowa „tlenek” z nazwą pierwiastka chemicznego w dopełniaczu, przykładowo: , czyli tlenek sodu. Jeśli dany pierwiastek chemiczny tworzy więcej niż jeden tlenek po dwuczłonowej nazwie w nawiasie należy podać stopień utlenienia w postaci cyfry rzymskiej, bez spacji między drugim członem nazwy a nawiasem z podanym stopniem utlenienia, przykładowo: tlenek żelaza() oraz tlenek żelaza().
Tlenki mieszane
Dla niektórych pierwiastków, np. dla żelaza i ołowiu, oprócz tlenków prostych, występują również tlenki mieszane, w których atomy danego pierwiastka występują na więcej niż jednym stopniu utlenienia. Dla takich związków nazwy tworzone są analogicznie, jak dla tlenków prostych, należy jednak podać wartości obydwu stopni utlenienia metalu. Do przykładów takich tlenków należą: – tlenek żelaza(,), – tlenek ołowiu(,), – tlenek ołowiu(,).
Napisz nazwy tlenków, których wzory podano poniżej.
































