Rozpuszczalność substancji
Mówimy o niektórych substancjach, że bardzo dobrze rozpuszczają się w wodzie. Nie znaczy to jednak, że mieszają się z nią w nieograniczonym stosunku.

definicję roztworu właściwego;
sposób otrzymywania roztworu właściwego;
czynniki wpływające na szybkość rozpuszczania substancji w wodzie.
rozróżniać pojęcia: roztworu nasyconego, roztworu nienasyconego oraz roztworu rozcieńczonego i roztworu stężonego,
opisywać zmiany rozpuszczalności ciał stałych i gazów w wodzie, w zależności od temperatury;
interpretować krzywe rozpuszczalności w celu określenia rozpuszczalności substancji.
1. Czy w tej samej ilości wody rozpuszcza się taka sama ilość każdej substancji?
Przeprowadź doświadczenie chemiczne, które będzie polegać na sprawdzeniu, czy w tej samej ilości wody rozpuszcza się taka sama ilość każdej substancji. Wybierz hipotezę, zweryfikuj ją, zapisz obserwacje i wnioski.
Zapisz hipotezę, obserwację i wnioski z doświadczenia.
Wykonano doświadczenie, w którym zbadano, czy wszystkie substancje rozpuszczają się w wodzie w tym samym stopniu.
Problem badawczy: Czy w określonej objętości (masie) wody można rozpuścić jednakową masę różnych substancji?
Hipoteza: W tej samej objętości (masie) wody rozpuszczają się niejednakowe masy różnych substancji.
Co było potrzebne:
cztery zlewki;
cztery bagietki;
cztery łyżeczki;
woda;
uwodniony siarczan() miedzi() ;
chlorek sodu (sól kuchenna);
cukier spożywczy (sacharoza);
jodek potasu.
Uwaga!
Uwodniony siarczan() miedzi() to sól, która w sieci krystalicznej zawiera cząsteczki wody. Nazywamy ją hydratem. Siarczan() miedzi() tworzy hydrat o wzorze , co oznacza, że na każdy kation miedzi oraz anion siarczanowy() w krysztale przypada pięć cząsteczek wody. Hydrat ten ma intensywne niebieskie zabarwienie, natomiast bezwodny jest biały. W dalszych etapach edukacji dowiesz się więcej na temat hydratów.
Przebieg doświadczenia:
Do czterech zlewek o jednakowej pojemności wlano taką samą objętość wody ().
Do każdej z nich wsypano po następujących substancji:
do zlewki – uwodnionego siarczanu() miedzi();
do zlewki – chlorku sodu;
do zlewki – cukru spożywczego;
do zlewki – jodku potasu.
Zawartość wszystkich zlewek mieszano w identyczny sposób za pomocą pręcików szklanych.
Obserwowano szybkość rozpuszczania poszczególnych substancji.
Hipoteza:
Postawiona hipoteza okazała się prawdziwa. W tej samej objętości (masie) wody rozpuszczają się niejednakowe masy różnych substancji.
Obserwacje:
Substancje ulegały rozpuszczeniu z różną szybkością. Po pewnym czasie chlorek sodu, cukier i jodek potasu uległy całkowitemu rozpuszczeniu. W zlewce z uwodnionym siarczanem() miedzi() pozostały nierozpuszczone kryształy.
Wnioski:
Substancje charakteryzują się różną rozpuszczalnością w wodzie.
2. Czy ilość substancji rozpuszczanej zależy od temperatury rozpuszczalnika?
Przeprowadź doświadczenie chemiczne, które będzie polegać na sprawdzeniu, czy ilość substancji, jaka ulegnie rozpuszczeniu, zależy od temperatury rozpuszczalnika. Wybierz hipotezę, zweryfikuj ją, zapisz obserwacje i wnioski.
Zapisz hipotezę, obserwację i wnioski z doświadczenia.
Zbadano wpływ temperatury na rozpuszczanie substancji stałej w wodzie na przykładzie azotanu() potasu.
Problem badawczy: Czy temperatura ma wpływ na ilość substancji stałej (azotanu() potasu), jaką można rozpuścić w określonej objętości wody?
Hipoteza: Im wyższa temperatura wody, tym więcej azotanu() potasu można w niej rozpuścić.
Co było potrzebne:
dwie zlewki;
dwie bagietki
łyżeczka;
palnik (czajnik);
płytka ceramiczna;
woda;
azotan() potasu.
Przebieg doświadczenia:
Do dwóch zlewek wlano po wody różniącej się temperaturą (np. i ).
Następnie do każdej zlewki wsypano po azotanu() potasu.
Zawartość obu zlewek mieszano w identyczny sposób za pomocą pręcików szklanych.
Obserwowano szybkość rozpuszczania poszczególnych substancji.
Hipoteza: Postawiona hipoteza okazała się prawdziwa. Im wyższa temperatura wody, tym więcej azotanu() potasu można w niej rozpuścić.
Obserwacje: Azotan() potasu nie rozpuścił się całkowicie w chłodnej wodzie, natomiast w ciepłej – rozpuścił się całkowicie.
Wnioski: Ilość substancji rozpuszczonej w wodzie zależy od temperatury i w przypadku azotanu() potasu rośnie wraz z jej wzrostem.
Przeprowadź doświadczenie chemiczne, które będzie polegać na sprawdzeniu, jaki wpływ na rozpuszczanie gazu (tlenku węgla(IV)) w wodzie ma temperatura. Wybierz hipotezę, zweryfikuj ją, zapisz obserwacje i wnioski.
Zapisz hipotezę, obserwację i wnioski z doświadczenia.
Przeprowadzono doświadczenie, w którym zbadano jaki wpływ na rozpuszczanie gazu (tlenku węgla()) w wodzie ma temperatura.
Problem badawczy: Jaki wpływ na rozpuszczanie gazu (tlenku węgla()) w wodzie ma temperatura?
Hipoteza: Im wyższa temperatura wody, tym mniej gazu się w niej rozpuści (ilość gazu rozpuszczonego w wodzie maleje wraz ze wzrostem temperatury).
Co było potrzebne:
trzy zlewki;
woda gazowana schłodzona w lodówce;
woda wodociągowa schłodzona w lodówce;
woda wodociągowa o temperaturze pokojowej;
wodę wodociągowa o temperaturze (wrzątek).
Uwaga!
Pamiętaj o zachowaniu ostrożności, aby uniknąć oparzenia wrzątkiem.
Przebieg doświadczenia:
Do trzech zlewek o identycznej pojemności wlano jednakową objętość schłodzonej w lodówce wody gazowanej (kilkadziesiąt ).
Do każdej z nich dodano taką samą objętość wody wodociągowej o różnej temperaturze:
do pierwszej zlewki – wodę schłodzoną w lodówce;
do drugiej zlewki – wodę o temperaturze pokojowej;
do trzeciej zlewki – wodę o temperaturze około (wrzątek).
Obserwowano pojawianie się pęcherzyków gazu w zlewkach oraz ich ilość.
Obserwacje:
W pierwszej zlewce nie pojawiły się pęcherzyki gazu. W drugiej i trzeciej zlewce pojawiły się pęcherzyki gazu, ale w zlewce trzeciej było ich znacznie więcej.
Hipoteza:
Postawiona hipoteza okazała się prawdziwa. Im wyższa temperatura wody, tym mniej gazu się w niej rozpuści (ilość gazu rozpuszczonego w wodzie maleje wraz ze wzrostem temperatury).
Wnioski:
Po dodaniu gorącej wody do wody mineralnej, wzrasta jej temperatura i wydzielają się z niej pęcherzyki gazu. Im wyższa była temperatura dodanej wody, tym więcej wydzielało się gazu. Wraz ze wzrostem temperatury maleje ilość gazu rozpuszczonego w wodzie.

Film dostępny pod adresem /preview/resource/R5JTMNxsNVE5u
Na stole laboratoryjnym znajdują się trzy zlewki o jednakowej objętości oraz butelka wody mineralnej. Do pierwszej wlewana jest schłodzona woda, do drugiej woda o temperaturze pokojowej, a do trzeciej woda gazowana. W zlewce drugiej i trzeciej wydzielają się pęcherzyki gazu. W trzeciej jest ich najwięcej.
Ilość substancji, która może ulec rozpuszczeniu w wodzie, zależy od temperatury. W przypadku gazów ilość ta maleje wraz ze wzrostem temperatury, natomiast dla ciał stałych wielkość ta na ogół rośnie.
3. Roztwór nasycony i nienasycony
Jeśli w roztworze wodnym znajduje się maksymalna ilość substancji rozpuszczonej, a kolejna dodana porcja nie ulegnie już rozpuszczeniu, to mamy do czynienia z roztworem nasyconymroztworem nasyconym. Każdy inny roztwór, który nie osiągnął stanu nasycenia, określa się mianem roztworu nienasyconegoroztworu nienasyconego.
Z uwagi na zależność między ilością substancji rozpuszczonej a jej temperaturą, roztwór, który jest nasycony w temperaturze niższej, nie będzie nim w temperaturze wyższej, w której najczęściej może rozpuścić się więcej substancji.

Chemicy posługują się także określeniami roztworów odnoszącymi się do ilości rozpuszczonej w nich substancji. Wyróżniają na tej podstawie:
roztwór stężonyroztwór stężony, w którym ilość substancji rozpuszczonej jest identyczna jak w roztworze nasyconym lub niewiele mniejsza;
roztwór rozcieńczonyroztwór rozcieńczony, czyli roztwór, który zawiera co najmniej kilkakrotnie mniej substancji niż roztwór stężony.
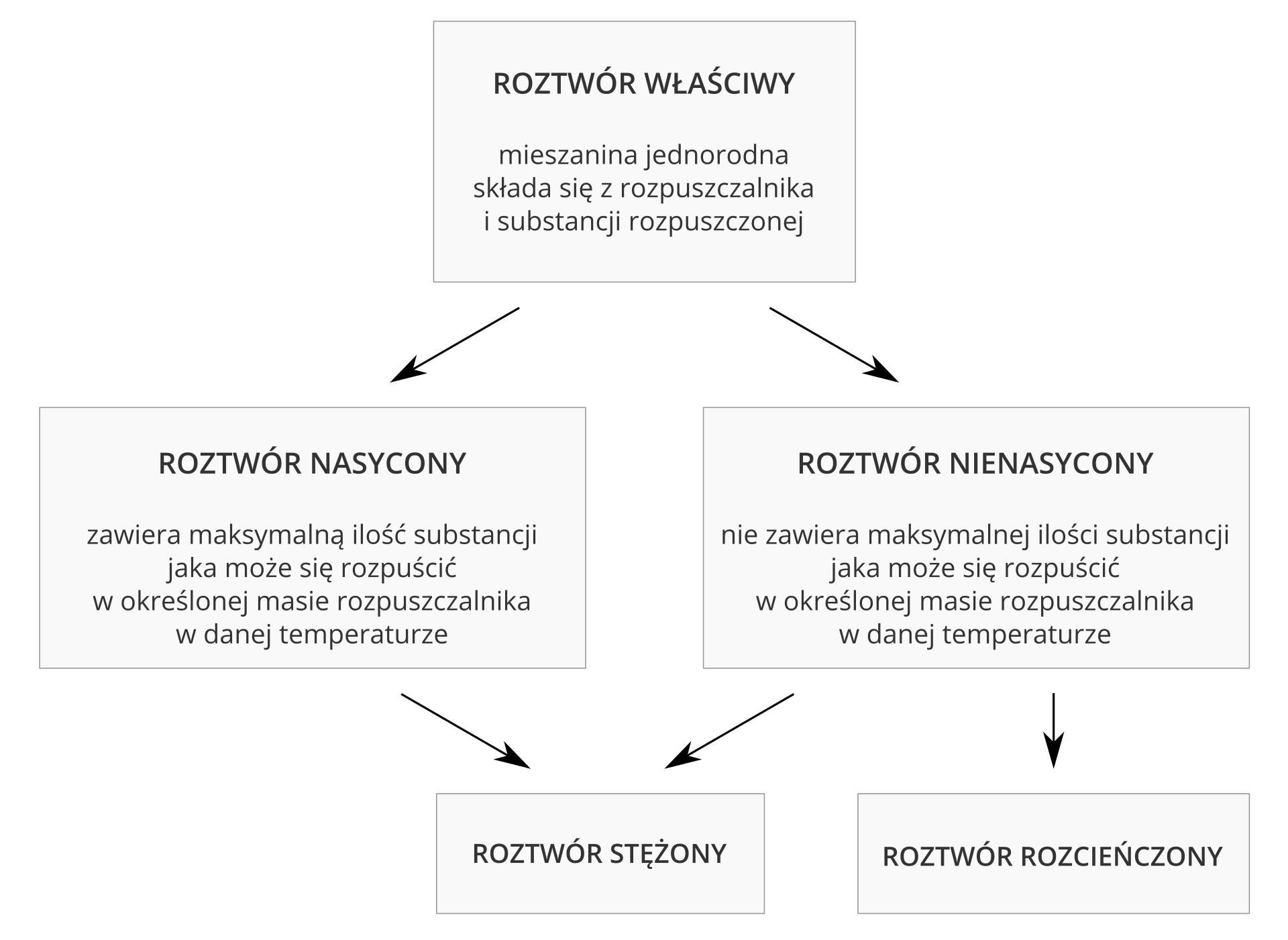
Każdy roztwór nasycony jest roztworem stężonym, ale nie każdy roztwór stężony jest nasyconym.
Każdy roztwór rozcieńczony jest jednocześnie nienasyconym, ale roztworem nienasyconym może być zarówno roztwór rozcieńczony, jak i stężony.

Połącz w pary typy roztworów z ich charakterystyką.
4. Rozpuszczalność
Niektóre substancje, jak na przykład propan--on (aceton), czy etanol mieszają się z wodą w nieograniczonej ilości. Jednak większość związków chemicznych wykazuje ograniczoną rozpuszczalność w wodzie. Są substancje, które rozpuszczają się w niej tylko w niewielkim stopniu (np. w ilości w wody). Istnieją też dobrze rozpuszczalne substancje, których ilość w roztworze może przekraczać nawet czterokrotnie masę wody.
Miarą zdolności substancji do rozpuszczania się w wodzie jest rozpuszczalnośćrozpuszczalność. Określa ona maksymalną ilość substancji, jaka może rozpuścić się w ustalonej masie lub objętości rozpuszczalnika w danej temperaturze i pod stałym ciśnieniem. W tablicach fizycznych i chemicznych rozpuszczalność jest najczęściej wyrażana jako liczba gramów substancji, którą można rozpuścić w wody w danej temperaturze i pod stałym ciśnieniem. Dane te zostały wyznaczone doświadczalnie.
Temperatura | Chlorek sodu | Cukier | Siarczan miedzi | Azotan potasu | Azotan sodu | Jodek potasu | Octan sodu | Chlorek potasu |
Źródło: na podstawie W. Mizerski, Tablice chemiczne, Warszawa 2003 | ||||||||
Temperatura | Dwutlenek węgla | Tlen | Azot | Wodór |
– | ||||
– | ||||
– | ||||
– | ||||
Źródło: na podstawie W. Mizerski, Tablice chemiczne, Warszawa 2003 | ||||
Narysuj wykres zależności rozpuszczalności substancji gazowych w wodzie od temperatury. W tym celu skorzystaj z powyższej tabeli.
Rozpuszczalność tlenu w wody w temperaturze wynosi: Możliwe odpowiedzi: 1. ., 2. ., 3. ., 4. .
Na podstawie danych zawartych w tabelach, opisz zależność rozpuszczalności ciał stałych i gazów od temperatury, uzupełniając poniższe zdania.
Wraz ze wzrostem temperatury rozpuszczalność gazów w wodzie 1. rośnie, 2. rośnie lub maleje, 3. maleje.
5. Krzywe rozpuszczalności
Na podstawie danych liczbowych przedstawiających zależność rozpuszczalności substancji od temperatury, sporządza się wykres nazywany krzywą rozpuszczalnościkrzywą rozpuszczalności.
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
azotan() potasu (linia czerwona):
–
–
–
–
–
–
–
–
–
–
–
jodek potasu (linia jasnozielona):
–
–
–
–
–
–
–
–
–
–
–
chlorek sodu (sól kuchenna) (linia pomarańczowa):
–
–
–
–
–
–
–
–
–
–
–
chlorek potasu (linia niebieska):
–
–
–
–
–
–
–
–
–
–
–
azotan() sodu (linia fioletowa):
–
–
–
–
–
–
–
–
–
–
–
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
octan sodu (linia pomarańczowa):
–
–
–
–
–
–
sacharoza (cukier) (linia żółtopomarańczowa):
–
–
–
–
–
–
szczawian amonu (linia żółtozielona):
–
–
–
–
–
–
Krzywa rozpuszczalności pozwala określić, jak zmienia się rozpuszczalność danej substancji w zależności od temperatury. Dostarcza również informacji o tym, czy jest to zmiana znaczna czy niewielka. Z wykresu odczytuje się maksymalną ilość substancji, jaką można rozpuścić w wody w określonej temperaturze.
W temperaturze równej rozpuszczalność jodku potasu wynosi , co można zapisać jako ). Co oznacza ten zapis? Wybierz prawidłową odpowiedź.
Oczyszczanie substancji – krystalizacja
Otrzymywane w laboratorium związki chemiczne zazwyczaj nie są czyste i zawierają niewielkie ilości innych substancji, nazywanych zanieczyszczeniami. Aby otrzymać czysty produkt, jako metodę oczyszczania stosuje się m.in. krystalizację. Polega ona na tym, że w odpowiednio dobranym rozpuszczalniku, w temperaturze jego wrzenia, rozpuszcza się zanieczyszczoną substancję, otrzymując tym samym jej nasycony roztwór.
Następnie mieszaninę sączy się na gorąco i pozostawia w spokoju przez pewien czas. W trakcie powolnego ochładzania mieszaniny, substancja wydziela się z roztworu w postaci kryształów, a zanieczyszczenia pozostają w roztworze.
Warunkiem koniecznym do przeprowadzenia krystalizacji jest dobranie takiego rozpuszczalnika, w którym dana substancja będzie się łatwo rozpuszczała się w wysokich temperaturach, a już w niższych – słabo. Ponadto ów rozpuszczalnik – niezależnie od temperatury – będzie bardzo dobrze rozpuszczał zanieczyszczenia.

Podczas krystalizacji substancja wydziela się powoli z roztworu
Podsumowanie
W takiej samej objętości wody rozpuszczają się różne ilości rozmaitych substancji.
Ilość substancji stałej, rozpuszczonej w wodzie, zależy od temperatury i najczęściej rośnie wraz z jej wzrostem.
Wraz ze wzrostem temperatury maleje ilość rozpuszczonego w wodzie gazu.
Roztwór, który w danej temperaturze zawiera maksymalną ilość substancji rozpuszczonej, a kolejna dodana porcja substancji nie ulega rozpuszczeniu, nazywamy roztworem nasyconym.
Roztwór, który w danej temperaturze nie zawiera maks. ilości substancji rozpuszczonej i w którym możliwe jest rozpuszczenie dodatkowej porcji substancji, to roztwór nienasycony.
Roztwór rozcieńczony zawiera co najmniej kilkakrotnie mniej substancji niż roztwór stężony.
W roztworze stężonym ilość substancji rozpuszczonej jest taka sama jak w roztworze nasyconym lub niewiele mniejsza.
Maksymalna ilość substancji, jaka może rozpuścić się w ustalonej masie lub objętości rozpuszczalnika w danej temperaturze i pod stałym ciśnieniem, nazywa się rozpuszczalnością. Może być wyrażana jako liczba gramów substancji, jaką można rozpuścić w rozpuszczalnika w danej temperaturze i pod stałym ciśnieniem.
Wykres przedstawiający zależność rozpuszczalności danej substancji od temperatury nazywa się krzywą rozpuszczalności.
Przygotuj nasycony roztwór cukru w wodzie w wybranej temperaturze.
Oblicz, jaką masę ma roztwór nasycony chlorku sodu w temperaturze , który powstał przez rozpuszczenie odpowiedniej ilości substancji w wody.
Słownik
wykres przedstawiający zależność rozpuszczalności danej substancji od temperatury
określa maks. ilość substancji, jaka może rozpuścić się w rozpuszczalnika w danej temperaturze i pod stałym ciśnieniem
roztwór, który w danej temperaturze zawiera maks. ilość substancji rozpuszczonej, a dodana kolejna do niej porcja nie ulega rozpuszczeniu
roztwór, który w danej temperaturze nie zawiera maks. ilości substancji rozpuszczonej i w którym można rozpuścić dodatkową jej porcję
roztwór, który zawiera co najmniej kilkakrotnie mniej substancji rozpuszczonej niż roztwór stężony
roztwór, w którym ilość substancji rozpuszczonej jest taka sama jak w roztworze nasyconym lub niewiele mniejsza
Ćwiczenia
Uzupełnij luki w tekście. Wybierz właściwe określenia spośród podanych.
temperatury, roztworu, objętości roztworu, rozpuszczalnika, masy substancji rozpuszczonej, rozpuszczalności, substancji rozpuszczonej, masy rozpuszczalnika, roztworu, masy substancji rozpuszczonej, rozpuszczalnika, substancji rozpuszczonej, masy rozpuszczalnika
Rozpuszczalność to ilość .......................................................... znajdującej/ego się w 100 g ........................................................... Krzywa rozpuszczalności przedstawia zależność .......................................................... od ...........................................................
Na podstawie wykresu rozpuszczalności, uszereguj substancje wg rozpuszczalności (rosnąco) w temperaturze .
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
azotan() potasu (linia czerwona):
–
–
–
–
–
–
–
–
–
–
–
jodek potasu (linia jasnozielona):
–
–
–
–
–
–
–
–
–
–
–
chlorek sodu (sól kuchenna) (linia pomarańczowa):
–
–
–
–
–
–
–
–
–
–
–
chlorek potasu (linia niebieska):
–
–
–
–
–
–
–
–
–
–
–
azotan() sodu (linia fioletowa):
–
–
–
–
–
–
–
–
–
–
–
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
octan sodu (linia pomarańczowa):
–
–
–
–
–
–
sacharoza (cukier) (linia żółtopomarańczowa):
–
–
–
–
–
–
szczawian amonu (linia żółtozielona):
–
–
–
–
–
–
Rozpuszczalność pewnej substancji maleje wraz ze wzrostem temperatury. Na podstawie tej informacji oceń, czy podane zdania są prawdziwe, czy fałszywe.
| Prawda | Fałsz | |
| Roztwór, który w temperaturze 10°C jest roztworem nasyconym, po ogrzaniu do temperatury 50°C stanie się roztworem nienasyconym. | □ | □ |
| Podczas schładzania roztworu nasyconego wydzieli się z niego rozpuszczona substancja. | □ | □ |
| Aby z roztworu nasyconego o temperaturze 20°C otrzymać roztwór nasycony o temperaturze70°C, konieczne będzie dodanie substancji po ogrzaniu roztworu. | □ | □ |
| W 100 g rozpuści się więcej substancji, jeśli woda będzie miała wyższą temperaturę. | □ | □ |
| Roztwór, który w temperaturze 60°C jest roztworem nasyconym, w temperaturze niższej stanie się roztworem nienasyconym. | □ | □ |
Proces krystalizacji jest jedną z metod oczyszczania substancji. Polega na rozpuszczeniu zanieczyszczonej substancji w odpowiednio dobranym rozpuszczalniku, w wysokiej temperaturze. Podczas stygnięcia, oczyszczana substancja wydziela się z roztworu, a zanieczyszczenia pozostają w rozpuszczalniku.
Na podstawie powyższych informacji, oceń, które zdania dotyczące rozpuszczalnika zawierają informacje prawdziwe, a które fałszywe.
Proces krystalizacji jest jedną z metod oczyszczania substancji. Polega na rozpuszczeniu w wysokiej temperaturze zanieczyszczonej substancji w odpowiednio dobranym rozpuszczalniku. Podczas stygnięcia, oczyszczana substancja wydziela się z roztworu, a zanieczyszczenia pozostają w rozpuszczalniku.
Na podstawie powyższych informacji, oceń, które zdania dotyczące substancji oczyszczanej zawierają informacje prawdziwe, a które fałszywe.
Przeprowadzono doświadczenie, które pozwaliło sprawdzić, czy woda wodociągowa zawiera rozpuszczony gaz. W tym celu do dwóch naczyń wlano właśnie tę wodę. Jedno naczynie zaczęto podgrzewać, a drugie włożono do miski wypełnionej lodem.
Wybierz i zaznacz obserwacje i wnioski, które mogły zostać zapisane podczas przeprowadzania doświadczenia chemicznego.
Bibliografia
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy ósmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac edukacja 2020.