Sole – otrzymywanie
Sole posiadają budowę jonową. Składają się z kationu (najczęściej metalu lub innych kationów, np. amonu , uranylu lub kationów organicznych typu , gdzie to np. , , a to dowolna grupa organiczna) i anionu reszty kwasowej. Aby otrzymać sól, potrzebujesz obu jonów. Zastanów się, z jakich związków możesz je pozyskać? W naszych rozważaniach pozostaniemy przy najbardziej typowych solach, w których kationem jest jon metalu.
Zapisując równanie reakcji, w której chcemy otrzymać sól zawierającą kation metalu, musimy się zastanowić, jakich substancji możemy użyć, aby w układzie reakcyjnym był obecny pożądany kation. Poniżej podano przykłady typów substancji chemicznych, jakich możemy ku temu użyć:
Przykłady substancji, z których można pozyskać kationy metali i aniony reszt kwasowych, wchodzących w skład związków, jakimi są sole
- Nazwa kategorii: kation metalu{id=1}{value=32}
- Nazwa kategorii: wodorotlenek{links=1}{value=20}
- Nazwa kategorii: NaOH{value=8}
- Nazwa kategorii: Ca(OH)[subscript]2[/]{value=8}
- Nazwa kategorii: KOH{value=8}
- Nazwa kategorii: Cu(OH)[subscript]2[/]{value=8}
- Nazwa kategorii: Mg(OH)[subscript]2[/]{value=8}
- Nazwa kategorii: Fe(OH)[subscript]2[/]{value=8}
- Nazwa kategorii: LiOH{value=8}
- Nazwa kategorii: Ba(OH)[subscript]2[/]{value=8}
- Nazwa kategorii: Zn(OH)[subscript]2[/]{value=8} Koniec elementów należących do kategorii wodorotlenek{links=1}{value=20}
- Nazwa kategorii: sól{links=1}{value=20}
- Nazwa kategorii: Na[subscript]2[/]SO[subscript]4[/]{value=8}
- Nazwa kategorii: AgNO[subscript]3[/]{value=8}
- Nazwa kategorii: CuSO[subscript]4[/]{value=8}
- Nazwa kategorii: BaCl[subscript]2[/]{value=8}
- Nazwa kategorii: CaCO[subscript]3[/]{value=8}
- Nazwa kategorii: K[subscript]2[/]CO[subscript]3[/]{value=8}
- Nazwa kategorii: NaCl{value=8}
- Nazwa kategorii: Na[subscript]2[/]S{value=8}
- Nazwa kategorii: CuCl[subscript]2[/]{value=8} Koniec elementów należących do kategorii sól{links=1}{value=20}
- Nazwa kategorii: tlenek metalu{links=1}{value=20}{color=#66CC99}
- Nazwa kategorii: K[subscript]2[/]O{value=8}
- Nazwa kategorii: MgO{value=8}
- Nazwa kategorii: CuO{value=8}
- Nazwa kategorii: Fe[subscript]2[/]O[subscript]3[/]{value=8}
- Nazwa kategorii: CaO{value=8}
- Nazwa kategorii: Li[subscript]2[/]O{value=8}
- Nazwa kategorii: Na[subscript]2[/]O{value=8} Koniec elementów należących do kategorii tlenek metalu{links=1}{value=20}{color=#66CC99}
- Nazwa kategorii: metal{links=1}{value=20}{color=#66CCCC}
- Nazwa kategorii: Mg{value=8}
- Nazwa kategorii: Zn{value=8}
- Nazwa kategorii: Al{value=8}
- Nazwa kategorii: Fe{value=8}
- Nazwa kategorii: Cu{value=8}
- Nazwa kategorii: Cr{value=8}
- Nazwa kategorii: Pb{value=8} Koniec elementów należących do kategorii metal{links=1}{value=20}{color=#66CCCC}
- Elementy należące do kategorii kation metalu{id=1}{value=32}
- Elementy należące do kategorii wodorotlenek{links=1}{value=20}
- Elementy należące do kategorii sól{links=1}{value=20}
- Elementy należące do kategorii tlenek metalu{links=1}{value=20}{color=#66CC99}
- Elementy należące do kategorii metal{links=1}{value=20}{color=#66CCCC}
Analogicznie, aby wprowadzić konkretny anion, możemy wybierać spośród substancji zebranych poniżej:
- Nazwa kategorii: anion reszty kwasowej
- Nazwa kategorii: niemetal
- Nazwa kategorii: S
- Nazwa kategorii: Cl
- Nazwa kategorii: I Koniec elementów należących do kategorii niemetal
- Nazwa kategorii: sól
- Nazwa kategorii: Na[baseline‑shift: sub; font‑size: smaller;]2[/]SO[baseline‑shift: sub; font‑size: smaller;]4[/]
- Nazwa kategorii: AgNO[baseline‑shift: sub; font‑size: smaller;]3[/]
- Nazwa kategorii: CuSO[baseline‑shift: sub; font‑size: smaller;]4[/]
- Nazwa kategorii: BaCl[baseline‑shift: sub; font‑size: smaller;]2[/]
- Nazwa kategorii: CaCO[baseline‑shift: sub; font‑size: smaller;]3[/]
- Nazwa kategorii: K[baseline‑shift: sub; font‑size: smaller;]2[/]CO[baseline‑shift: sub; font‑size: smaller;]3[/]
- Nazwa kategorii: NaCl
- Nazwa kategorii: Na[baseline‑shift: sub; font‑size: smaller;]2[/]S
- Nazwa kategorii: CuCl[baseline‑shift: sub; font‑size: smaller;]2[/] Koniec elementów należących do kategorii sól
- Nazwa kategorii: tlenek niemetalu
- Nazwa kategorii: CO[baseline‑shift: sub; font‑size: smaller;]2[/]
- Nazwa kategorii: SO[baseline‑shift: sub; font‑size: smaller;]2[/]
- Nazwa kategorii: Mn[baseline‑shift: sub; font‑size: smaller;]2[/]O[baseline‑shift: sub; font‑size: smaller;]7[/]
- Nazwa kategorii: P[baseline‑shift: sub; font‑size: smaller;]4[/]O[baseline‑shift: sub; font‑size: smaller;]10[/]
- Nazwa kategorii: Cl[baseline‑shift: sub; font‑size: smaller;]2[/]O[baseline‑shift: sub; font‑size: smaller;]5[/]
- Nazwa kategorii: N[baseline‑shift: sub; font‑size: smaller;]2[/]O[baseline‑shift: sub; font‑size: smaller;]5[/] Koniec elementów należących do kategorii tlenek niemetalu
- Nazwa kategorii: kwas
- Nazwa kategorii: HCl
- Nazwa kategorii: H[baseline‑shift: sub; font‑size: smaller;]2[/]SO[baseline‑shift: sub; font‑size: smaller;]4[/]
- Nazwa kategorii: HNO[baseline‑shift: sub; font‑size: smaller;]3[/]
- Nazwa kategorii: CH[baseline‑shift: sub; font‑size: smaller;]3[/]COOH Koniec elementów należących do kategorii kwas
- Elementy należące do kategorii anion reszty kwasowej
- Elementy należące do kategorii niemetal
- Elementy należące do kategorii sól
- Elementy należące do kategorii tlenek niemetalu
- Elementy należące do kategorii kwas
Metody otrzymywania soli
Jeżeli połączysz 2 powyższe mapy pocjęciowe, otrzymasz 10 metod otrzymywania soli – ale pamiętaj, metody te mają swoje ograniczenia! Nie każdą z nich można otrzymać każdą z soli.
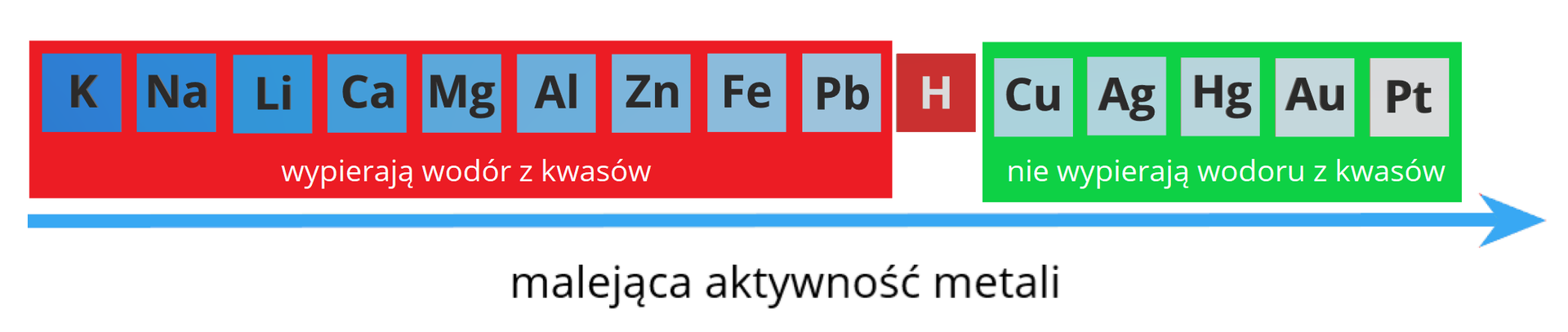
Reakcje metali z kwasami
Reakcji z wydzieleniem wodoru będą ulegały tylko metale o ujemnych wartościach potencjału. Pozostałe metale nie wypierają wodoru z kwasów. , , i mogą jednak reagować ze stężonym, gorącym kwasem siarkowym(VI) oraz z rozcieńczonym i stężonym kwasem azotowym(V). W reakcjach tych nie powstaje jednak wodór, ale odpowiednie tlenki
Inne metale, takie jak np. żelazo, również mogą reagować z kwasami silnie utleniającymi bez wydzielenia wodoru, np.:
Reakcje te przebiegają w dwóch etapach:
Etap 1: metal utlenia się do swojego tlenku;
Etap 2: tlenek metalu reaguje z kwasem, dając odpowiednią sól. Dlatego też metale ulegające pasywacji, nie roztwarzają się w stężonym kwasie azotowym. Do takich przypadków należą: glin, chrom, żelazo oraz kobalt, nikiel i molibden. W rozcieńczonym roztworze pasywacja zachodzi w dużo mniejszym stopniu i roztworzenie metalu staje się bardziej prawdopodobne.

Reakcja tlenku zasadowego z kwasem bądź tlenku amfoteryczneg z mocnym kwasem
W wyniku reakcji powstaje sól i woda. Przykładowe równania reakcji:
Skutecznym produktem usuwającym rdzę jest... Cola! Wystarczy zanurzyć w niej przedmiot ze śladami rdzy na kilka minut, a następnie dokładnie wyszorować, umyć i osuszyć. Dzieje się tak za sprawą obecnego w niej kwasu ortofosforowego, który reaguje z rdzą (tlenkami żelaza).
Reakcja wodorotlenku z kwasem
W jej wyniku powstaje sól i woda. Jest to najbardziej uniwersalna metoda otrzymywania soli. Przykładowe równania reakcji:
Reakcja wodorotlenku z tlenkiem kwasowym
W reakcji tej otrzymać można tylko sole kwasów tlenowych. Przykładowe równania reakcji:
Reakcja tlenku kwasowego z tlenkiem zasadowym
W wyniku reakcji powstaje sól – tylko otrzymywanie soli kwasów tlenowych. Przykładowe równania reakcji
Reakcja metalu z niemetalem
Powstaje sól – tylko otrzymywanie soli kwasów beztlenowych. Przykładowe równania reakcji:
Reakcja metalu i rozpuszczalnej w wodzie soli mniej aktywnego metalu
Powstaje inna sól i inny metal (mówimy wtedy o wypieraniu metalu z roztworu jego soli). Przykładowe równania reakcji:
Reakcja soli z kwasem
Powstaje inna sól i inny kwas. Zachodzi, gdy powstała sól jest solą trudno rozpuszczalną w wodzie lub gdy sól biorąca udział w reakcji jest solą słabego kwasu i reaguje z mocnym kwasem. Przykładowe równania reakcji:
Reakcja wodorotlenku i soli
Powstają inna sól i inny wodorotlenek. Reakcja zachodzi w przypadku, gdy wszystkie substraty są rozpuszczalne, natomiast jeden z produktów – sól lub wodorotlenek – jest trudno rozpuszczalny. Przykładowe równania reakcji:
Reakcje między dwiema solami
Zachodzą one wówczas, gdy powstają sole trudniej rozpuszczalne od soli stanowiących substraty tych reakcji. Ponadto, substratami mogą być jedynie dobrze rozpuszczalne sole. Przykładowe równania reakcji:
Otrzymując sole, warto korzystać z tabeli rozpuszczalności
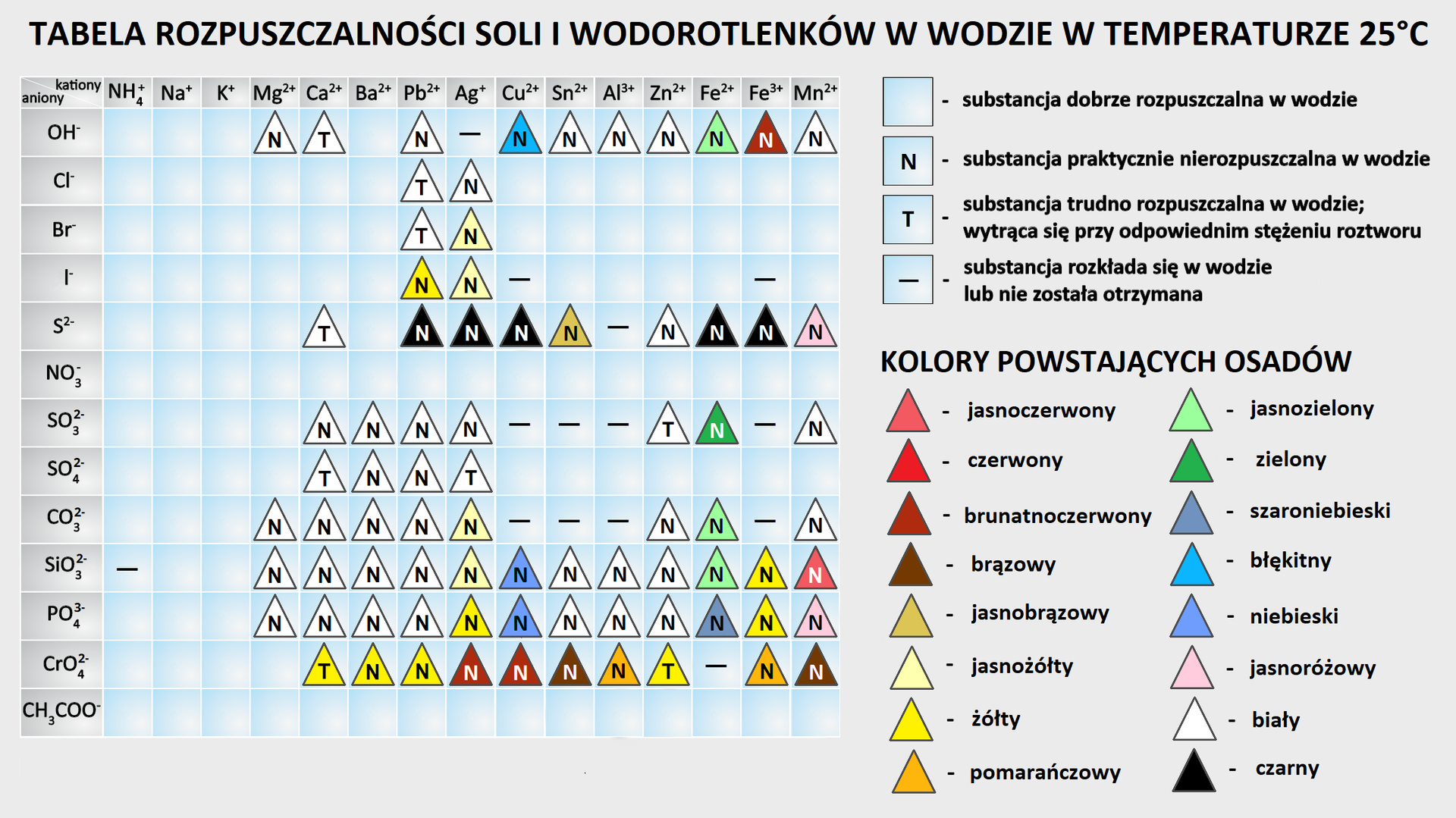
lub zapamiętać wynikające z niej reguły dla popularnych soli:
dobrze rozpuszczalne są sole litowców (sodu, potasu) i amonu;
dobrze rozpuszczalne są azotany, etaniany (octany) i chlorany;
większość siarczanów należy do dobrze rozpuszczalnych (wyjątkami są: , , );
do trudno rozpuszczalnych należą i ;
większość chlorków, bromków i jodków jest dobrze rozpuszczalna z wyjątkiem soli , i ;
większość siarczków metali jest trudno rozpuszczalna (dobrze rozpuszczalne są siarczki litowców, berylowców i amonu);
większość węglanów i ortofosforanów jest trudno rozpuszczalna, dobrze rozpuszczalne są węglany i ortofosforany litowców i amonu.
Umiejętność pisania i uzgadniania równań reakcji jest niezbędna w tzw. analizie chemicznej.
Zapoznaj się z możliwościami poniższego laboratorium chemicznego i zaproponuj doświadczenia, w wyniku przeprowadzenia których możesz otrzymać sole. Następnie zapoznaj się z problemem badawczym, sformułuj i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje, wyniki oraz zapisz wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D7PDSJDMV
Zapoznaj się z opisem serii eksperymentów przeprowadzanych w laboratorium chemicznym. Następnie zapoznaj się z problemem badawczym, sformułuj i zweryfikuj własną hipotezę. Na koniec rozwiąż krótkie zadania sprawdzające.
Analiza eksperymentu: Otrzymywanie siarczanu magnezu różnymi metodami.
Problem badawczy: Czy siarczan magnezu można otrzymać za pomocą sześciu różnych metod?
Hipoteza: Siarczan magnezu można otrzymać za pomocą sześciu różnych metod.
Sprzęt laboratoryjny:
probówki (6 sztuk) – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
pipety jednorazowe – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
roztwór kwasu siarkowego, siarczan miedzi – roztwór wodny, siarczek magnezu – roztwór wodny, wodorotlenek magnezu, tlenek magnezu, magnez.
Przebieg eksperymentu:
Probówka 1 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano magnezu.
Probówka 2 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano tlenku magnezu.
Probówka 3 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano wodorotlenku magnezu.
Probówka 4 – Umieszczono w probówce za pomocą pipety jednorazowej siarczanu miedzi, a następnie dodano magnezu.
Probówka 5 – Umieszczono w probówce za pomocą pipety jednorazowej siarczanu miedzi, a następnie dodano siarczku magnezu.
Probówka 6 – Umieszczono w probówce za pomocą pipety jednorazowej siarczku magnezu i dodano do niej roztworu kwasu siarkowego. Następnie ustaw nad probówkę uniwersalny papierek wskaźnikowy.
Obserwacje:
Probówka 1 . Magnez po wprowadzeniu do kwasu roztwarza się. Wydziela się bezbarwny gaz.
Probówka 2. Tlenek magnezu po wprowadzeniu do kwasu roztwarza się.
Probówka 3. Wodorotlenek magnezu po wprowadzeniu do kwasu roztwarza się.
Probówka 4. Magnez roztwarza się. Niebieski roztwór odbarwia się. Wytrąca się brunatnoczerwony (różowoczerwony) osad.
Probówka 5. Wytrąca się czarny osad. Niebieski roztwór odbarwia się.
Probówka 6. Wydziela się bezbarwny gaz o zapachu zgniłych jaj. Zwilżony wodą uniwersalny papierek wskaźnikowy zmienia zabarwienie na czerwone.
Wyniki:
Gazem wydzielającym się w probówce pierwszej jest wodór. W probówce czwartej roztwór zmienia kolor na jasnozielony, ze względu na powstającą w reakcji chemicznej miedź. Czarnym osadem pojawiającym się w probówce piątej jest siarczek miedzi. Wydzielającym się gazem w probówce szóstej, o charakterystycznym zapachu, jest kwas siarkowodorowy.
Wnioski:
Siarczan magnezu jest solą, którą można otrzymać za pomocą sześciu różnych metod. Hipoteza została potwierdzona.