Sole – właściwości fizyczne i chemiczne
Czy sole są odporne na działanie wysokich temperatur?
Czy wiesz, czy sole są odporne na działanie wysokich temperatur? Przy pomocy symulacji, sprawdź wpływ temperatury na niektóre z nich, a następnie wykonaj zamieszczone poniżej ćwiczenia.
Zapoznaj się z opisem poniższej symulacji interaktywnej, dotyczącej wpływu temperatury na sole.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5CKEQNT1
Uzupełnij poniższy dziennik. Zaproponuj hipotezę/hipotezy. Następnie rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zapisz cząsteczkowe równanie reakcji, zachodzącej podczas prażenia węglanu wapnia.
Zapisz cząsteczkowe równanie reakcji, zachodzącej podczas prażenia węglanu wapnia.
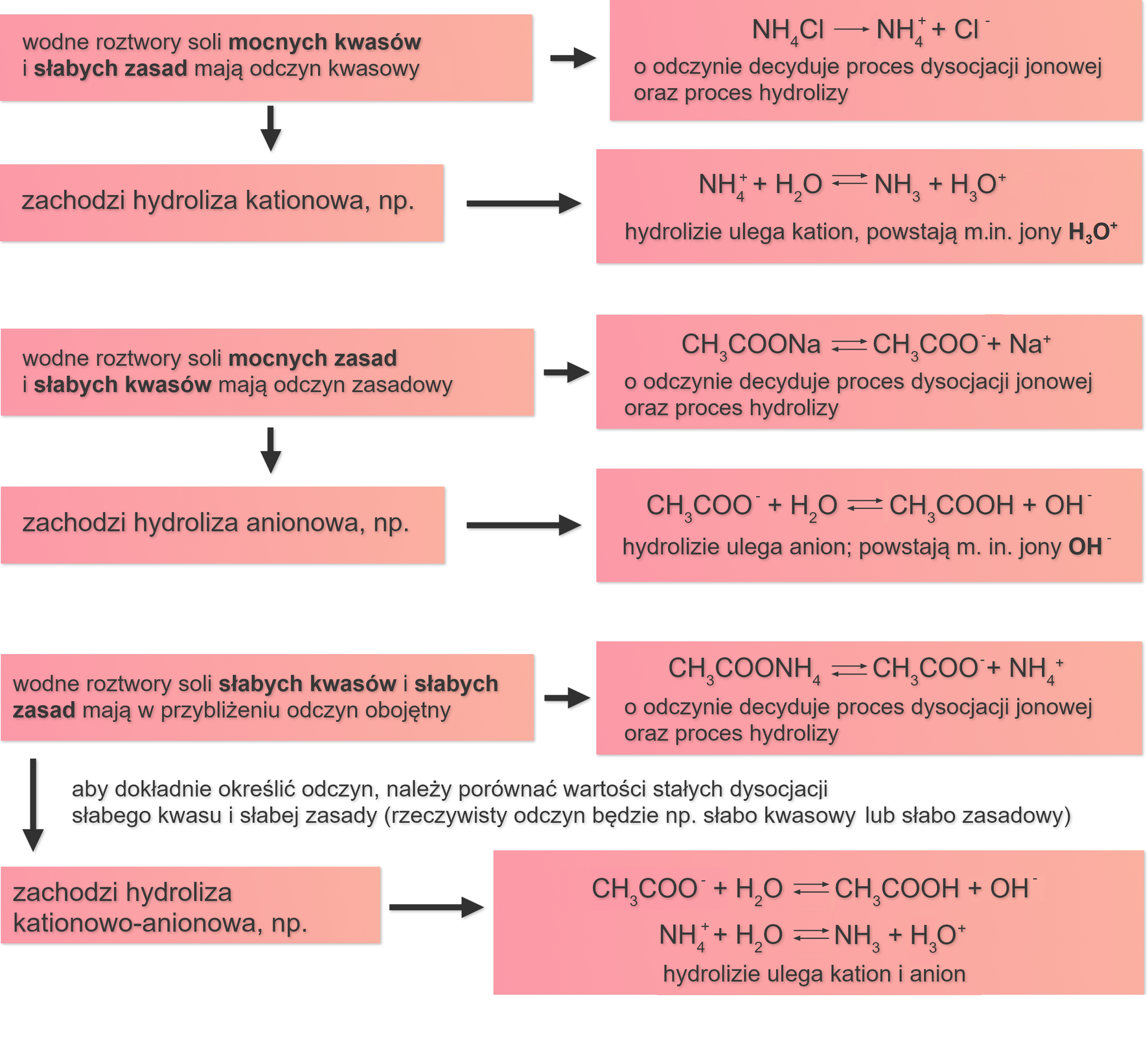
Przeanalizuj poniższy schemat hydrolizy wodnych roztworów różnych soli i odpowiedz na powyższe pytanie.
Przeanalizuj opis schematu hydrolizy wodnych roztworów różnych soli i odpowiedz na powyższe pytanie.
Hydroliza | ||
|---|---|---|
hydroliza kationowa – hydrolizie ulega kation | hydroliza anionowa – hydrolizie ulega anion | hydroliza kationowo‑anionowa – hydrolizie ulega kation i anion |
kwasowy odczyn roztworu | zasadowy odczyn roztworu | odczyn zbliżony do obojętnego |
sole pochodzące od mocnych kwasów i słabych zasad | sole pochodzące od mocnych zasad i słabych kwasów | sole pochodzące od słabych zasad i słabych kwasów |
Tabela 1. Hydroliza – podsumowanie
Indeks górny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Warszawa 2010. Indeks górny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Warszawa 2010.
Przeprowadź eksperyment w laboratorium chemicznym. Zapisz problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie sformułuj wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5CKEQNT1
Zadanie: Sprawdzenie, czy odczyn wszystkich soli jest obojętny.
Hipoteza: Odczyn soli nie zawsze jest obojętny.
Sprzęt laboratoryjny: zlewka (150 centymetrów sześciennych) - naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych; pH‑metr - urządzenie służące do pomiaru pH analizowanych substancji chemicznych; tryskawka - plastikowe naczynie zamknięte nakrętką z długą końcówką. Tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę; cylinder miarowy - podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy.
Badane substancje to roztwory wodne o stężeniach 1 mol na decymetr sześciennyIndeks górny 33, 0,5 mola na decymetr sześciennyIndeks górny 33 i 0,1 mola na decymetr sześciennyIndeks górny 33, następujących substancji: chlorek sodu, cyjanek sodu, fluorek sodu, wodorosiarczan(VI) sodu, chlorek amonu, fluorek amonu, azotan(III) potasu, siarczan(VI) potasu, węglan potasu, octan amonu, siarczan(IV) sodu.
Instrukcja: Wybrano roztwór do badania i przeniesiono go na blat stołu laboratoryjnego. Wybrano stężenie roztworu. Odmierzono cylindrem miarowym 50 centymetrów sześciennych wybranego roztworu i przenieś go do zlewki. Następnie przy użyciu pH‑metru sprawdzono pH roztworu. Przed i po dokonaniu pomiaru przemyto elektrodę wodą.
Wnioski: Odczyn soli zależy od jej rodzaju. Jeśli sól pochodzi od mocnego kwasu oraz mocnej zasady odczyn będzie obojętny (lub bliski obojętnego). Jeśli sól pochodzi od słabego kwasu i mocnej zasady odczyn będzie zasadowy, jeśli sól pochodzi od mocnego kwasu i słabej zasady to odczyn jest kwasowy. Ostatni przypadek to jeśli sól pochodzi od słabego kwasu i słabej soli to odczyn jest obojętny (lub bliski obojętnego).
Jak na wartość pH wpływa zmiana objętości i zmiana stężenia wodnych roztworów soli?
Jakie związki dysocjują?
- Nazwa kategorii: Dysocjacja[br]elektrolityczna
- Nazwa kategorii: związki[br]nieorganiczne
- Nazwa kategorii: sole[br]nieorganiczne
- Nazwa kategorii: sole[br]proste
- Nazwa kategorii: wodorosole
- Nazwa kategorii: hydroksosole Koniec elementów należących do kategorii sole[br]nieorganiczne
- Nazwa kategorii: kwasy[br]nieorganiczne
- Nazwa kategorii: wodorotlenki Koniec elementów należących do kategorii związki[br]nieorganiczne
- Nazwa kategorii: związki[br]organiczne
- Nazwa kategorii: sole[br]organiczne
- Nazwa kategorii: kwasy[br]karboksylowe
- Nazwa kategorii: aminy
- Nazwa kategorii: fenole
- Nazwa kategorii: aminokwasy Koniec elementów należących do kategorii związki[br]organiczne
- Elementy należące do kategorii Dysocjacja[br]elektrolityczna
- Elementy należące do kategorii związki[br]nieorganiczne
- Elementy należące do kategorii sole[br]nieorganiczne
- Elementy należące do kategorii związki[br]organiczne
- M e – metal;
- R – reszta kwasowa;
- M e indeks górny, m, plus, koniec indeksu górnego – kation metalu lub kation amonu (N H indeks dolny, cztery, koniec indeksu dolnego, indeks górny, plus, koniec indeksu górnego);
- m – wartościowość metalu;
- n – wartościowość reszty kwasowej.
Mol siarczan(sześć) potasu K indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego dysocjuje całkowicie na dwa mole kationów potasu i jeden mol anionów siarczanowych(sześć), zgodnie z równaniem:
W przypadku wodorosoli oraz hydroksosoli, reakcja dysocjacji zachodzi analogicznie jak dla obojętnych soli prostych.
- dysocjacja wodorosoli – wodorosiarczanu(sześć) sodu:
- dysocjacja hydroksosoli – chlorku wodorotlenku wapnia:
- Kwasy jednoprotonowe Kwasy jednoprotonowe ulegają reakcji dysocjacji elektrolitycznej pod wpływem wody. Schematyczne równanie można zapisać jako:
- H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego – kation oksoniowy;
- A indeks górny, minus, koniec indeksu górnego – anion reszty kwasowej.
- Kwasy wieloprotonowe Kwasy wieloprotonowe ulegają stopniowej reakcji dysocjacji pod wpływem wody. Przykładem jest kwas ortofosforowy(pięć) H indeks dolny, trzy, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego. Kwas ortofosforowy(pięć) jest kwasem trójprotonowym, w którym dysocjacja będzie zachodzić trójetapowo:
- w pierwszym etapie zachodzi reakcja zgodnie z poniższym równaniem:
H indeks dolny, trzy, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O strzałka w lewo nad strzałką w prawo H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, minus, koniec indeksu górnego
W tym przypadku równanie reakcji zapisujemy ze strzałkami skierowanymi w przeciwne strony, ponieważ kwas ortofosforowy(pięć) jest kwasem słabym. Jeśli jednak kwas jest mocny, jak np. kwas siarkowy(sześć) H indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego, to w pierwszym etapie równanie reakcji zapisujemy z jedną strzałką. - w kolejnym etapie zachodzi reakcja zgodnie z poniższym równaniem:
H indeks dolny, dwa, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, minus, koniec indeksu górnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O strzałka w lewo nad strzałką w prawo H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego, plus, H P O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, dwa, minus, koniec indeksu górnego - w ostatnim etapie zachodzi reakcja zgodnie z poniższym równaniem:
H P O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, dwa, minus, koniec indeksu górnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O strzałka w lewo nad strzałką w prawo H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego, plus, P O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, trzy, minus, koniec indeksu górnego
W przypadku mocnych kwasów reakcja dysocjacji elektrolitycznej zachodzi w stu procentach albo prawie w stu procentach, dlatego też, w przypadku mocnych kwasów, równania dysocjacji elektrolitycznej zapisujemy z jedną strzałką, skierowaną w stronę produktów. Dysocjacja elektrolityczna słabych kwasów nieorganicznych (np. H F) jest reakcją odwracalną i zachodzi tylko w pewnym, zwykle niewielkim stopniu. Z tego względu w równaniu reakcji stosuje się strzałki skierowane w przeciwne strony.
Przykład:
Dysocjacji w wodzie ulegają wodorotlenki metali aktywnych, np. K O H. Dla tego związku dysocjację zapisujemy zgodnie z równaniem:
Większość wodorotlenków dysocjuje całkowicie, wówczas równanie reakcji zapisujemy, stosując jedną strzałkę skierowaną w kierunku produktów. Zarówno wodorotlenki jedno-, jak i wielowodorotlenowe ulegają dysocjacji elektrolitycznej pod wpływem wody, ale w przeciwieństwie do kwasów, dysocjacja wodorotlenków wielowodorotlenowych nie jest stopniowa. Wyjątkiem jest wodorotlenek wapnia, który dysocjuje w dwóch etapach.
Kwasy karboksylowe to zazwyczaj słabe kwasy, co oznacza, że dysocjują częściowo. Proces dysocjacji jest reakcją odwracalną, dlatego w równaniu reakcji stosuje się strzałki skierowane w przeciwne strony. Schematycznie równanie reakcji dysocjacji elektrolitycznej kwasu karboksylowego możemy zapisać jako: Ilustracja przedstawiająca równanie reakcji dysocjacji kwasu karboksylowego. Cząsteczka kwasu karboksylowego zbudowanego z podstawnika R oraz grupy karboksylowej C O O H dodać cząsteczka wody H indeks dolny, dwa, koniec indeksu dolnego, O. Strzałka w prawo, strzałka w lewo, za strzałkami anion karboksylanowy zbudowany z grupy R połączonej z grupą C O O indeks górny, minus, koniec indeksu górnego dodać jon hydroniowy H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego., Aminy Aminy dysocjują zgodnie z równaniem:
Aminy to słabe zasady o mocy porównywalnej do amoniaku. Dysocjacja elektrolityczna amin jest reakcją odwracalną. Z tego względu w równaniu reakcji stosuje się strzałki skierowane w przeciwne strony., Aminokwasy Aminokwasy to wielofunkcyjne pochodne węglowodorów o wzorze ogólnym zbliżonym do:
- R – fragment węglowodorowy (może zwierać także inne grupy funkcyjne).
opisIlustracja przedstawiająca reakcję dysocjacji fenolu. Cząsteczka benzenolu (czyli fenolu) zbudowanego z sześcioczłonowego pierścienia aromatycznego podstawionego grupą hydroksylową O H. Dodać cząsteczkę wody H indeks dolny, dwa, koniec indeksu dolnego, O. Strzałka w prawo, strzałka w lewo, za strzałkami anion fenolanowy zbudowany z pierścienia fenylowego podstawionego atomem tlenu obdarzonym ładunkiem ujemnym dodać kation hydroniowy H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, plus, koniec indeksu górnego., Sole organiczne Wśród soli organicznych wyróżnić możemy:
- Mydła – sole metali lub kationu amonu oraz wyższych kwasów karboksylowych (kwasów tłuszczowych)
- R – fragment węglowodorowy nasycony lub nienasycony;
- m – wartościowość metalu;
- M e – metal lub kation amonu.
Wzór ogólny mydła:
Przykładem mydła, które rozpuszcza się w wodzie i dysocjuje na jony, jest palmitynian sodu, którego proces dysocjacji elektrolitycznej można przedstawić w postaci równania:
- Sole pozostałych kwasów karboksylowych
- R – atom wodoru, grupa alifatyczna lub aromatyczna;
- m – wartościowość metalu;
- M e – metal lub grupa amonowa N H indeks dolny, cztery, koniec indeksu dolnego.
Wzór ogólny soli:
Przykładem soli, która rozpuszcza się w wodzie i dysocjuje na jony, jest octan sodu (sól kwasu octowego):
- Fenolany
- A r – grupa aromatyczna;
- m – wartościowość metalu;
- M e – metal lub grupa amonowa N H indeks dolny, cztery, koniec indeksu dolnego.
Wzór ogólny soli:
W odróżnieniu od alkoholanów, które w kontakcie z wodą ulegają reakcji rozkładu z otrzymaniem wodorotlenku, fenolany mogą ulegać dysocjacji elektrolitycznej, a proces ten można zapisać w postaci:
Przykładem soli, która rozpuszcza się w wodzie i dysocjuje na jony, jest fenolan sodu (sól sodowa fenolu):
Jak sprawnie potrafisz zapisywać równania dysocjacji elektrolitycznej? Zagraj w domino. Na planszy rozsypanych jest kilkanaście kostek domino – Twoje zadanie polega na dokładaniu kolejno po jednym tak, aby jeden koniec kostki wskazywał na wzór związku przed dysocjacją, a drugi koniec pokazywał jony powstałe w procesie dysocjacji.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5CKEQNT1
Sprawdź swoją wiedzę, rozwiązując quiz.
Zaznacz poprawne odpowiedzi.
B a nawias, O H, zamknięcie nawiasu, indeks górny, plus, koniec indeksu górnego 1. H indeks dolny, dwa, koniec indeksu dolnego, O powyżej, strzałka w prawo, 2. dwa O H indeks górny, minus, koniec indeksu górnego, 3. H indeks dolny, dwa, koniec indeksu dolnego, O powyżej strzałki równowagowe, 4. ← poniżej, strzałka w prawo, 5. strzałka w prawo, 6. B a indeks górny, dwa, plus, koniec indeksu górnego, 7. O H indeks górny, minus, koniec indeksu górnego 1. H indeks dolny, dwa, koniec indeksu dolnego, O powyżej, strzałka w prawo, 2. dwa O H indeks górny, minus, koniec indeksu górnego, 3. H indeks dolny, dwa, koniec indeksu dolnego, O powyżej strzałki równowagowe, 4. ← poniżej, strzałka w prawo, 5. strzałka w prawo, 6. B a indeks górny, dwa, plus, koniec indeksu górnego, 7. O H indeks górny, minus, koniec indeksu górnego plus O H indeks górny, minus, koniec indeksu górnego
Zapisz równanie dysocjacji elektrolitycznej kwasu siarkowodorowego.