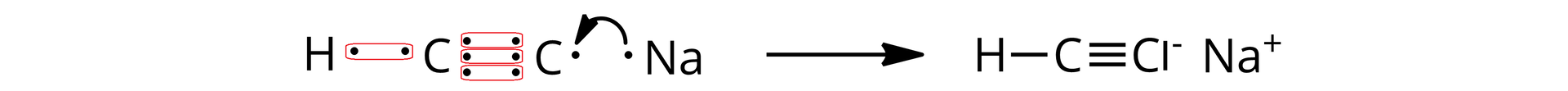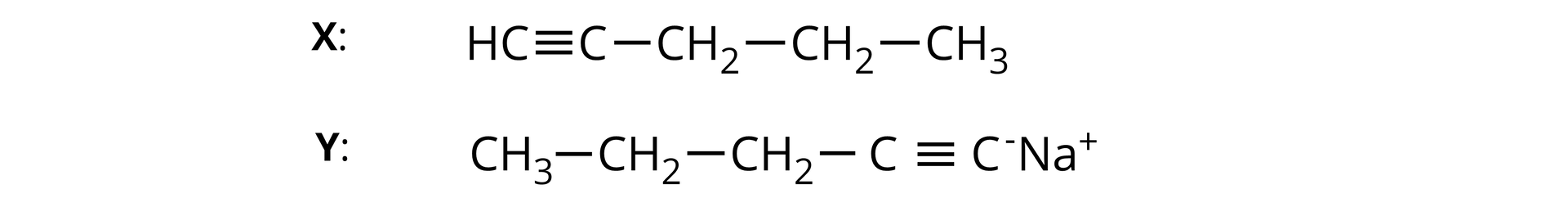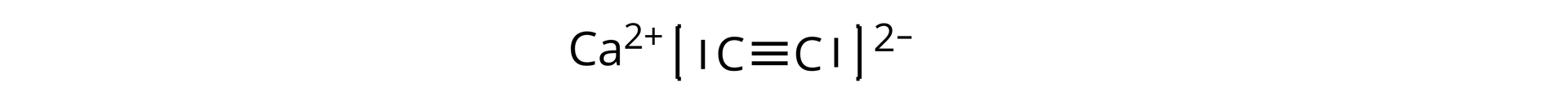Sprawdź się
Przedstaw wzór elektronowy acetylenku sodu i schemat powstawania wiązania jonowego.
Ustal, jakie organiczne związki chemiczne kryją się pod literami X i Y w poniższym schemacie reakcji. Narysuj wzory półstrukturalne tych związków.

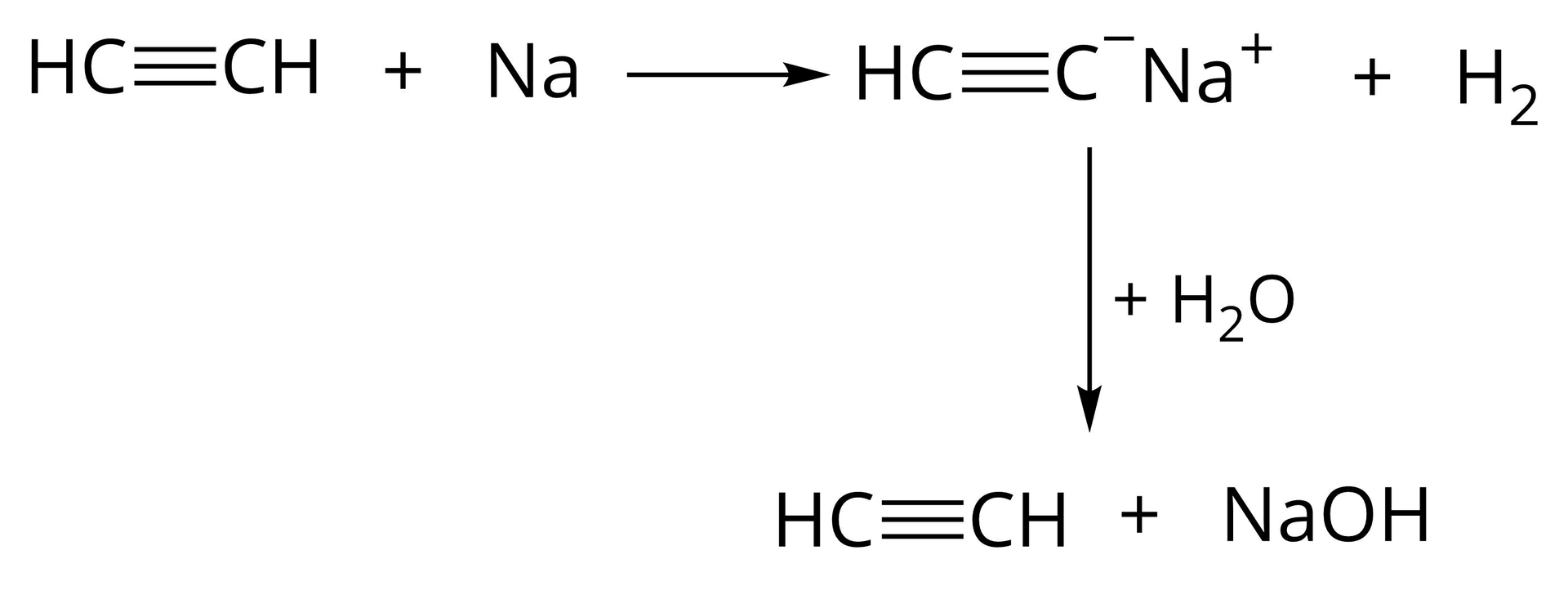
Z etynu, poddanego reakcji z sodem, uzyskuje się acetylenek monosodu. Ten z kolei, poddany reakcji z wodą, dowodzi o pewnych właściwościach alkinów terminalnych. Wyjaśnij, o jakie właściwości chodzi, uzasadniając swoją odpowiedź.
Węglik wapnia to nieorganiczny związek chemiczny wapnia z grupy węglików jonowych. W wyniku jego reakcji z wodą otrzymuje się acetylen.

Strukturalnie węglik wapnia i acetylenek sodu są do siebie podobne. Zapisz wzór elektronowy kreskowy węgliku wapnia i zaproponuj jego inną nazwę w oparciu o podobieństwo do acetylenku sodu.
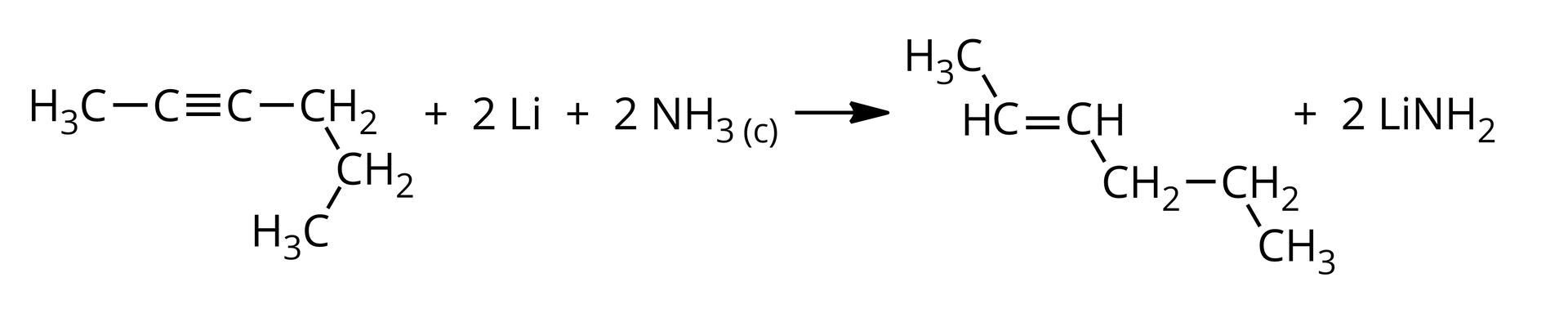
Stosując wzory półstrukturalne zapisz uproszczone równanie reakcji redukcji heks--ynu z litem w ciekłym amoniaku. We wzorze produktu organicznego uwzględnij jego konfigurację w oparciu o rodzaj otrzymanego izomeru typu /.
Podaj dwa stwierdzenia udowadniające, że reakcja heks--ynu z litem w ciekłym amoniaku to reakcja redukcji alkinu do alkenu.