Symulacja interaktywna
Poniższa symulacja przedstawia mechanizm przebiegu reakcji alkinów z metalami alkalicznymi w obecności amoniaku. Dokonaj analizy zawartych w niej przykładów. Następnie przedstaw mechanizm reakcji otrzymywania ()-heks--enu metodą redukcji alkinu w środowisku ciekłego amoniaku.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D10RDT7Ej
Poniższa symulacja przedstawia mechanizm przebiegu reakcji alkinów z metalami alkalicznymi. Zapoznaj się z opisem symulacji, a następnie wykonaj ćwiczenia sprawdzające.
W symulacji wyświetlają się kolejno mechanizmy reakcji wybranych alkinów z sodem w środowisku amoniaku lub z litem, również z udziałem . Wśród substratów znalazły się etyn, pent--yn oraz -metyloheks--yn. Szczególną uwagę zwrócono na fakt tworzenia wiązania jonowego pomiędzy sodem a cząsteczką alkinu oraz w odróżnieniu od niego wiązania kowalencyjnego w mechanizmie dla litu. Różnica wynika z właściwości elektronowych obu pierwiastków. Poniżej opisano przykładowe mechanizmy omawianej reakcji, odpowiednio – z udziałem sodu oraz litu.
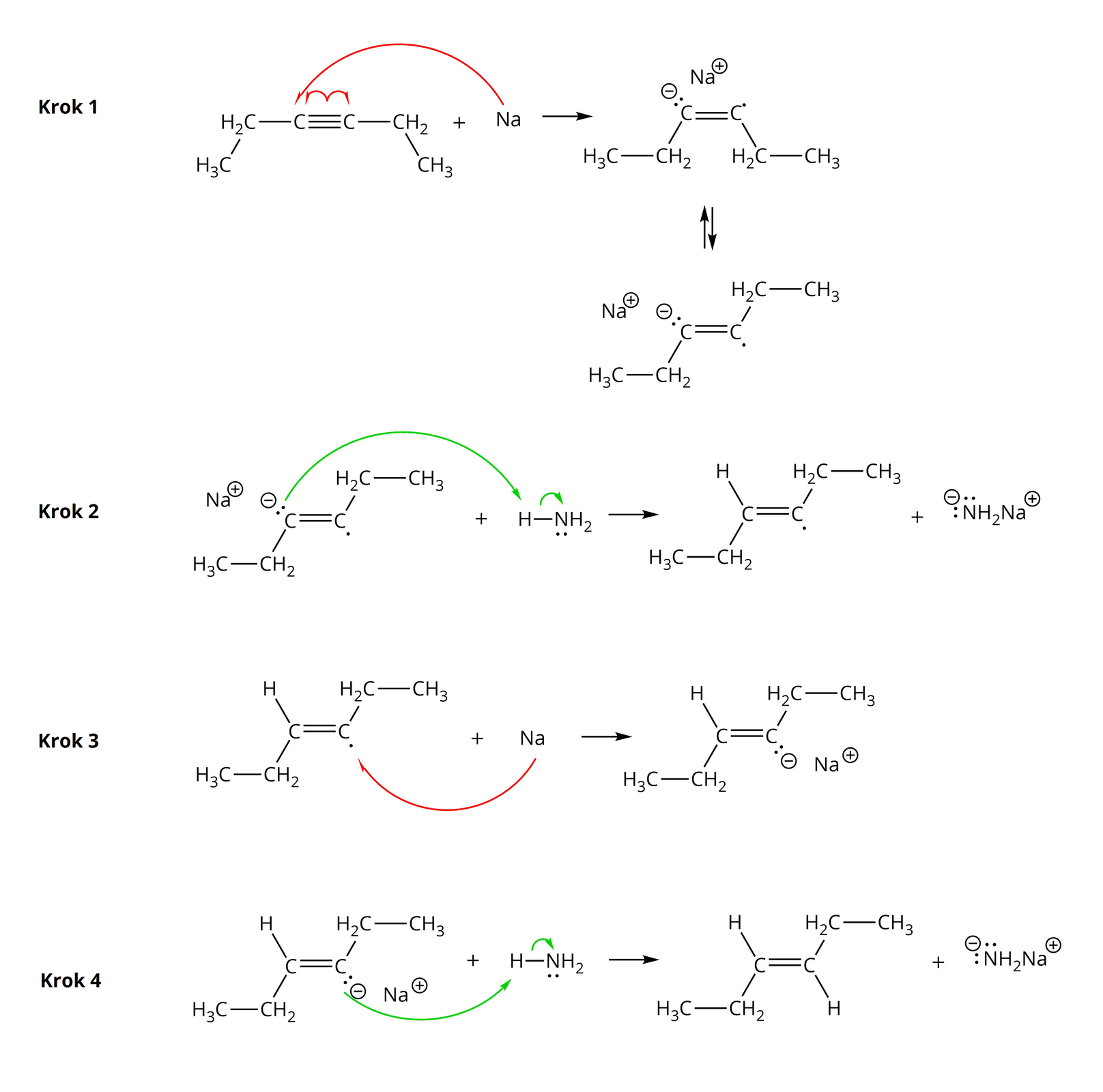
Mechanizm reakcji pent--ynu z sodem w środowisku ciekłego amoniaku
Pierwszy etap mechanizmu
Pierwszy etap mechanizmu reakcji pent--ynu z sodem w środowisku ciekłego amoniaku zakłada powstanie anionorodnika w wyniku ataku sodu na cząsteczkę alkinu i zerwania wiązania potrójnego. Cząsteczka alkinu zbudowanego z dwóch atomów węgla połączonych za pomocą wiązania potrójnego. Pierwszy z atomów węgla podstawiony jest grupą metylową , natomiast drugi grupą etylową . Dodać atom sodu , od którego poprowadzono łukowatą strzałkę z połową grotu do jednego z atomów węgla przy wiązaniu potrójnym w alkinie. Natomiast od jednego z trzech wiązań pomiędzy atomami węgla w alkinie poprowadzono dwie łukowate strzałki z połową grotu – po jednej do każdego z dwóch atomów węgla przy wspomnianym wiązaniu. Za sodem strzałka w prawo. Za strzałką anionorodnik zbudowany z dwóch atomów węgla połączonych wiązaniem podwójnym. Pierwszy z nich połączony jest z podstawnikiem metylowym, a drugi z etylowym. Przy pierwszym atomie węgla zaznaczono dwie kropki oznaczające wolną parę elektronową oraz znak minus. Przy drugim znajduje się pojedyncza kropka oznaczająca niesparowany elektron. Oba podstawniki znajdują się po jednej stronie płaszczyzny wyznaczonej przez wiązanie podwójne, to znaczy są w położeniu . Ładunek anionorodnika kompensowany jest przez kation sodu . Strzałki równowagowe. Przedstawiono analogiczną strukturę, w której atomy połączone są w cząsteczce tak samo, jednak zmianie uległa geometria wokół wiązania podwójnego. To znaczy podstawniki znajdują się teraz po przeciwnej stronie płaszczyzny wyznaczonej przez wiązanie podwójne. Podstawnik metylowy pod płaszczyzną, a etylowy nad.
Drugi etap mechanizmu
Drugi etap mechanizmu reakcji pent--ynu z sodem w środowisku ciekłego amoniaku zakłada uprotonowanie anionorodnika. Anionorodnik o geometrii E reaguje z cząsteczką amoniaku , w której wiązanie pojedyncze łączy atom wodoru z atomem azotu N z zaznaczonymi dwiema kropki, reprezentującymi wolną parę elektronową. Od wolnej pary elektronowej zlokalizowanej na jednym z atomów węgla w anionorodniku poprowadzono łukowatą strzałkę z pełnym grotem do atomu wodoru w cząsteczce amoniaku. Od wiązania łączącego atom wodoru z atomem azotu poprowadzono drugą łukowatą strzałkę z pełnym grotem do tegoż atomu azotu. Strzałka w prawo. Za strzałką rodnik zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki metylowy i etylowy znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Przy pierwszym atomie węgla znajduje się ponadto atom wodoru, a przy drugim kropka – oznaczająca niesparowany elektron. Dodać cząsteczkę amidku sodu z dwoma wolnymi parami elektronowymi zaznaczonymi na atomie azotu.
Trzeci etap mechanizmu
Trzeci etap mechanizmu reakcji pent--ynu z sodem w środowisku ciekłego amoniaku zakłada powstanie karboanionu. Rodnik o geometrii E reaguje z sodem , co reprezentuje łukowata strzałka z połową grotu poprowadzona od atomu sodu do elektronu w rodniku. Rodnik zbudowany jest z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki metylowy i etylowy znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Przy pierwszym atomie węgla znajduje się ponadto atom wodoru, a przy drugim kropka – oznaczająca niesparowany elektron. Strzałka w prawo, za strzałką karboanion zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Przy pierwszym atomie węgla znajduje się ponadto atom wodoru, a przy drugim dwie kropki – oznaczające wolną parę elektronową – oraz znak minus – wskazujący na ładunek, którym obdarzony jest atom węgla. Karboanion stabilizowany jest przez kation sodu .
Czwarty etap mechanizmu
Czwarty etap mechanizmu reakcji pent--ynu z sodem w środowisku ciekłego amoniaku prowadzi do powstania pożądanego produktu, to znaczy alkenu o geometrii E. Karboanion zbudowany jest z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Przy pierwszym atomie węgla znajduje się ponadto atom wodoru, a przy drugim dwie kropki – oznaczające wolną parę elektronową – oraz znak minus – wskazujący na ładunek, którym obdarzony jest atom węgla. Karboanion stabilizowany jest przez kation sodu . Karboanion reaguje z amoniakiem , co reprezentuje łukowata strzałka z pełnym grotem poprowadzona od pary elektronowej zlokalizowanej na atomie węgla do atomu wodoru połączonego z atomem azotu w cząsteczce amoniaku. Wiązanie łączące atom wodoru z atomem azotu zostaje zerwane, co przedstawia łukowata strzałka z pełnym grotem poprowadzona od tegoż wiązania do atomu azotu. Strzałka w prawo, za strzałką E alken zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki metylowy i etylowy znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Podobnie jak atomy wodoru również połączone z atomami węgla przy wiązaniu podwójnym. Dodać cząsteczkę amidku sodu . Na atomie azotu N, w cząsteczce amidku sodu zaznaczono ponadto dwie wolne pary elektronowe w postaci dwóch par kropek.
Mechanizm reakcji etynu z litem w środowisku ciekłego amoniaku
Pierwszy etap mechanizmu
Pierwszy etap mechanizmu reakcji etynu z litem w środowisku ciekłego amoniaku zakłada powstanie związku metaloorganicznego. Cząsteczka alkinu zbudowanego z dwóch atomów węgla połączonych za pomocą wiązania potrójnego. Każdy z atomów węgla podstawiony jest jednym atomem wodoru. Dodać atom litu , od którego poprowadzono łukowatą strzałkę z połową grotu do jednego z atomów węgla przy wiązaniu potrójnym w alkinie. Natomiast od jednego z trzech wiązań pomiędzy atomami węgla w alkinie poprowadzono dwie łukowate strzałki z połową grotu – po jednej do każdego z dwóch atomów węgla przy wspomnianym wiązaniu. Za litem strzałka w prawo. Za strzałką związek metaloorganiczny. Jest on rodnikiem zbudowanym z dwóch atomów węgla połączonych wiązaniem podwójnym. Każdy z wspomnianych atomów węgla podstawiony jest atomem wodoru. Ponadto pierwszy atom węgla połączony jest wiązaniem kowalencyjnym z atomem litu. Przy drugim węglu znajduje się pojedyncza kropka oznaczająca niesparowany elektron. Oba podstawniki, czyli atomy wodoru, znajdują się po jednej stronie płaszczyzny wyznaczonej przez wiązanie podwójne, to znaczy są w położeniu . Strzałki równowagowe. Przedstawiono analogiczną strukturę, w której atomy połączone są tak samo, jednak zmianie uległa geometria wokół wiązania podwójnego. To znaczy podstawniki znajdują się teraz po przeciwnej stronie płaszczyzny wyznaczonej przez wiązanie podwójne.
Drugi etap mechanizmu
Drugi etap mechanizmu reakcji etynu z litem w środowisku ciekłego amoniaku zakłada uprotonowanie rodnika. Rodnik o geometrii E reaguje z cząsteczką amoniaku , w której wiązanie pojedyncze łączy atom wodoru z atomem azotu N z zaznaczonymi dwiema kropki, reprezentującymi wolną parę elektronową. Od wiązania łączącego atom węgla z atomem litu w rodniku poprowadzono łukowatą strzałkę z pełnym grotem do atomu wodoru w cząsteczce amoniaku. A od wiązania łączącego atom wodoru z atomem azotu poprowadzono drugą łukowatą strzałkę z pełnym grotem do tegoż atomu azotu. Strzałka w prawo. Za strzałką rodnik zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Przy pierwszym atomie węgla znajdują się dwa atomy wodoru, a przy drugim jeden atom wodoru oraz kropka – oznaczająca niesparowany elektron. Dodać cząsteczkę amidku sodu z dwoma wolnymi parami elektronowymi zaznaczonymi na atomie azotu.
Trzeci etap mechanizmu
Trzeci etap mechanizmu reakcji etynu z litem w środowisku ciekłego amoniaku zakłada powstanie związku litoorganicznego. Rodnik o geometrii reaguje z litem , co reprezentuje łukowata strzałka z połową grotu poprowadzona od atomu litu do elektronu w rodniku. Rodnik zbudowany jest z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Podstawniki metylowy i etylowy znajdują się po przeciwnych stronach płaszczyzny wiązania podwójnego. Przy pierwszym atomie węgla znajdują się dwa atomy wodoru, a przy drugim jeden atom wodoru oraz kropka – oznaczająca niesparowany elektron. Strzałka w prawo, za strzałką związek litoorganiczny zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Przy pierwszym atomie węgla znajdują się dwa atomy wodoru, a przy drugim jeden atom wodoru oraz atom litu – połączony z węglem wiązaniem kowalencyjnym.
Czwarty etap mechanizmu
Czwarty etap mechanizmu reakcji etynu z litem w środowisku ciekłego amoniaku prowadzi do powstania pożądanego produktu, to znaczy alkenu (w przypadku niesymetrycznego związku o geometrii E). Związek litoorganiczny zbudowany jest z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Przy pierwszym atomie węgla znajdują się dwa atomy wodoru, a przy drugim jeden atom wodoru oraz atom litu – połączony z węglem wiązaniem kowalencyjnym. Związek ten reaguje z amoniakiem , co reprezentuje łukowata strzałka z pełnym grotem poprowadzona od pary elektronowej łączącej atom węgla z atomem litu do atomu wodoru w cząsteczce amoniaku. Wiązanie łączące atom wodoru z atomem azotu w amoniaku zostaje zerwane, co przedstawia łukowata strzałka z pełnym grotem poprowadzona od tegoż wiązania do atomu azotu. Strzałka w prawo, za strzałką eten zbudowany z dwóch atomów węgla połączonych za pomocą wiązania podwójnego. Każdy z nich podstawiony jest dwoma atomami wodoru. Dodać cząsteczkę amidku sodu . Na atomie azotu N, w cząsteczce amidku sodu zaznaczono ponadto dwie wolne pary elektronowe w postaci dwóch par kropek.
Powstające nowe wiązanie chemiczne pomiędzy atomem węgla a atomem sodu jest wiązaniem: Możliwe odpowiedzi: 1. jonowym., 2. kowalencyjnym spolaryzowanym., 3. kowalencyjnym niespolaryzowanym., 4. koordynacyjnym., 5. wodorowym.
Powstający produkt organiczny powyższej reakcji, należy do grupy: Możliwe odpowiedzi: 1. związków typu soli., 2. kwasów., 3. zasad., 4. wodorków., 5. podtlenków., 6. związków koordynacyjnych.