Sprawdź się
Zaznacz prawidłową definicję. Konfiguracja elektronowa to...
- jest to opis atomu, polegający na rozkładzie elektronów na podstawie prawdopodobieństwa ich położenia w atomie w funkcji odległości od jądra.
- zbiór elektronów o tej samej wartości głównej liczby kwantowej (n).
- zbiór elektronów, zawierający takie same wartości dla głównej liczby kwantowej (n), pobocznej liczby kwantowej (l) oraz magnetycznej liczby kwantowej (m).
- nieregularność w strukturze elektronowej, zapewniająca lepsze korzyści energetyczne.
Poniżej przedstawiony został zapis klatkowy konfiguracji elektronowej atomu pewnego pierwiastka.
Zapoznaj się z opisem zapisu klatkowego konfiguracji elektronowej atomu pewnego pierwiastka.
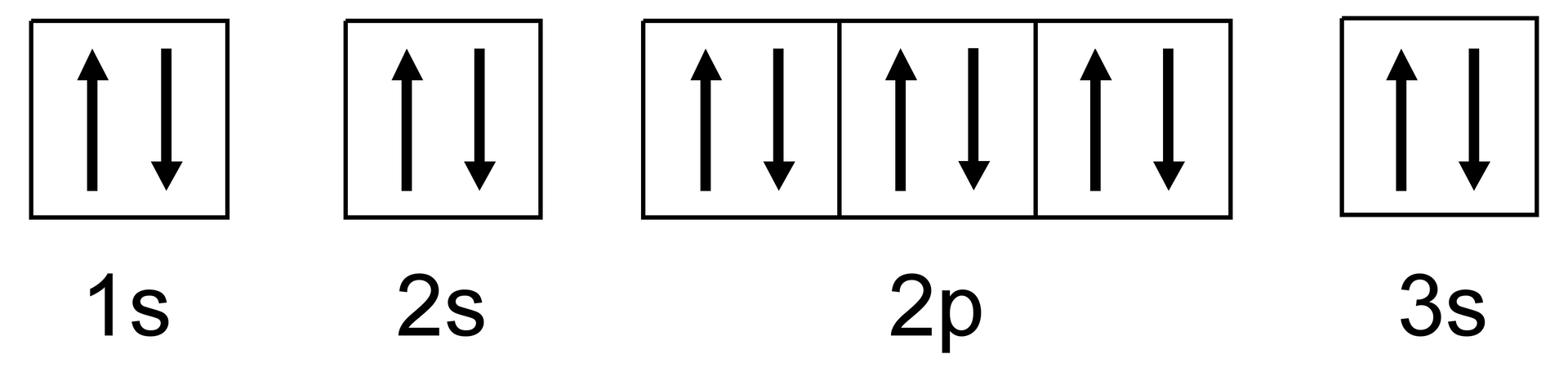
Wybierz prawidłowy zapis skrócony.
Przedstaw konfigurację elektronową, zawierającą oznaczenia literowe powłok, w postaci konfiguracji zawierającej oznaczenia orbitali. Napisz, jakiego pierwiastka dotyczy.
B. : Liczbę atomową Z: Tu uzupełnij. Liczbę protonów w jądrze: Tu uzupełnij. Liczbę elektronów walencyjnych: Tu uzupełnij.
C. : Liczbę atomową Z: Tu uzupełnij. Liczbę protonów w jądrze: Tu uzupełnij. Liczbę elektronów walencyjnych: Tu uzupełnij.
Na podstawie konfiguracji elektronowej podaj wymienione informacje.
A.
Liczbę atomową Z: .............
Liczbę protonów w jądrze: .............
Liczbę elektronów walencyjnych: .............
B.
Liczbę atomową Z: .............
Liczbę protonów w jądrze: .............
Liczbę elektronów walencyjnych: .............
C.
Liczbę atomową Z: .............
Liczbę protonów w jądrze: .............
Liczbę elektronów walencyjnych: .............
Na podstawie przedstawionych poniżej konfiguracji elektronowych:
:
:
:
:
:
:
Podaj konfigurację elektronową atomu manganu, a następnie rozwiąż poniższe podpunkty.
A. Napisz konfigurację elektronową jonów oraz jonu .
B. Określ liczbę powłok elektronowych w tych jonach.
C. Określ liczbę niesparowanych elektronów w tych jonach.
D. Który jon jest trwalszy?
Elektrony walencyjne pewnego pierwiastka chemicznego opisują liczby kwantowe znajdujące się w tabeli.
Numer elektronu | Wartości liczb kwantowych | |||
|---|---|---|---|---|
Podaj nazwę i symbol pierwiastka chemicznego oraz pełny zapis konfiguracji elektronowej.