Sprawdź się
Który z opisów dotyczy wodorków typu soli? Wskaż prawidłową odpowiedź.
- Posiadają budowę jonową i w stanie stopionym przewodzą prąd elektryczny.
- Posiadają budowę jonową i po rozpuszczeniu przewodzą prąd elektryczny.
- Posiadają budowę molekularną i w stanie stopionym przewodzą prąd elektryczny.
- Posiadają budowę molekularną, dzięki czemu przewodzą prąd elektryczny.
Wskaż prawidłową odpowiedź, opisującą wodorki jonowe.
- Posiadają wysoką temperaturę topnienia.
- Charakteryzują się dużą kruchością.
- Mają niską temperaturę topnienia.
- Charakteryzują się małą kruchością.
Wskaż zestaw, który przedstawia wyłącznie wodorki typu soli.
- , , ,
- , , ,
- , , ,
- , , ,
Spośród podanych poniżej wodorków, wybierz wodorki typu soli i podaj ich nazwy.
{#}{#}{#}{}{}{#}{}
Zapoznaj się z opisem rysunku, przedstawiającego model . Uzupełnij poniższe zdania (wybierając odpowiednie wyrazy) i opisz rysunek.
Poniższy rysunek przedstawia model . Uzupełnij poniższe zdania (wybierając odpowiednie wyrazy) i opisz rysunek.
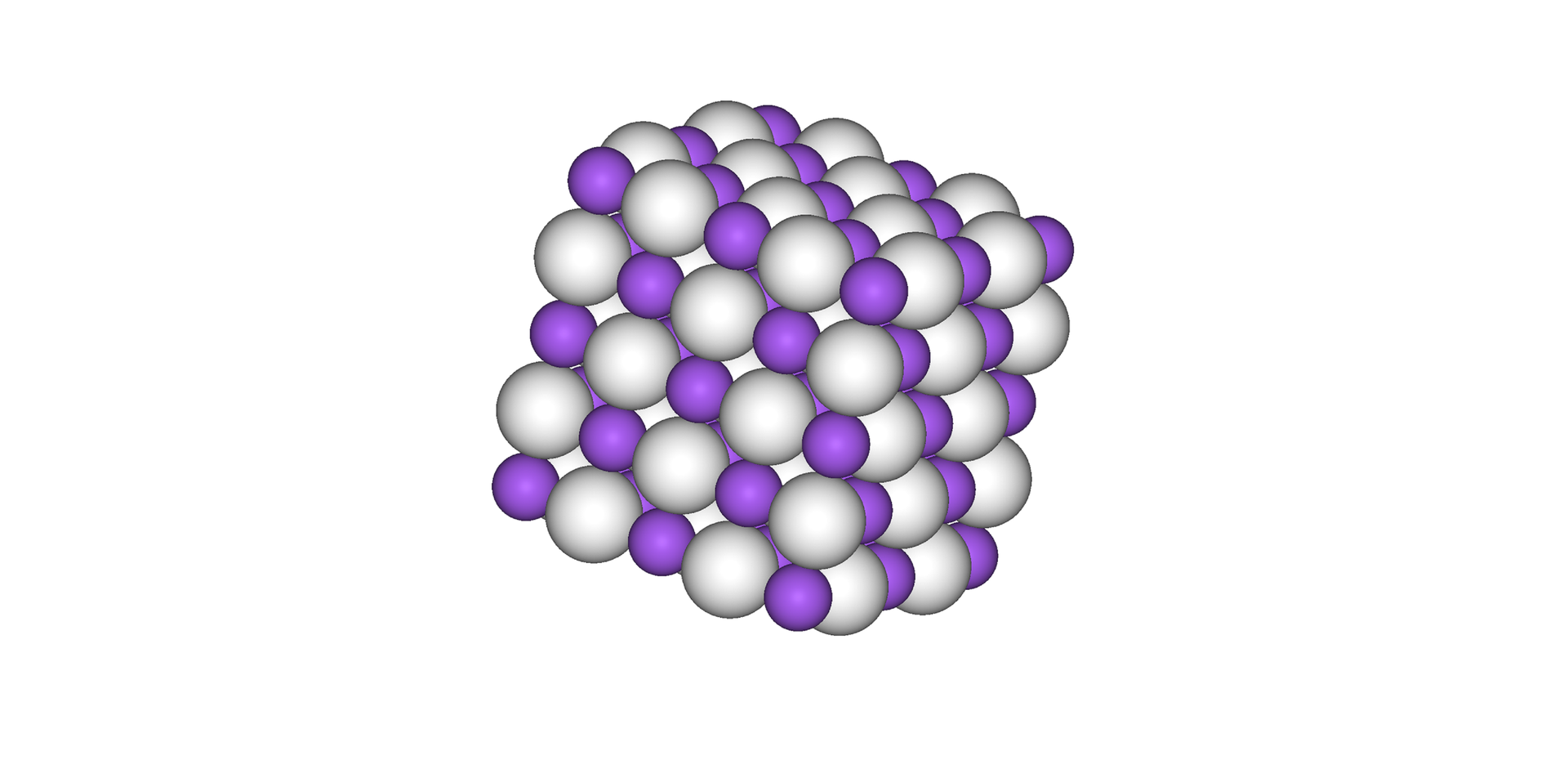
metaliczny, jonowe, molekularne, niskotopliwa, siły dipol-dipol, jonów, cząsteczek, wysokotopliwa, oddziaływania kulombowskie, kationów, typu soli, w stanie stałym, siły van der Waalsa, stanie stopionym, kowalencyjny
NaH to wodorek ......................................................, którego kryształy ...................................................... zbudowane są z naprzemiennie ułożonych ....................................................... Pomiędzy nimi występują ....................................................... Wodorek sodu to substancja ...................................................... i krucha, która przewodzi prąd w .......................................................
- luka do uzupełnienia luka do uzupełnienia luka do uzupełnienia
- luka do uzupełnienia luka do uzupełnienia
- luka do uzupełnienia luka do uzupełnienia luka do uzupełnienia luka do uzupełnienia
- luka do uzupełnienia luka do uzupełnienia
Uzupełnij brakujące pola równań reakcji chemicznych.
, , , , , , , , , , , , , , , , , , , , , , ,
Pewien wodorek typu soli składa się z 95,24% wagowych pierwiastka . Ustal wzór sumaryczny tego wodorku.
Oblicz, ile gazu wydzieli się w wyniku reakcji wodorku rubidu z wodą (w przeliczeniu na warunki normalne). Wynik podaj z dokładnością do drugiego miejsca po przecinku. W obliczeniach przyjmij, że masa atomowa rubidu wynosi , a masa atomowa wodoru .