Sprawdź się
Połącz w pary poniższe pojęcia z ich wyjaśnieniem
każdy stan drobiny o energii wyższej niż energia jej stanu podstawowego, stan o najniższej energii (w danych warunkach), pochłanianie energii promieniowania elektrochemicznego oddziałującego z drobiną, prowadzące do jej przejścia w stan wzbudzony, metoda analizy jakościowej, wykorzystująca zjawisko emisja promieniowania elektromagnetycznego o określonej długości fali przez kationy metali
| analiza płomieniowa | |
| stan podstawowy drobiny | |
| stan wzbudzony drobiny | |
| absorbcja |
Zaznacz zdanie fałszywe.
- Sód to pierwszy litowiec, który rozpoczyna tę grupę.
- Litowce tworzą wyłącznie wiązania jonowe.
- Litowce nie występują w stanie wolnym.
Zaznacz zdanie prawdziwe.
- Litowce są najbardziej reaktywne spośród wszystkich metali.
- Litowce występują na stopniu utlenienia +II.
- Do litowców zaliczamy: wodór, lit, sód, potas, rubid, cez oraz frans.
Pewien trudnorozpuszczalny fluorek litowca barwi płomień na karminowo. Podaj nazwę systematyczną tego związku.
Odpowiedz na pytanie:
W jakim celu stosuje się stężony kwas chlorowodorowy (solny) w doświadczeniu badania zachowania litowców w płomieniu palnika?
Kationy litowców barwią płomień w charakterystyczny sposób. Przenieś do tabeli nazwy barw płomienia, jakie obserwuje się po włożeniu pręcika nasączonego wybranymi roztworami soli litowców.
, , , ,
| Kation litowca | Barwa płomienia |
|---|---|
W wyniku reakcji potasu z tlenem powstał nadtlenek potasu. Oblicz, ile atomów potasu wzięło udział w reakcji, jeśli powstały dwa mole nadtlenku potasu.
Uczeń, chcąc zbadać barwę płomienia litu, przygotował roztwór zawierający kationy litu. W tym celu wprowadził chlorku litu oraz mola azotanu() litu i uzupełnił wodą destylowaną do objętości . Oblicz stężenie molowe kationów litu w otrzymanym roztworze.
Litowce ulegają licznym reakcjom, a ich jony barwią płomień palnika w charakterystyczny sposób. Przeanalizuj poniższy chemograf i zapisz równania reakcji chemicznych oznaczonych numerami -.
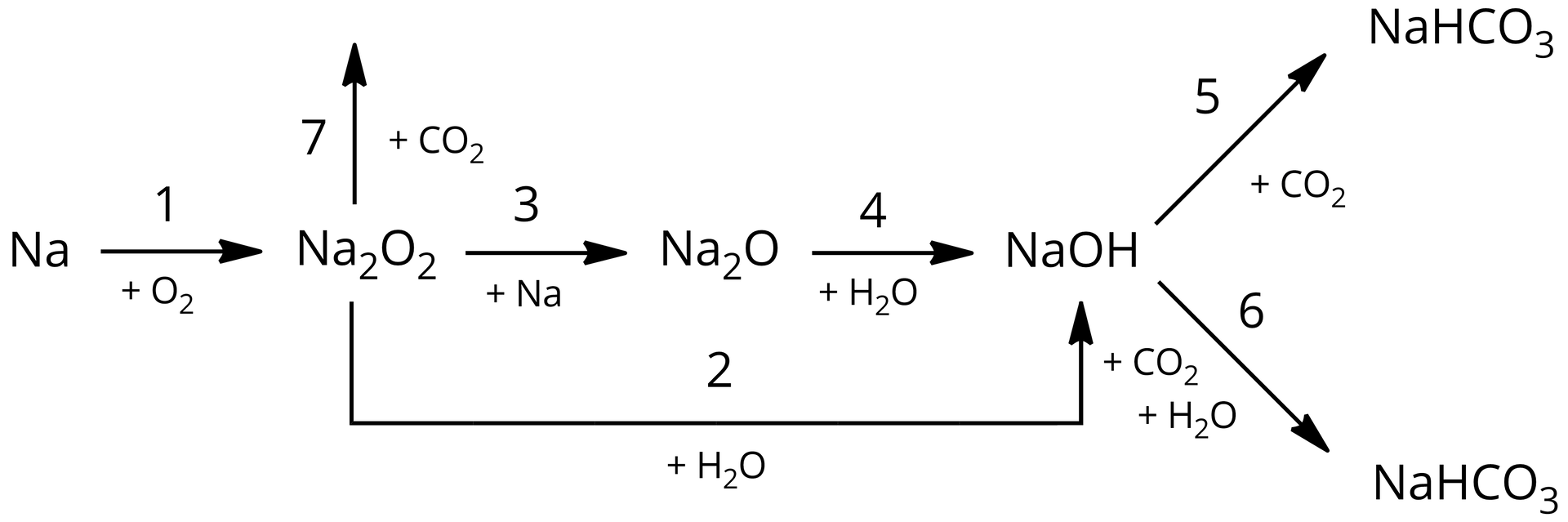
Wybierz prawidłowe dokończenie następującego równania reakcji chemicznej: .
Opisz, dlaczego pokaz fajerwerków jest szkodliwy dla środowiska.
Wyjaśnij, dlaczego podczas analizy płomieniowej roztworów wodnych soli nie wolno używać wody kranowej jako rozpuszczalnika?