Sprawdź się
Wskaż poprawne odpowiedzi.
Uzupełnij równanie dysocjacji elektrolitycznej. W puste pola wstaw odpowiednie wyrażenia, przeciągając je w puste miejsca.
W roztworze o objętości znajdują się następujące jony: kationów potasu, anionów azotanowych() i kationów wapnia.
Jakie sole rozpuszczono, aby otrzymać ten roztwór?
W czterech probówkach (-) rozpuszczono w wodzie substancje, które dysocjują na jony, podane poniżej probówek. Zapisz ich nazwy, wzory sumaryczne substancji, które wprowadzono do każdej z probówek oraz równania dysocjacji elektrolitycznej tych substancji.
W czterech probówkach (-) rozpuszczono w wodzie substancje, które dysocjują na jony. Zapoznaj się z opisem ilustracji. Zapisz ich nazwy, wzory sumaryczne substancji, które wprowadzono do każdej z probówek oraz równania dysocjacji elektrolitycznej tych substancji.

Napisz równania dysocjacji elektrolitycznej następujących soli:
1.
2.
3.
4.
5.
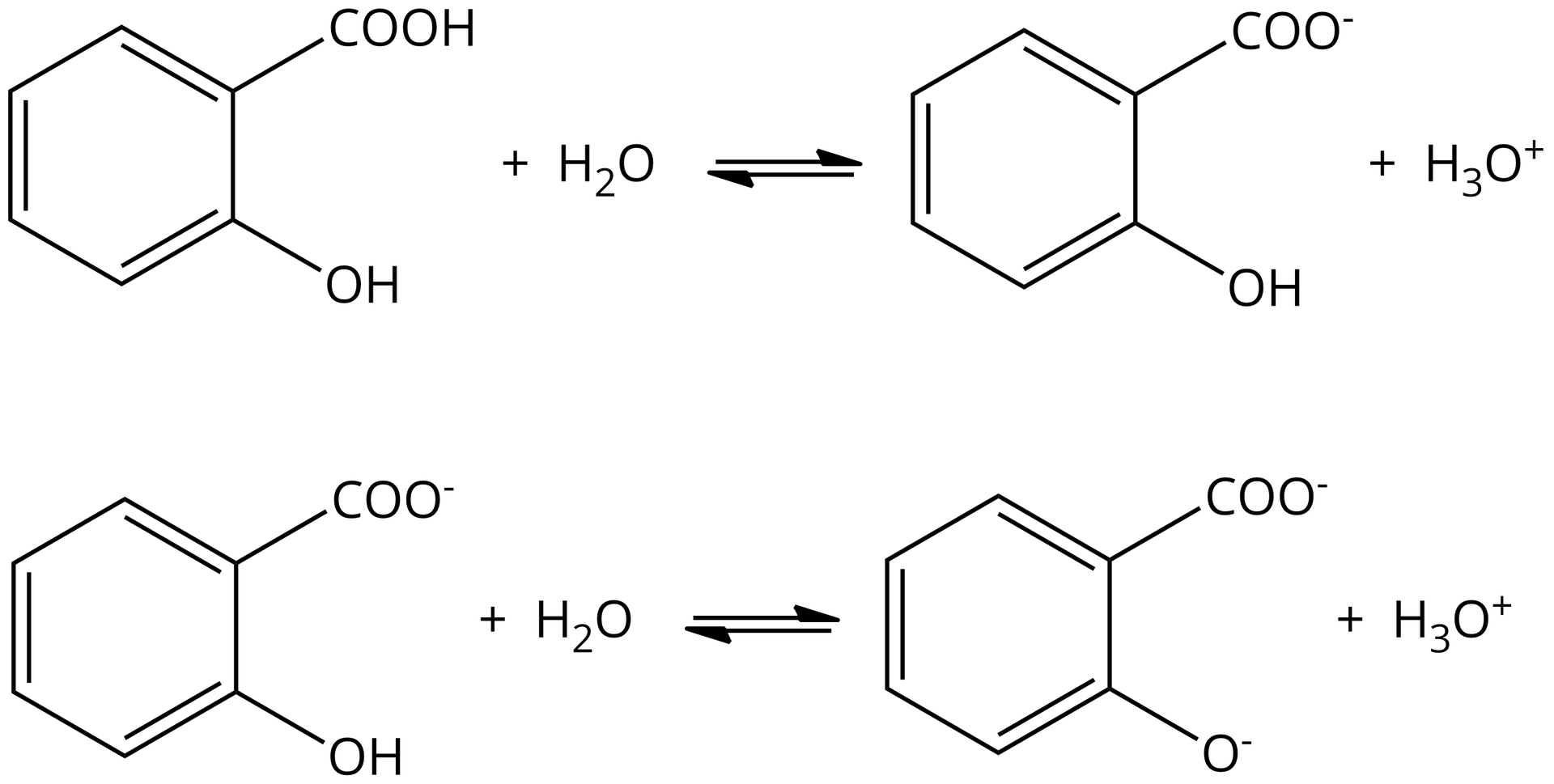
Analizując strukturę węglanu sodu, wyjaśnij, dlaczego dysocjuje zgodnie z równaniem reakcji:
Wodorowęglan amonu – zwany potocznie „amoniakiem” – to biały, krystaliczny proszek o wyraźnym zapachu, dobrze rozpuszczalny w wodzie. Był stosowany jako środek spulchniający do pieczenia.
Zapisz równanie dysocjacji elektrolitycznej tego związku, a następnie sprawdź poprawną odpowiedź.
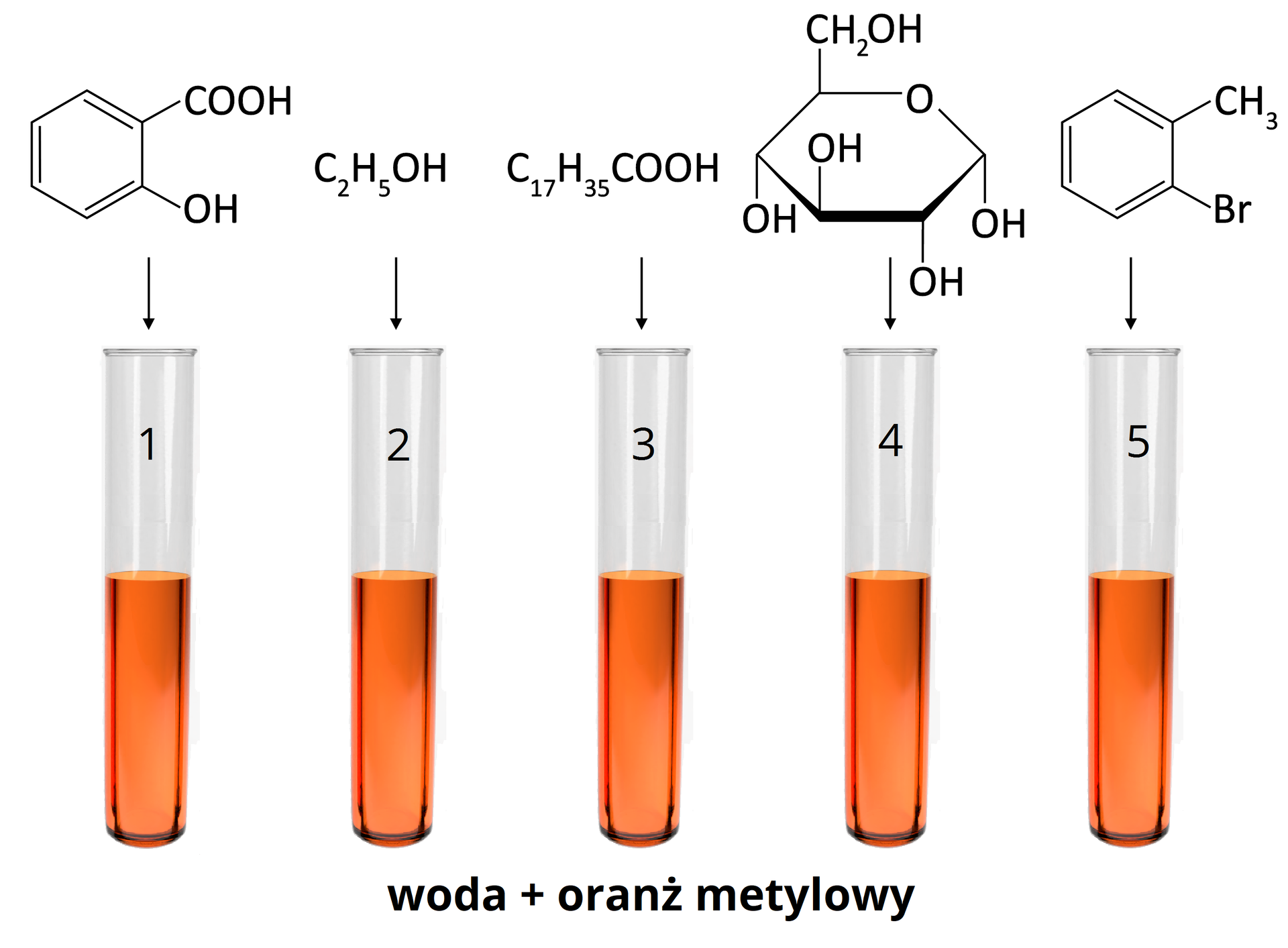
Do pięciu probówek dodano wodę oraz oranż metylowy, a następnie dodano substancje o podanych poniżej wzorach. Zastanów się, które z nich rozpuszczają i mieszają się z wodą, a następnie oceń, w których probówkach substancje ulegają dysocjacji elektrolitycznej. Zapisz odpowiednie równania dysocjacji elektrolitycznej i określ, w których probówkach wskaźnik przyjął barwę czerwoną.
Odpowiedź porównaj z odpowiedzią zamieszczoną we wskazówkach i kluczach odpowiedzi.