Sprawdź się
Jakie barwy przybiera chlorek kobaltu w zależności od stopnia uwodnienia?
W jakich uwodnionych formach występuje chlorek kobaltu? Podaj wzory sumaryczne.
Uzupełnij tabelę właściwymi nazwami lub wzorami sumarycznymi hydratów.
Napisz nazwę systematyczną hydratu o wzorze sumarycznym .
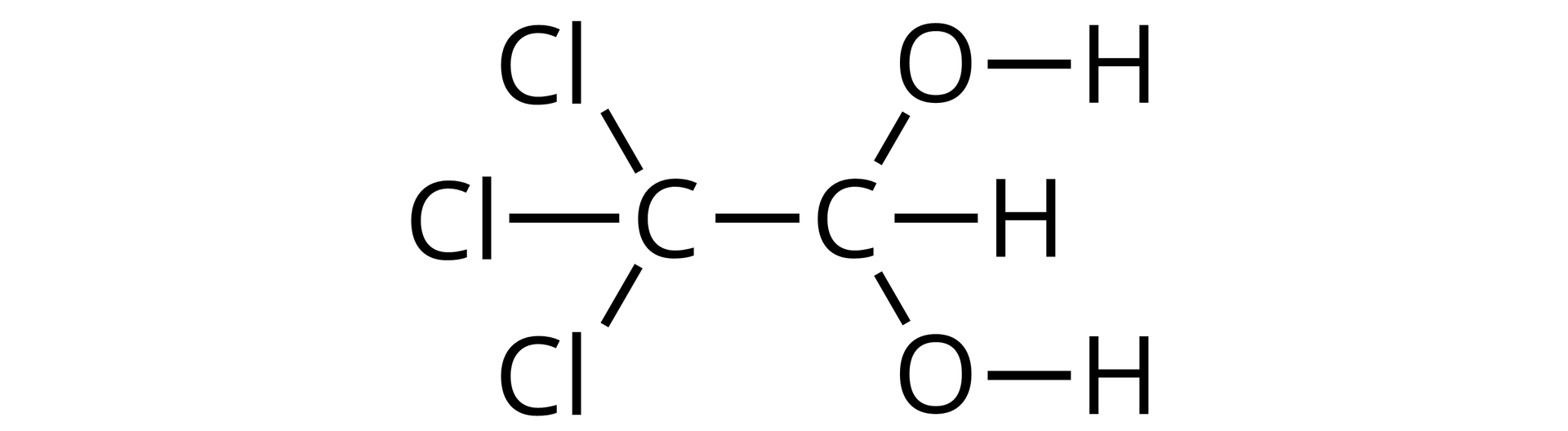
Narysuj wzór strukturalny wodzianu chloralu.
Sporządzono roztwór , rozpuszczając siarczanu miedzi — woda w wody. Oblicz stężenie procentowe tego roztworu.
Rozpuszczono siarczanu miedzi — woda w wody. Oblicz stężenie molowe tego roztworu, zakładając, że gęstość otrzymanego roztworu jest równa gęstości wody. Gęstość wody wynosi .
Koperwas zielony lub zielony witriol żelaza to dawne nazwy uwodnionej soli o wzorze . Oblicz , jeśli wiadomo, że stosunek masowy do wody w tym związku wynosi . Podaj wzór oraz nazwę systematyczną tego związku.