Sprawdź się
Wybierz poprawną odpowiedź.
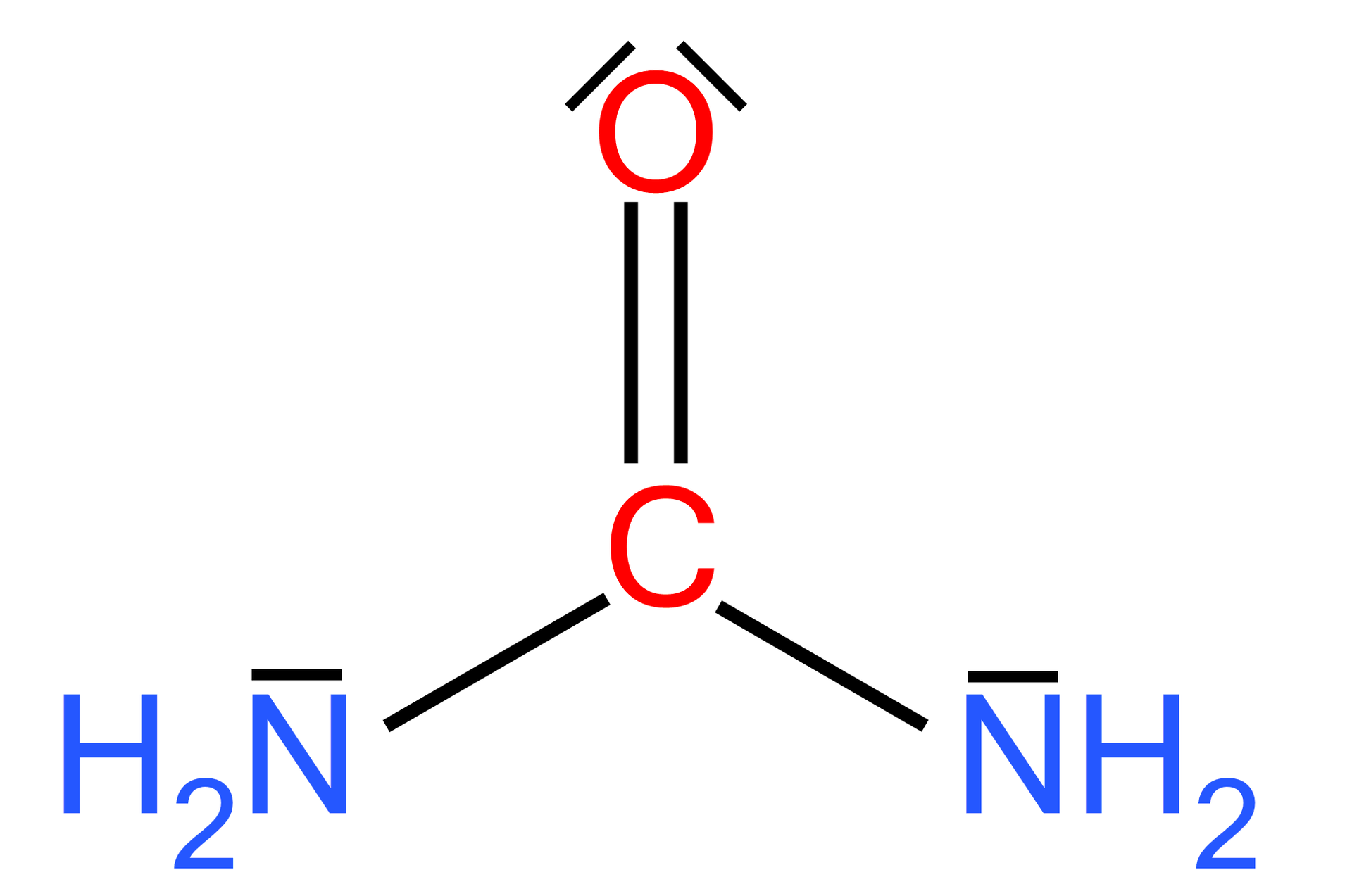
Mocznik to:
- diamid kwasu węglowego
- amid kwasu węglowego
- amina kwasu węglowego
- diamina kwasu węglowego
W dwóch nieoznaczonych probówkach znajdował się acetamid i mocznik. Do obu wprowadzono roztwór kwasu siarkowego(VI). W jednej z tych probówek zaczął wydzialć się bezbarwny, bezwonny gaz, w drugiej nie zaobserwowano intensywnego wydzielania, ale dało się poczuć charakterystyczny zapach octu. W oparciu o wskazane obserwacje uzupełnij poniższe wnioski.
aldehyd octowy, amoniak, kwas etanowy, azot, mocznik, tlenek węgla(IV), acetamid
W probówce, w której wydzielał się bezwonny, bezbarwny gaz znajdował się związek o nazwie ................................... Wydzielającym się gazem jest ................................... W probówce, w której dało się wyczuć zapach octu znajdował się ................................... Za charakterystyczny zapach uwalniany w trakcie reakcji odpowiedzialny jest ...................................
Połącz w pary poniższe pojęcia z ich wyjaśnieniem.
związek chemiczny zawierający dwa ugrupowania amidowe, związek wielkocząsteczkowe zbudowane z reszt aminokwasowych, połączonych wiązaniem peptydowym, związek nieorganiczny, diamid kwasu węglowego
| mocznik | |
| diamid | |
| białko |
Narysuj wzór mocznika i zaznacz wszystkie wolne pary elektronowe w otrzymanym wzorze. Wskaż typ hybrydyzacji atomu węgla.
Rozwiąż zadanie.
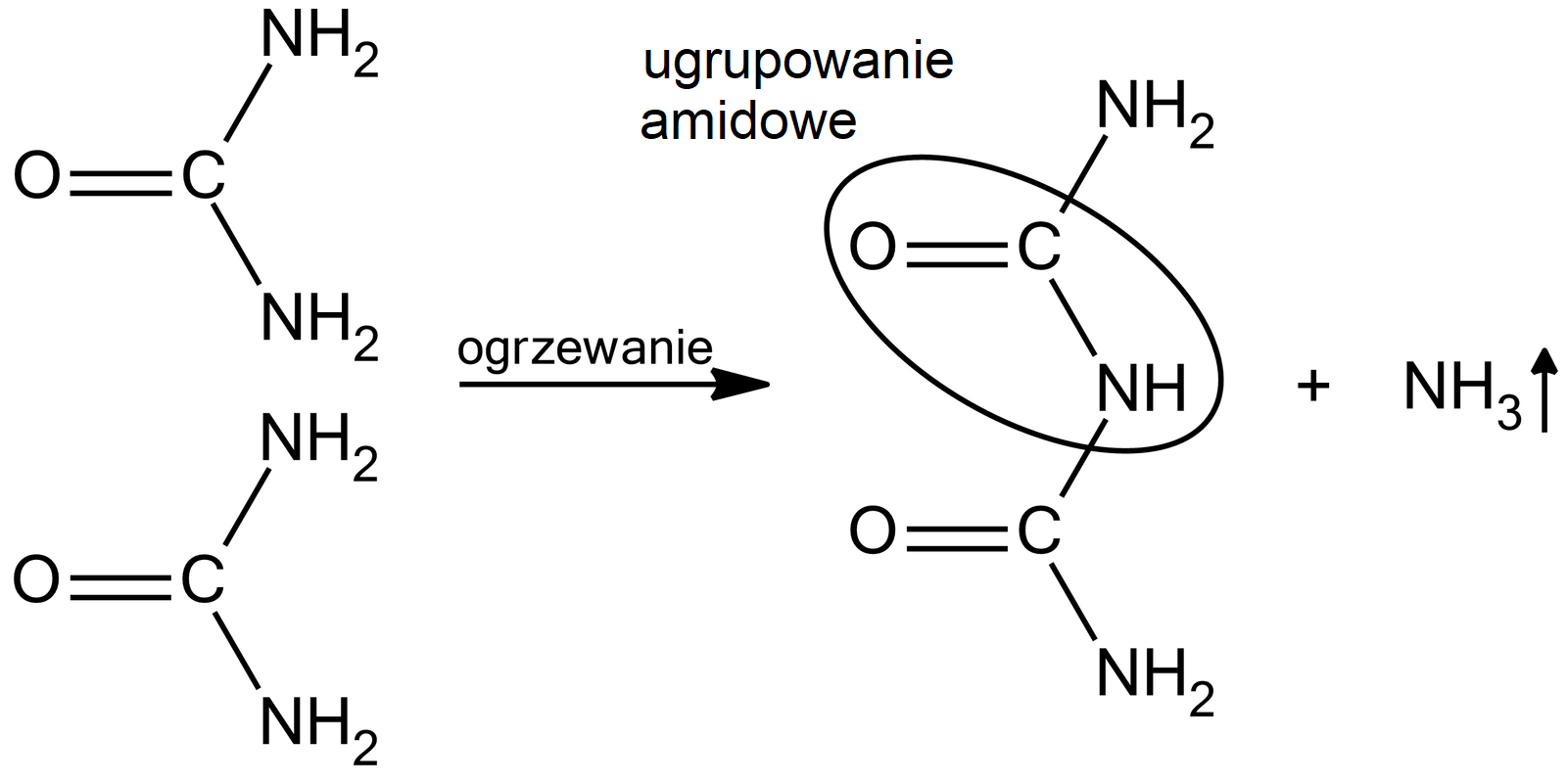
Biuret to związek powstający w wyniku kondensacji dwóch cząsteczek mocznika. Zapisz równanie tej reakcji oraz zaznacz i nazwij charakterystyczne wiązanie, występujące w cząsteczce biuretu.
Biuret to związek powstający w wyniku kondensacji dwóch cząsteczek mocznika . Zapisz równanie tej reakcji w formie cząsteczkowej oraz nazwij i opisz charakterystyczne wiązanie, występujące w cząsteczce biuretu.
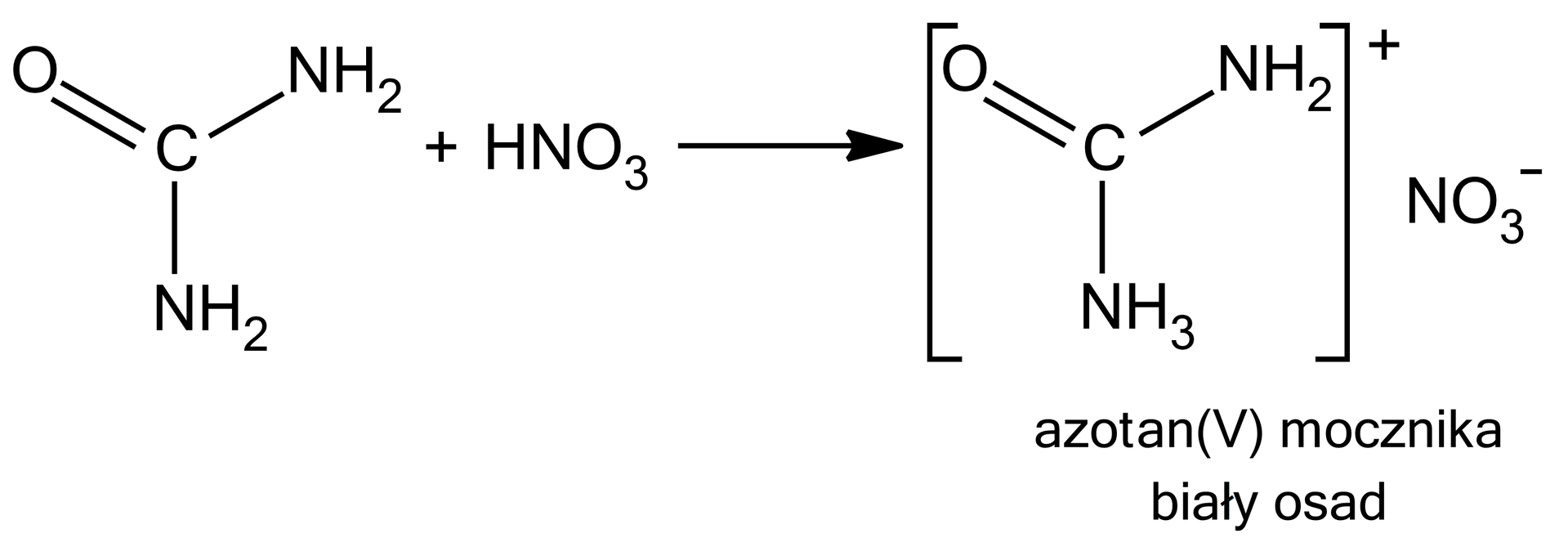
Analityczny sposób wykrywania mocznika w moczu, polega na przeprowadzeniu reakcji z kwasem azotowym(). Zapisz równanie tej reakcji i podaj nazwę otrzymanego produktu. Określ, jaki charakter chemiczny mocznika potwierdzono w tej reakcji?
Zapoznaj się z tekstem, a następnie rozwiąż zadanie.
W zależności od stężenia mocznika w moczu możemy wywnioskować, jakie problemy zdrowotne ma pacjent. Duże stężenie mocznika może sygnalizować o problemach z nerkami, odwodnieniu lub o zbyt dużej ilości białka w diecie. Za małe stężenie mocznika może być spowodowane niedożywieniem, problemami z wątrobą czy nadmiernym oddawaniu moczu. Do laboratorium dostarczono moczu, w którym oznaczono mocznika. Norma dla zdrowego człowieka wynosi – . Na podstawie wyniku określ, czy osoba, która przekazała próbkę do badań jest zdrowa czy nie? , ,
Zapoznaj się z poniższym tekstem, a następnie rozwiąż zadanie.
W celu ustalenia wzoru sumarycznego mocznika spalono w tlenie próbki tego związku i otrzymano i . Ustalono również, że mocznik zawiera około masowych azotu, a jego masa molowa wynosi . Ustal wzór sumaryczny mocznika.
Zapoznaj się z poniższym tekstem, a następnie rozwiąż zadanie.
Uczeń w laboratorium chciał otrzymać mocznik podczas syntezy amoniaku i tlenku węgla(). W tym celu przygotował roztwóru amoniaku o stężeniu o stężeniu . Następnie dodał odpowiedniego katalizatora i zanużył w roztworze rurkę, przez którą doprowadzał tlenek węgla(). Oblicz, ile gram mocznika otrzymał uczeń. Załóż, że wydajność reakcji wynosi . Wynik podaj z dokładnością do części setnych. , , .