Sprawdź się
Pokaż ćwiczenia:
Ćwiczenie 1
Liczbą przestrzenną (Lp) nazywamy:
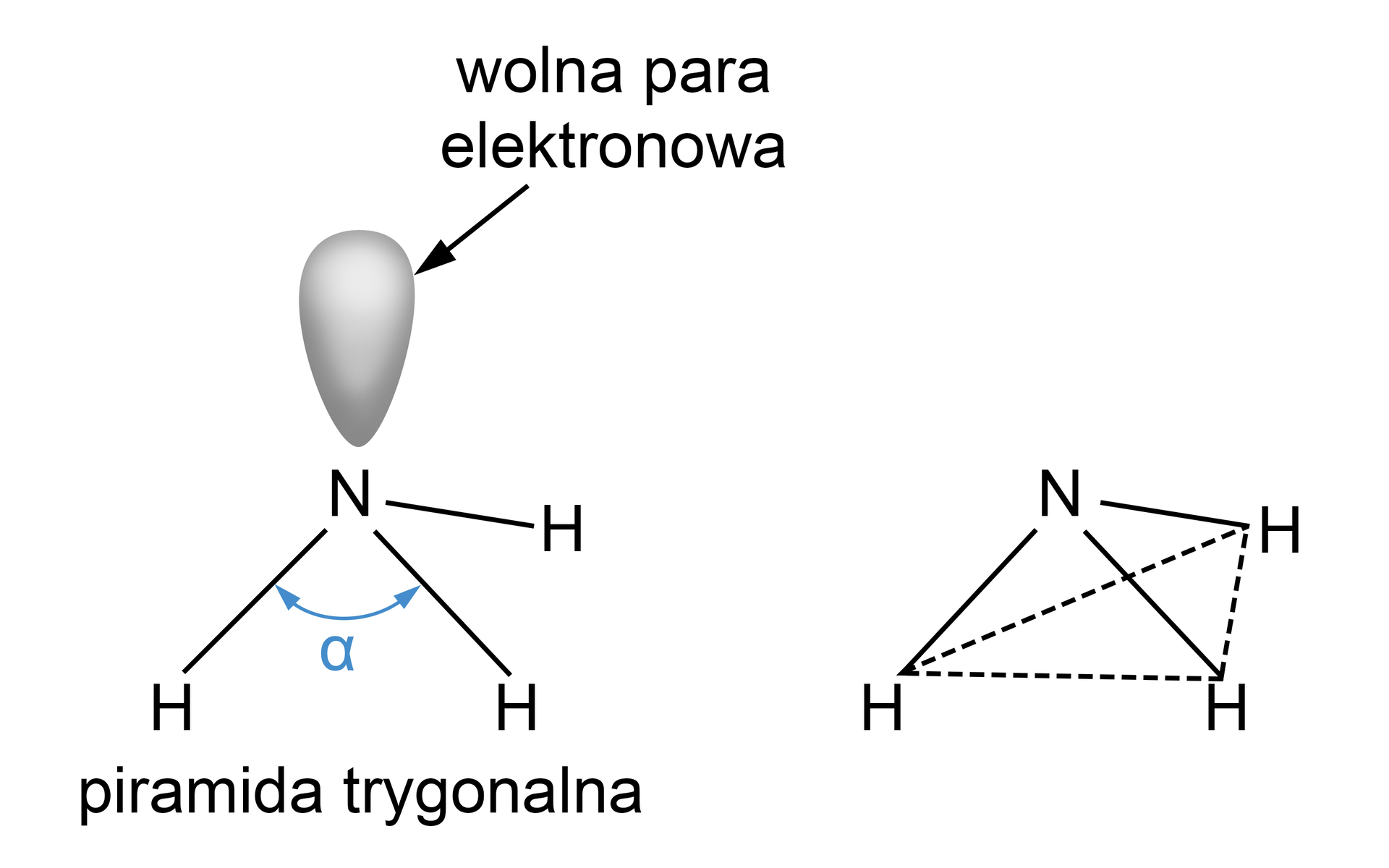
- sumę wolnych par elektronowych atomu centralnego oraz par elektronowych sigma (σ)
- sumę wolnych par elektronowych atomu centralnego oraz par elektronowych pi (Π)
- sumę wolnych par elektronowych dowolnego atomu oraz par elektronowych pi (Π)
Ćwiczenie 2
Połącz w pary nazwy orientacji przestrzennych z odpowiednimi związkami. orientacja dygonalna Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6. orientacja trygonalna Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6. orientacja tetragonalna (tetraedryczna) Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6. orientacja pentagonalna Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6. orientacja heksagonalna Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6. orientacja heptagonalna Możliwe odpowiedzi: 1. , 2. , 3. , , , 4. , , 5. , , , 6.
IF<sub>7</sub>, CO<sub>2</sub>, BeCl<sub>2</sub>, HCN, PCl<sub>5</sub>, NH<sub>4</sub><sup>+</sup>, CH<sub>4</sub>, SF<sub>6</sub>, CO<sub>3</sub><sup>2-</sup>, BF<sub>3</sub>, NO<sub>3</sub><sup>-</sup>
| orientacja dygonalna | |
| orientacja trygonalna | |
| orientacja tetragonalna (tetraedryczna) | |
| orientacja pentagonalna | |
| orientacja heksagonalna | |
| orientacja heptagonalna |
Ćwiczenie 3
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 4
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 5
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 6
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 7
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 8
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 9
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Ćwiczenie 10
Wymyśl pytanie na kartkówkę związane z tematem materiału.
W oparciu o koncepcję VSEPR uzupełnij poniższą tabelkę.
typ hybrydyzacji atomu centralnego, liczba wolnych par elektronowych na atomie centralnym, liczba wiązań sigma, kształt przestrzenny, kąt między wiązaniami [°], sp3, 107, sp3, brak, tetraedr, sp3, 105, sp3, 1, piramida trygonalna, 1, 4, 5, 5, 6, 6, brak, piramida trygonalna, piramida trygonalna, tetraedr, układ kątowy, układ kątowy, 108, 108, 106, 105, 110, 109, układ kątowy, tetraedr, tetraedr, brak
| cząsteczka lub jon | NH3 | NH4+ | H2O | H3O+ |
|---|---|---|---|---|
| typ hybrydyzacji atomu centralnego | sp3 | sp3 | sp3 | sp3 |
| liczba wolnych par elektronowych na atomie centralnym | brak | 1 | ||
| liczba wiązań sigma | ||||
| kształt przestrzenny | tetraedr | piramida trygonalna | ||
| kąt między wiązaniami [°] | 107 | 105 |