Sprawdź się
Uzupełnij tekst wybierając prawidłowe określenie.
bezbarwnym, cięższym, żółtym, mało rozpoznawalnym, charakterystycznym, lżejszym
Amoniak jest lekkim, ........................................ gazem o ........................................ zapachu, drażniący błony śluzowe. Amoniak jest gazem ........................................ od powietrza.
Zaznacz prawidłowe stwierdzenie. Może być więcej niż jedna poprawna odpowiedź.
- metoda bezpośredniej syntezy
- reakcja mocnej zasady na sole amonowe w podwyższonej temperaturze
- termiczny rozkład soli amonowych
- reakcja słabej zasady na sole amonowe w temperaturze pokojowej
- rozkład soli amonowych pod wpływem kwasu solnego.
W 1918 r. Fritz Haber otrzymał Nagrodę Nobla z chemii za opracowanie przemysłowej metody syntezy amoniaku: . Reakcję prowadzi się w wysokiej temperaturze w obecności heterogenicznego katalizatora (żelaza z dodatkiem i ). W jakiej postaci najlepiej zastosować taki katalizator?
- W postaci drutu
- W postaci sproszkowanej.
- W postaci blachy
- W postaci kulek o znacznej średnicy
W oparciu o teorię VSEPR określ kształt cząsteczki amoniaku.
Ogrzewanie chlorku amonu z roztworem wodorotlenku sodu powoduje wydzielanie się amoniaku. W reakcji tej powstają także chlorek sodu i woda. Zapisz równanie opisanej reakcji.
W probówce znajduje się wodny roztwór azotanu(V) amonu. Mając do dyspozycji wodorotlenek sodu, zaproponuj doświadczalny sposób potwierdzenia obecności tego związku. Podaj słowny opis planowanego doświadczenia, obserwacje, wnioski i odpowiednie równanie reakcji.
W zależności od ilości użytego tlenu, spalanie amoniaku może prowadzić do wydzielenia się azotu lub tlenku azotu(II). Zapisz równania tych reakcji chemicznych.
Azotek litu reaguje z wodą. Produktami reakcji są wodorotlenek litu oraz amoniak. Napisz odpowiednie równanie reakcji oraz oblicz objętość amoniaku (warunki normalne), którą można otrzymać w ten sposób z 70 g azotku litu. Wynik podaj z dokładnością do pierwszego miejsca po przecinku.
Kation amonu powstaje w czasie roztwarzania gazowego amoniaku w wodzie.
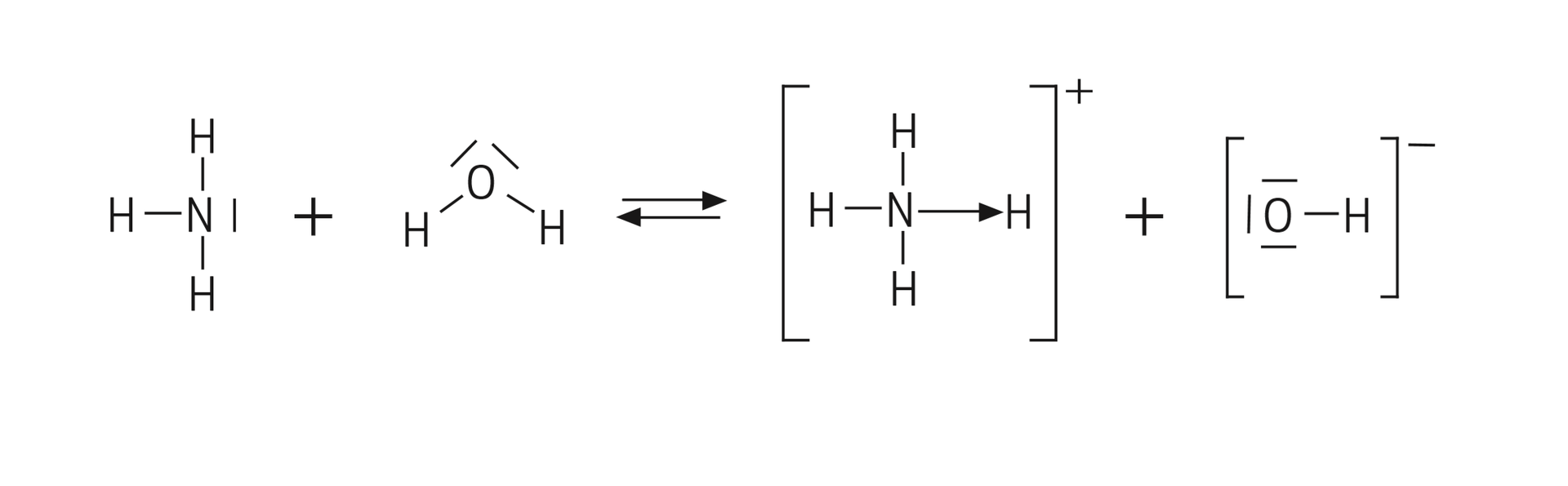
A. Napisz jonowe równanie reakcji tworzenia kationu amonu. W równaniu zastosuj wzory elektronowe, a w powstającym jonie amonu zaznacz wiązanie koordynacyjne.
A. Opisz, jak będzie przebiegało jonowe równanie reakcji tworzenia kationu amonu. Podaj wiązanie koordynacyjne.
B. Określ charakter kwasowo‑zasadowy amoniaku. Odpowiedź uzasadnij na podstawie teorii kwasów i zasad Lewisa.
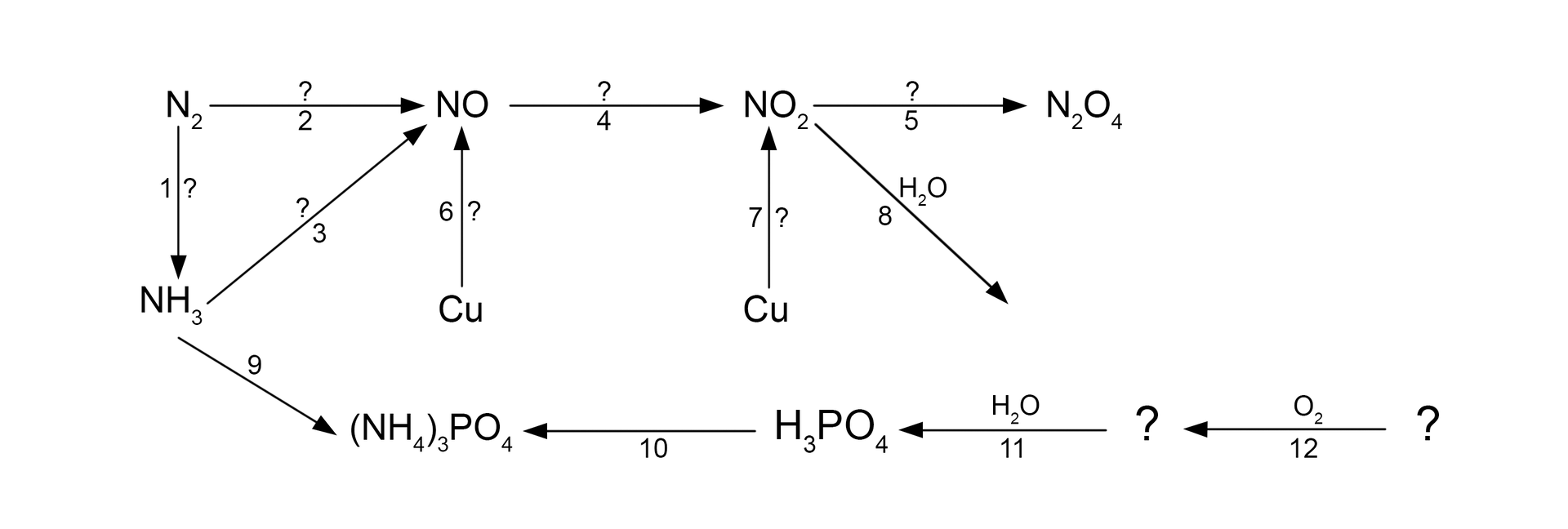
Zapisz równania reakcji zaznaczonych na poniższym schemacie.