Sprawdź się
Właściwości redukujące metanalu wynikają z posiadania przez niego:
- grupy aldehydowej.
- grupy karbonylowej.
- grupy hydroksylowej.
- grupy karboksylowej.
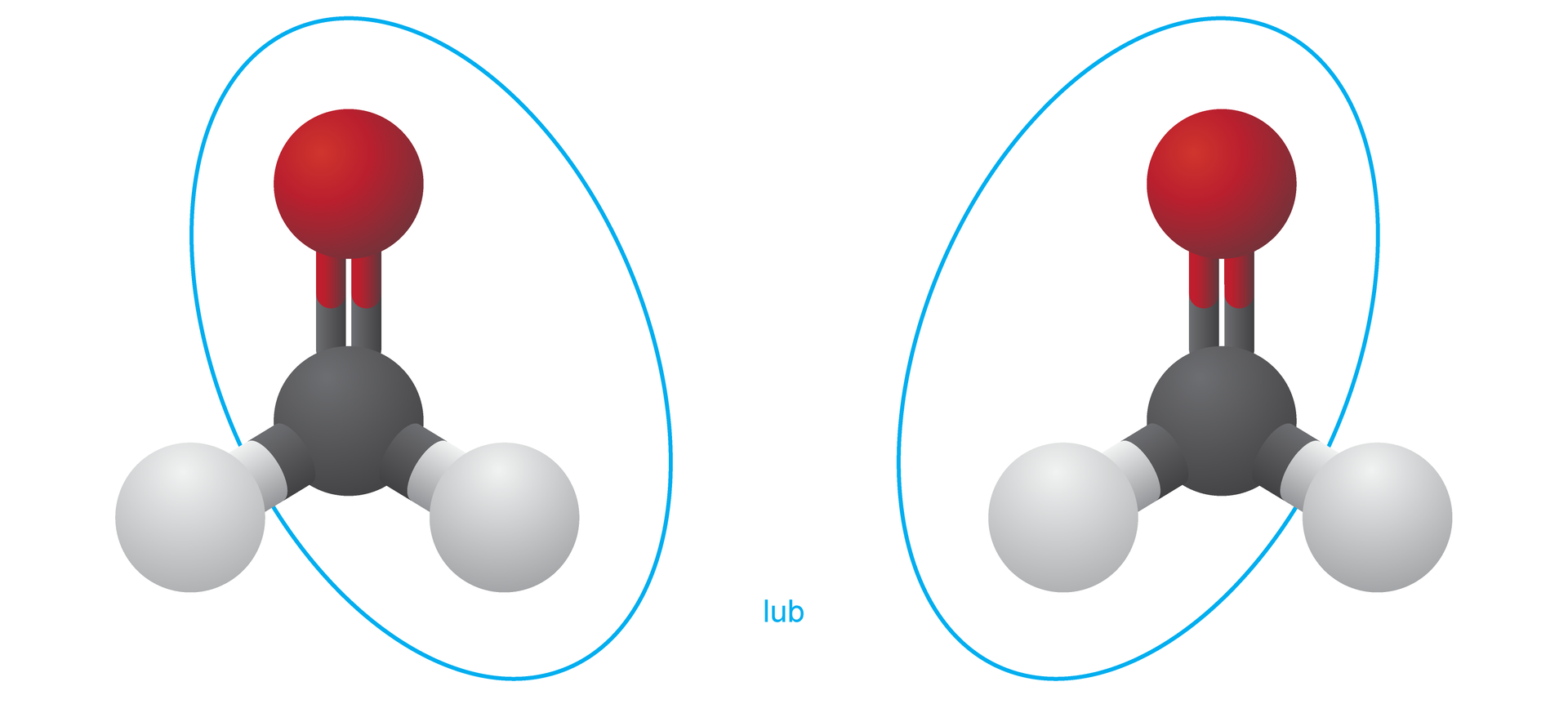
Na modelu cząsteczki metanalu zaznacz atom lub grupę atomów, które odpowiadają za jego właściwości redukujące.
Dobierz pojęcia do definicji.
Atom lub grupa atomów w związkach organicznych, która decyduje o właściwościach danego związku oraz jego przynależności do danej klasy związków., Zdolność substancji do redukowania innej substancji, przy utlenianiu samej siebie., Związek chemiczny, którego cząsteczka składa się atomu/jonu tzw. centralnego, połączonego za pomocą wiązań koordynacyjnych z ligandami.
| właściwości redukujące | |
| grupa funkcyjna | |
| związek kompleksowy |
Oceń prawdziwość zdań.
| Prawda | Fałsz | |
| Metanal posiada właściwości redukujące dzięki obecności grupy aldehydowej. | □ | □ |
| Atom węgla w cząsteczce metanalu zmienia swój stopień utlenienia z -I na I w próbie Trommera. | □ | □ |
| Nazwa zwyczajowa metanalu to aldehyd mrówkowy. | □ | □ |
| Grupa aldehydowa inaczej jest określana jako grupa formylowa. | □ | □ |
| Metanal ulega reakcji redukcji w próbie Tollensa. | □ | □ |
| Ceglastoczerwony osad, obserwowany w pozytywnej próbie Trommera z udziałem metanalu, to kwas metanowy, który powstaje w wyniku reakcji. | □ | □ |
Właściwości fizykochemiczne formaldehydu (metanalu):
Temperatura topnienia [°C] | Temperatura wrzenia [°C] | Odczyn wodnego roztworu |
|---|---|---|
-92 | -19 | obojętny |
Na podstawie powyższych informacji:
A. Określ stan skupienia formaldehydu w warunkach normalnych.
B. Określ stan skupienia formaldehydu w temperaturze -50°C.
C. Określ stan skupienia formaldehydu w temperaturze -100°C.
D. Określ stan skupienia formaldehydu w temperaturze 100°C.
E. Odpowiedz, czy formaldehyd w roztworze wodnym ulega dysocjacji elektrolitycznej?
Uzgodnij poniższe równanie reakcji, dobierając współczynniki stechiometryczne.
, , , , , , , , , ,
Formaldehyd (aldehyd mrówkowy) wykazuje właściwości redukujące, co potwierdza pozytywna próba Trommera. Poniżej przedstawiono nieuzgodnione równanie tej reakcji.
A. Przedstaw w formie jonowej, z uwzględnieniem oddawanych i pobieranych elektronów, równania procesów reakcji redukcji i utleniania, które zachodzą podczas omawianej reakcji. Odpowiedź zanotuj w zeszycie do lekcji chemii.
B. Podaj brakujące współczynniki stechiometryczne w poniższym schemacie reakcji.
C. Oceń, która z drobin (jon/ cząsteczka) pełni w reakcji rolę:
utleniacza;
reduktora.
W próbie Trommera wykorzystano formaldehyd (metanal). W wyniku reakcji powstało 1,44 g tlenku miedzi(I). Oblicz, ile moli i gramów formaldehydu wzięło udział w reakcji. Do obliczeń należy użyć mas atomowych w postaci liczb całkowitych.