Sprawdź się
Skonstruuj mapę myśli, przedstawiającą przykłady soli wapnia w przyrodzie.
- Nazwa kategorii: SOLE WAPNIA W PRZYRODZIE
Wykorzystaj podane elementy: KALCYT (węglan wapnia), DOLOMIT (węglan wapniowo-magnezowy), SIARCZAN(VI) WAPNIA, FLUOREK WAPNIA fluoryt, FOSFORAN WAPNIA, KREDA, TRAWERTYN, MARMUR, WAPIEŃ, ANHYDRYT – bezwodny siarczan(VI) wapnia, GIPS – siarczan(VI) wapnia: woda 1/2.
-
SOLE WAPNIA W PRZYRODZIE

Mapa przedstawia występowanie wapieni na terenie Polski. Na podstawie posiadanych danych, wybierz obszary, gdzie wydobywany jest wapień.
- Góry Świętokrzyskie
- obszar śląsko-krakowski
- pasmo krakowsko-wieluńskie
- Karpaty
- Dolny Śląsk
- Mazury
- obszar Słowińskiego Parku Narodowego
- Bieszczady
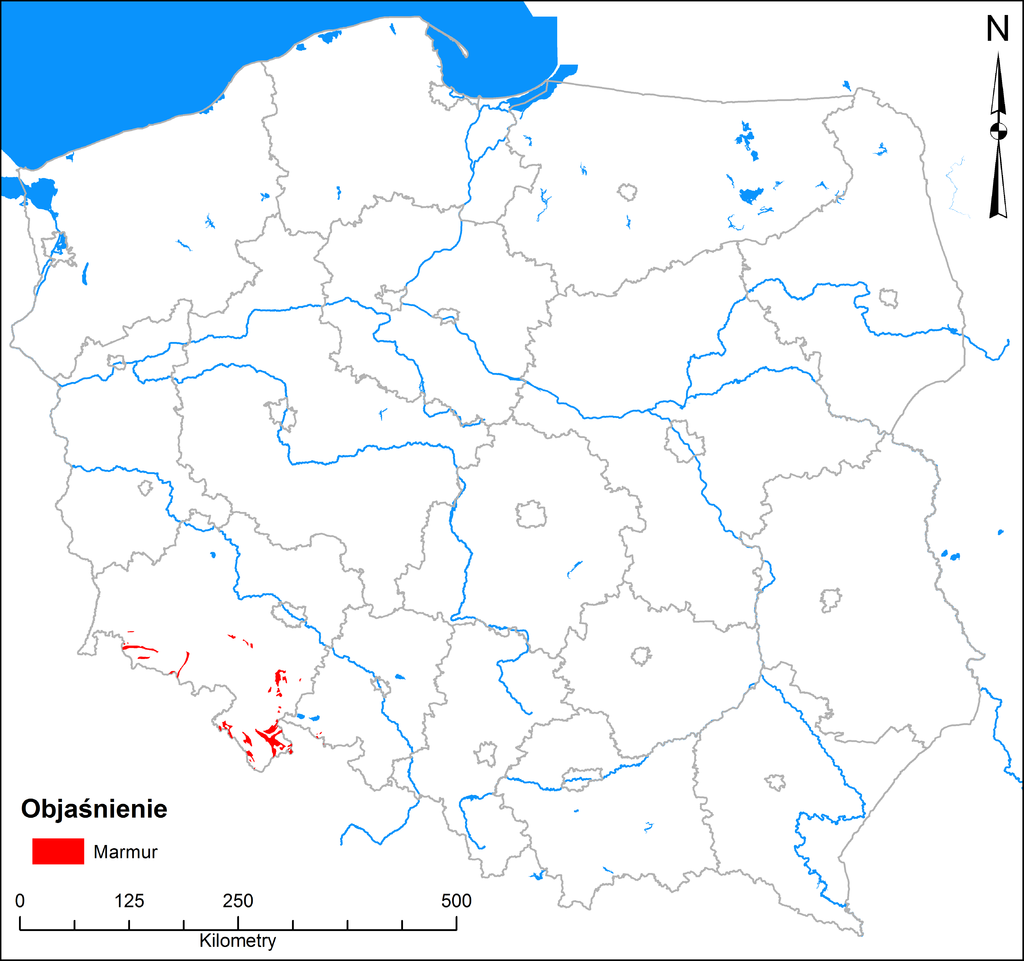
Sudetach, Karpatach, Kotlinie Sandomierskiej, Bieszczadach
W Polsce marmur wydobywany jest jedynie w ...............................................

Na podstawie danych z 2012 r., zawartych w powyższej tabeli, wskaż, które ze zdań są prawdziwe.
- W województwie wielkopolskim nie prowadzi się wydobycia gipsu i anhydrytu.
- Największe wydobycie gipsu i anhydrytu jest w województwie świętokrzyskim.
- W województwach podkarpackim i dolnośląskim jest w sumie osiem złóż.
- Ze złoża Borków-Chwałowice wydobywa się więcej skał wapiennych niż ze złoża Leszcze.
Uczeń przeprowadził doświadczenie, które zilustrował schematem:
Uczeń przeprowadził doświadczenie. Zapoznaj się z jego opisem.

Zapisz, jakich obserwacji powinien dokonać uczeń.
Wzór dowolnego związku chemicznego określa nie tylko jego skład jakościowy, ale również skład ilościowy. Oblicz procentową (w procentach wagowych) zawartość wapnia w tej soli o wzorze sumarycznym . Skorzystaj ze wzoru sumarycznego i układu okresowego pierwiastków.
Na zajęciach laboratoryjnych uczniowie mają zaprojektować zestaw do przeprowadzenia doświadczenia – badanie zachowania się węglanu wapnia pod wpływem ogrzewania.
Zaprojektuj odpowiedni zestaw doświadczalny. Zaznacz, jakich odczynników chemicznych spotrzebujesz do przeprowadzenia reakcji i analizy powstającego produktu. Zapisz równanie reakcji chemicznej, zachodzącej w i probówce.
Zaznacz, jakie odczynniki chemiczne i jaki sprzęt laboratoryjny potrzebujesz do przeprowadzenia podanych reakcji.
- wodę destylowaną
- palnik
- dwie zlewki
- naczynie z lodem
- dwie probówki
- stały węglan wapnia
- szklaną rurkę
- wodę wapienną
- korek
CO2↑, CO, H2CO3, CO2, H2O, H2O, Ca
Reakcja zachodząca w I probówce:
CaCO3 →T→ CaO + ............
Reakcja zachodząca w II probówce:
............ + Ca(OH)2 → CaCO3↓ + ............
