Sprawdź się
Zaznacz poprawną odpowiedź.
- Sublimacja nie jest przemianą fazową.
- Sublimacja jest przejściem ciała stałego w gaz.
- Sublimacja jest przejściem gazu w ciało stałe.
- Sublimacja jest procesem odwrotnym do krzepnięcia.
Pogrupuj elementy:
Które z poniższych przemian fazowych powodują wzrost, a które zmniejszenie entropii?
resublimacja, krystalizacja, topnienie, skraplanie, sublimacja, parowanie
| wzrost entropii | |
|---|---|
| zmniejszenie entropii |
Zaznacz poprawną odpowiedź.
W którym z procesów nastąpi wzrost entropii?
- w żadnym z wymienionych
Zaznacz prawidłową odpowiedź.
- Gazy mają większą gęstość niż ciecze.
- Ze wzrostem temperatury entropia rośnie.
- Przy przejściu gazu w ciało stałe entropia rośnie.
- Entropia rośnie wraz ze wzrostem stopnia uporządkowania atomów.
Nazwij poszczególne przemiany fazowe, przyporządkowując cyfrom daną nazwę przemiany:
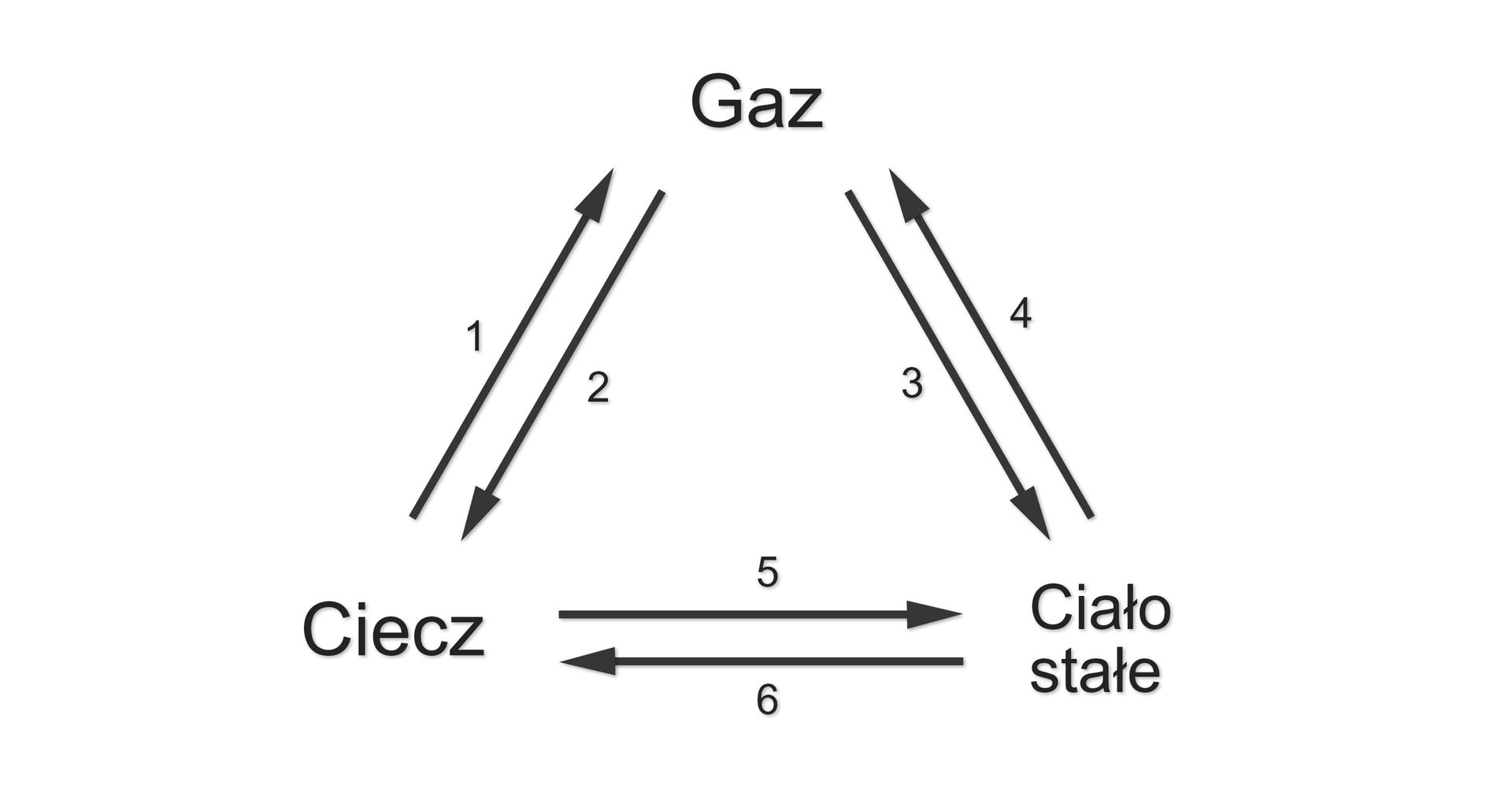
2 - 1. parowanie, 2. topnienie, 3. resublimacja, 4. skraplanie, 5. krzepnięcie, 6. sublimacja
3 - 1. parowanie, 2. topnienie, 3. resublimacja, 4. skraplanie, 5. krzepnięcie, 6. sublimacja
4 - 1. parowanie, 2. topnienie, 3. resublimacja, 4. skraplanie, 5. krzepnięcie, 6. sublimacja
5 - 1. parowanie, 2. topnienie, 3. resublimacja, 4. skraplanie, 5. krzepnięcie, 6. sublimacja
6 - 1. parowanie, 2. topnienie, 3. resublimacja, 4. skraplanie, 5. krzepnięcie, 6. sublimacja
skraplanie, krzepnięcie, topnienie, sublimacja, resublimacja, parowanie
1 — ........................
2 — ........................
3 — ........................
4 — ........................
5 — ........................
6 — ........................
Który z poniższych rysunków przedstawia uporządkowanie cząsteczek typowe dla ciał stałych, który dla cieczy, a który dla gazów? Wstaw odpowiedzi w odpowiednie miejsca.
Zapoznaj się z poniższym tekstem, a następnie odpowiedz na pytanie.
Jakie wnioski wysuniesz z podanych w tabeli molowych entropii standardowych różnych substancji podczas analizy ich stanów skupienia?
Substancja | S°Indeks dolny mm [] |
|---|---|
amoniak, | 192,5 |
azot, | 191,6 |
dwutlenek węgla, | 213,7 |
hel, | 126,2 |
tlen, | 205,1 |
woda (para), | 188,8 |
chlorek sodu, | 72,1 |
diament, C | 2,4 |
grafit, | 5,7 |
miedź, | 33,2 |
węglan wapnia, | 92,9 |
woda (s) | 45,0 |
Zapisz za pomocą wzorów, jak obliczysz zmianę entropii poniższej reakcji.