Sprawdź się
Połącz w pary poniższe pojęcia z ich wyjaśnieniem.
czyli taki, który może wymieniać z otoczeniem materię i energię, czyli taki, który nie może i nie wymienia z otoczeniem ani materii, ani energii, czyli taki, który nie wymienia z otoczeniem materii chemicznej, lecz może wymieniać z otoczeniem energię
| układ otwarty | |
| układ zamknięty | |
| układ izolowany |
Jak brzmi III zasada termodynamiki?
| Zdanie | Prawda | Fałsz |
| Wartość entropii dla kryształu idealnego wynosi w temperaturze . | □ | □ |
| Układem są wszystkie elementy zewnętrzne, które nie biorą udziału w danej reakcji chemicznej, a otoczeniem są reagenty biorące udział w danej reakcji chemicznej. | □ | □ |
| Układ izolowany jest układem, który nie wymienia z otoczeniem materii chemicznej, lecz może wymieniać z otoczeniem energię. | □ | □ |
| Przemiana izotermiczna to przemiana, w wyniku której cała energia przekazana ciału w postaci ciepła jest zużywana na wykonanie pracy przez gaz. | □ | □ |
Podaj wzór dla poniższej reakcji chemicznej, pozwalający na określenie .
Zdefiniuj wielkość opisaną wzorem.
Oblicz zmiany entropii towarzyszące procesowi dla poniższego modelu. Czy otrzymany wynik jest zgodny z teorią Boltzmanna?
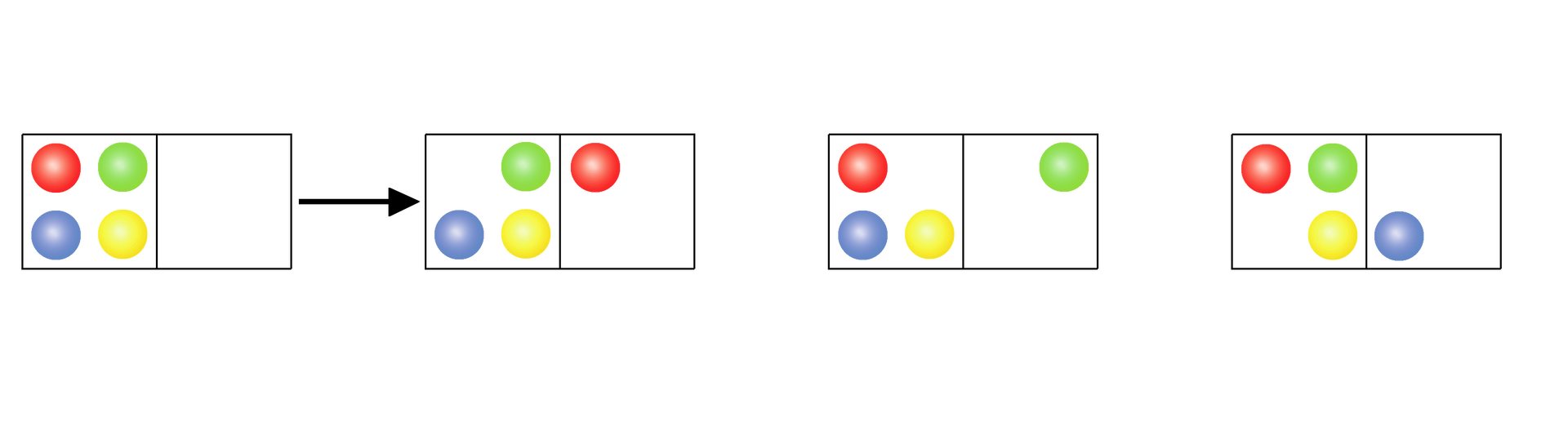
Uczeń wykonał odpowiednie obliczenia zmiany entropii całkowitej
() w celu sprawdzenia, czy lód ulega samorzutnemu roztopieniu w temperaturze -10°C oraz w 10°C.
Dla -10,00°C czyli 263,15 K | Dla 10,00°C czyli 283,15 K |
|---|---|
Na podstawie podanych informacji wyjaśnij, w jakich warunkach proces może być samorzutny i w jakich warunkach jest obserwowany.
Oblicz, w oparciu o podane dane, ile wynosi zmiana standardowej entropii dla poniższej reakcji:
Obliczenia przyjmij w stosunku do 1 mola tlenu.
Zapisz równanie reakcji całkowitego spalania ciekłego etanolu. Wykorzystując odpowiednie dane w tablicach, oblicz dla tej reakcji .
Oblicz zmianę standardowej entropii w trakcie reakcji addycji wodoru do propenu. Czy proces jest procesem samorzutnym? W jakich warunkach zachodzi?