Sprawdź się
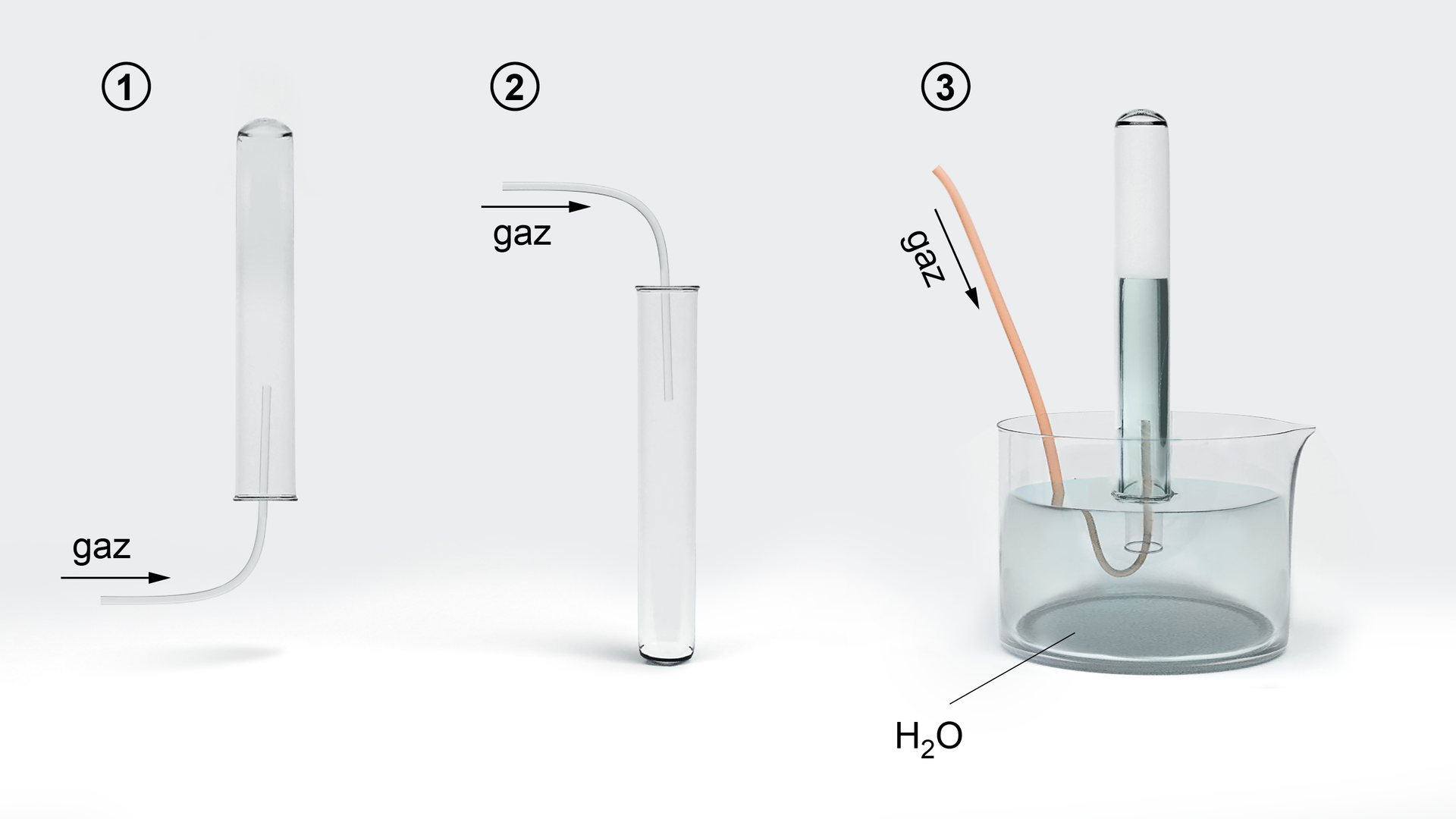
Którego z zestawów należy użyć do zbierania chloru?
Jaką objętość zajmie mola chloru w warunkach normalnych, a jaką w temperaturze i pod ciśnieniem ?
Chlor można otrzymać w reakcji synproporcjonowania kwasu chlorowego() i kwasu chlorowodorowego. Drugim produktem tej reakcji jest woda.
Zapisz równanie reakcji w formie cząsteczkowej i dobierz współczynniki, stosując metodę bilansu jonowo‑elektronowego.
Uzupełnij równania reakcji.
1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12. 1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12. 1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12. 1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12.
1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12.
1. , 2. reakcja nie zachodzi, 3. reakcja nie zachodzi, 4. , 5. , 6. , 7. , 8. , 9. , 10. , 11. , 12.
Wyjaśnij, dlaczego chlor wypiera cięższe fluorowce z ich soli?
Przeprowadzono reakcję wody chlorowej z roztworu bromku potasu o stężeniu . Oblicz masę otrzymanego bromu. Przyjmij, że wydajność reakcji wyniosła . Wynik podaj z dokładnością do .
Przeprowadzano szereg doświadczeń w celu porównania aktywności chloru, bromu i jodu. Po ich zakończeniu, sformułowano wnioski w postaci równań reakcji:
Korzystając z powyższych informacji, uszereguj badane fluorowce pod względem ich aktywności, od największej do najmniejszej (fluorowiec z największą aktywnością u góry).
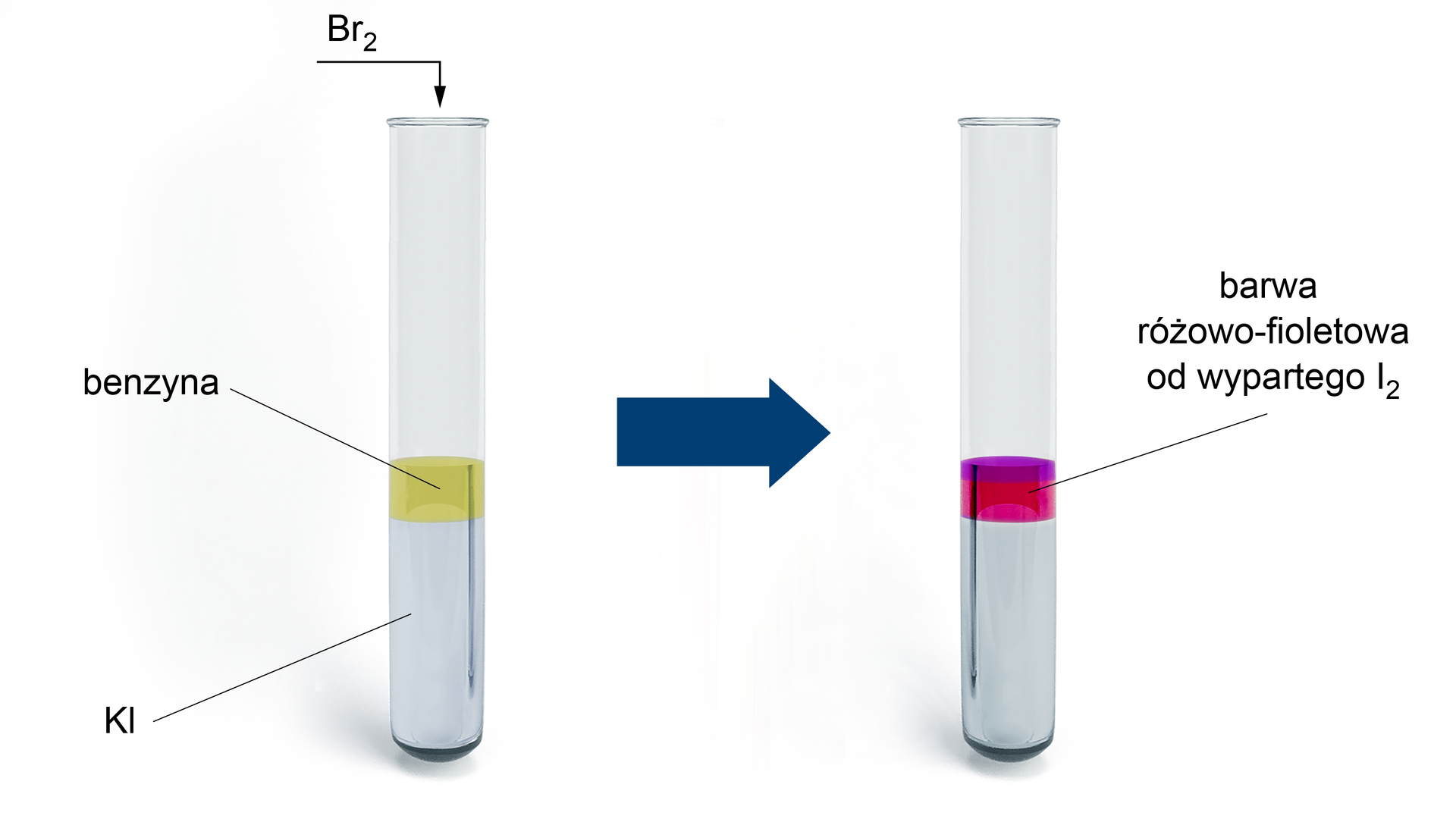
Zaproponuj doświadczenie, potwierdzające, że brom jest pierwiastkiem bardziej aktywnym od jodu. Narysuj schemat w zeszycie do chemii. Podaj obserwacje.