Tlenek krzemu - jego odmiany i właściwości fizykochemiczne
Tlenek krzemu()
Tlenek krzemu(), zwany krzemionką, jest związkiem bardzo rozpowszechnionym w przyrodzie. Stanowi skorupy ziemskiej, a jeśli uwzględnimy jego obecność w minerałach, gdzie występuje w postaci związanej (krzemiany, glinokrzemiany), to jego zawartość osiągnie skorupy ziemskiej. Krzemionka jest zatem głównym składnikiem piasku, skał i gleb.
Struktura
Wzór empiryczny tlenku krzemu() nie oddaje jego rzeczywistej struktury w stanie stałym – tworzy on bowiem rozbudowane struktury przestrzenne.
Przyjrzyj się strukturze krzemionki i określ, z iloma atomami tlenu połączony jest atom krzemu oraz z iloma atomami krzemu połączony jest atom tlenu.
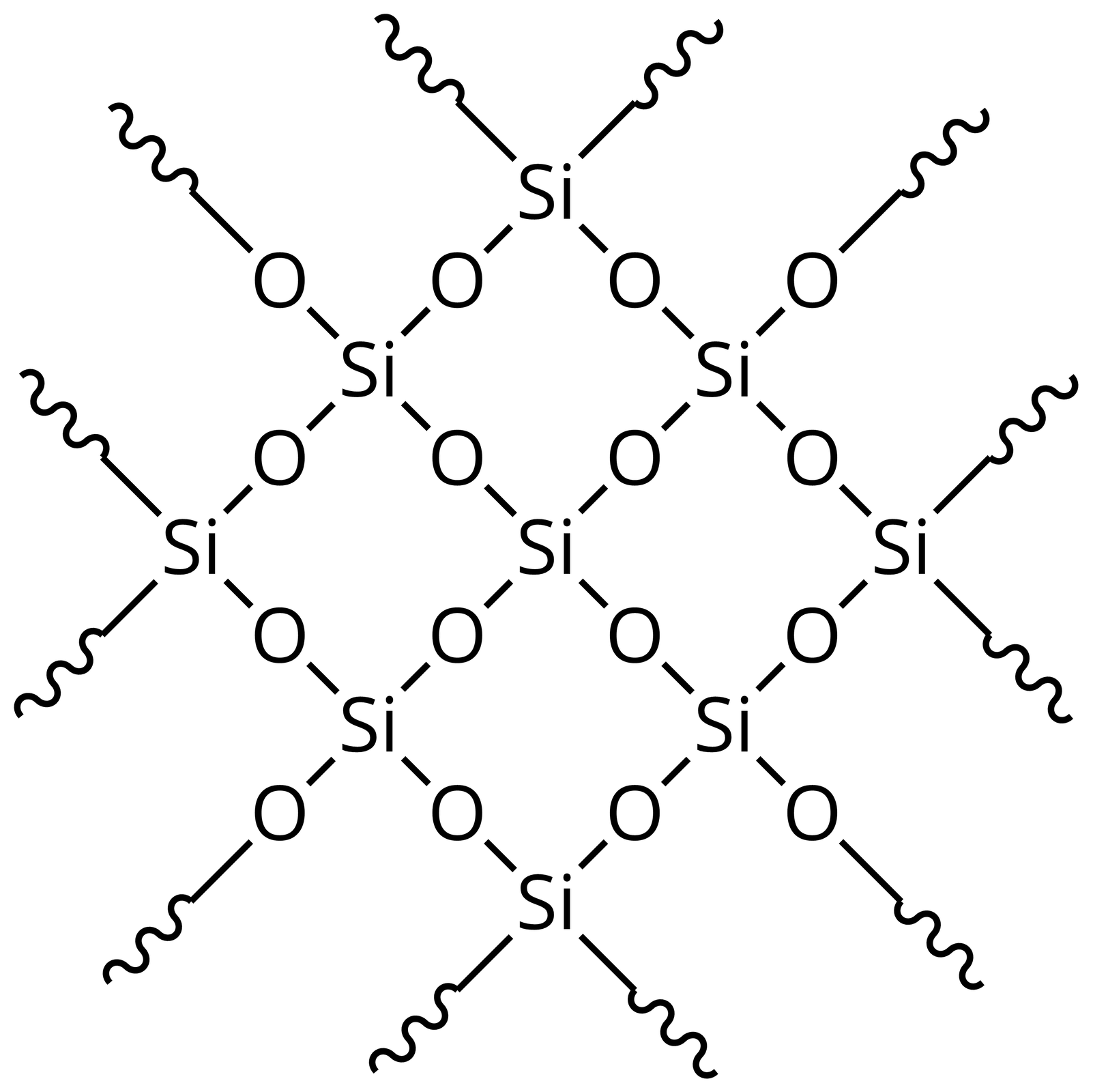
Każdy atom krzemu jest otoczony przez atomy tlenu, znajdujące się w narożach tetraedru względem tego atomu krzemu.
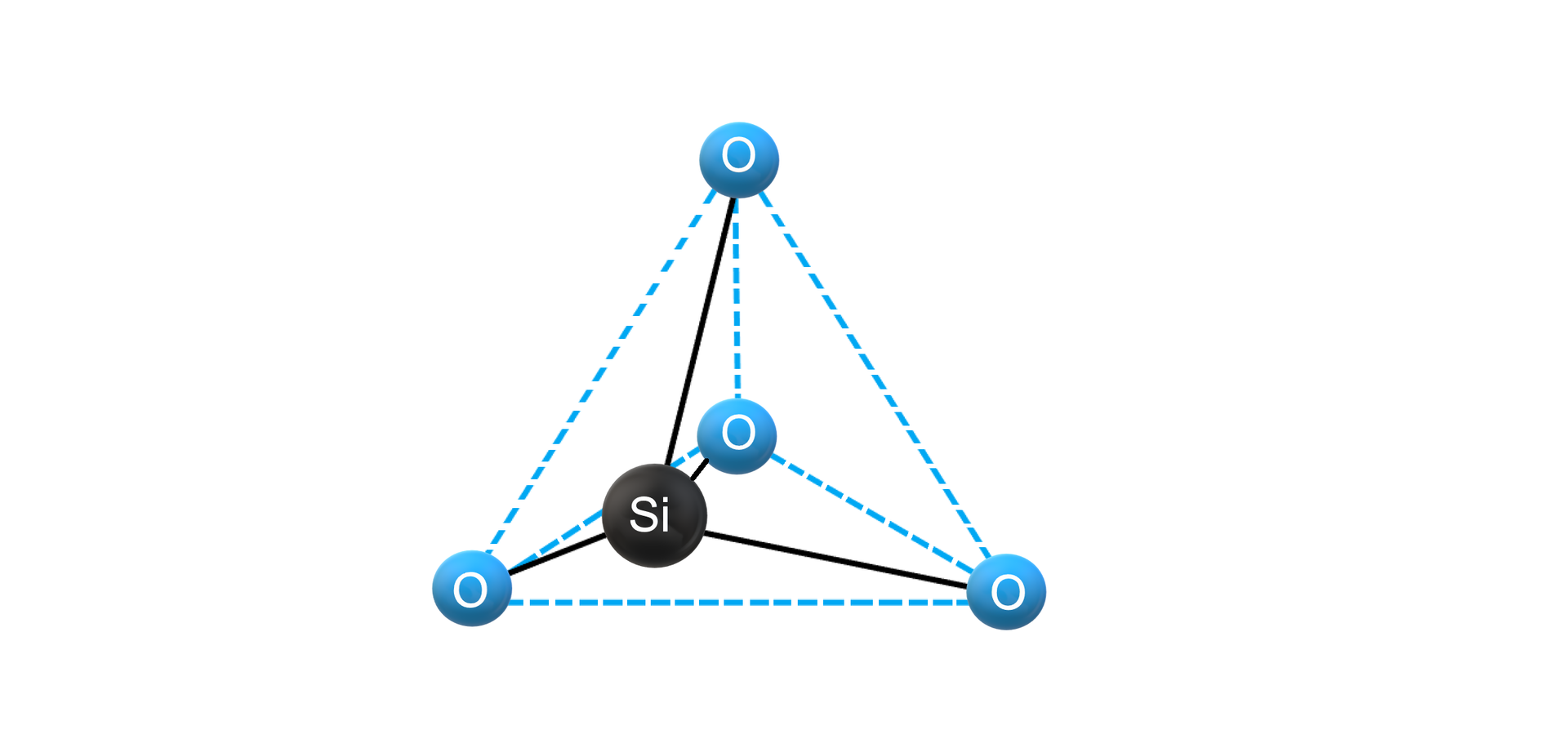
Tlenek krzemu() jest przykładem związku, który – podobnie jak diament – formułuje tzw. kryształ kowalencyjny.
Odmiany krystaliczne
Odmiany bezpostaciowe
Tlenek krzemu() jest podstawowym składnikiem piasku. Badając więc właściwości piasku, możemy jednocześnie określić właściwości tlenku krzemu().
Na podstawie przeprowadzonego doświadczenia oceń rozpuszczalność piasku, czyli w konsekwencji również tlenku krzemu() w wodzie. Zapisz wniosek, który dotyczy rozpuszczalności tlenku krzemu() w wodzie.
Na podstawie doświadczenia oceń zdolność do przewodzenia prądu przez stały tlenek krzemu().
Właściwości chemiczne
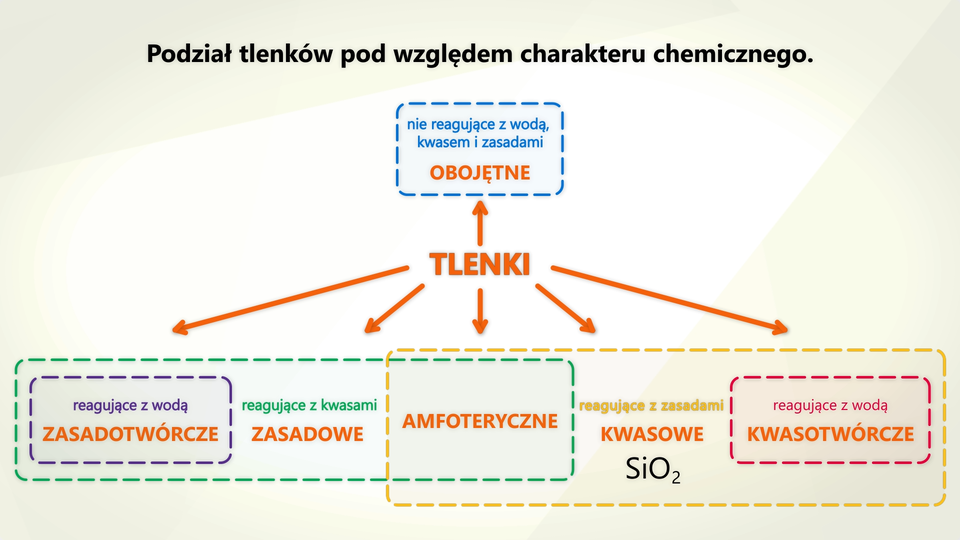
Tlenek krzemu() jest tlenkiem o charakterze kwasowym, ponieważ reaguje z wodorotlenkami, a nie reaguje z kwasami. W reakcji tlenku krzemu() z wodnym roztworem wodorotlenku sodu powstaje metakrzemian sodu i woda:
lub, przy nadmiarze wodorotlenku sodu, powstaje ortokrzemian sodu i woda:
Tlenek krzemu() ulega także analogicznej reakcji podczas stapiania z wodorotlenkiem sodu.
Tlenek krzemu() nie reaguje z wodą, zatem nie zachodzi reakcja tworzenia kwasu ani . Aby uzyskać te kwasy, należy najpierw poddać działaniu NaOH, a dopiero z otrzymanej soli uzyskać kwasy krzemowe. Zazwyczaj oprócz prostych kwasów otrzymuje się kwasy polikrzemowe, co obserwuje się za sprawą powstałego galaretowatego osadu.
Tlenek krzemu() ulega reakcji stapiania z węglanami litowców, co prowadzi do otrzymania metakrzemianów litowców. Przykładowo, reakcja tlenku krzemu() z węglanem sodu prowadzi do otrzymania metakrzemianu sodu i tlenku węgla():
lub ortokrzemianu sodu:
Jedynym kwasem, z którym wyjątkowo reaguje tlenek krzemu() już w temperaturze pokojowej, jest kwas fluorowodorowy:
Warto dodać, że jest gazem oraz że wskazany proces jest jednym z procesów. Inny to:
Proces ten zachodzi stosunkowo powoli, stąd nie przechowuje się kwasu fluorowodorowego w szklanych naczyniach.
W wysokiej temperaturze tlenek krzemu() reaguje z węglem:
Ogrzany tlenek krzemu() i magnez samorzutnie reagują ze sobą:
Zapoznaj się z poniższym filmem pt. „Właściwości fizykochemiczne tlenku krzemu”, a następnie rozwiąż zadania.
Film dostępny pod adresem /preview/resource/R1UILphaVYwRv
Film dotyczy właściwości fizykochemicznych tlenku krzemu(<math aria‑label="cztery">
krzemu(cztery) odpowiada za jego wysoką temperaturę topnienia, temperaturę wrzenia oraz twardość.. Możliwe odpowiedzi: Prawda, Fałsz. Szkło wodne to inaczej roztwór wodny krzemianu(cztery) baru.. Możliwe odpowiedzi: Prawda, Fałsz