W jaki sposób znając pH można obliczyć stężenie elektrolitu mocnego?
Obliczanie stężenia molowego roztworu mocnego kwasu na podstawie znajomości roztworu
Kwasy jednoprotonowe
Do mocnych kwasów jednoprotonowych należą np. , , , , , , .
Kwasy wieloprotonowe
Do mocnych kwasów wieloprotonowych należy np. .
Mocne kwasy wieloprotonowe dysocjujądysocjują wieloetapowo. Aby obliczyć stężenie jonów oksoniowych należy uwzględnić wartość stałej dysocjacji.
Obliczanie stężenia molowego mocnych wodorotlenków na podstawie znajomości pH roztworu
Mocne wodorotlenki, w których na jeden kation metalu przypada jeden anion wodorotlenkowy
Do mocnych wodorotlenków, w których na jeden kation metalu przypada jeden anion wodorotlenkowy należą np. , i pozostałe wodorotlenki litowców.
Mocne wodorotlenki, w których na jeden kation metalu przypadają dwa lub więcej anionów wodorotlenkowych
Do mocnych wodorotlenków, w których na jeden kation metalu przypadają dwa lub więcej anionów wodorotlenkowych, zaliczamy wszystkie wodorotlenki berylowców, z wyjątkiem wodorotlenku berylu.
Zapoznaj się z filmem, a dowiesz się, w jaki sposób obliczyć stężenie elektrolitu mocnego w roztworze, znając jedynie tego roztworu.
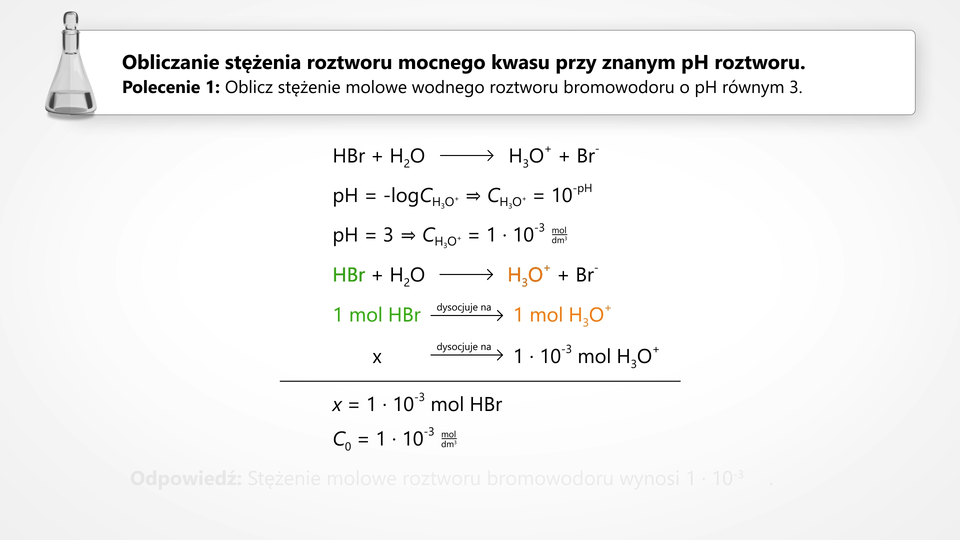
Film dostępny pod adresem /preview/resource/R16wUOFIMqOHl
Film nawiązujący do treści materiału dotyczącej obliczania stężenia mocnego elektrolitu na podstawie znajomości pH.
Oblicz stężenie molowe roztworu kwasu azotowego(V) o równym 4.
Oblicz stężenie molowe wodnego roztworu chlorowodoru, o równym 2,5. Wynik zaokrąglij do trzeciego miejsca po przecinku.
Oblicz stężenie molowe roztworu wodorotlenku litu o równym 10.
Oblicz stężenie molowe roztworu wodorotlenku baru, o równym 13.