Właściwości białek
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/bialka–wlasciwosci/D1Aexot3h
Białka stanowią masy ludzkiego ciała. Biorąc pod uwagę fakt, że około masy ciała stanowi woda, białka są jego podstawowym elementem budulcowym. W związku z tym ważne jest, aby nasza dieta była odpowiednio bogata w produkty zawierające białka. Czy wiesz, jak doświadczalnie sprawdzić, który z produktów zawiera białko? Czy znasz właściwości fizykochemiczne białek i procesy zachodzące podczas obróbki produktów zawierających białko?
budowę aminokwasów;
sposób łączenia się (kondensacji) cząsteczek aminokwasów;
produkty reakcji kondensacji aminokwasów;
definicję białka;
pierwiastki chemiczne wchodzące w skład białek.
projektować i przeprowadzać doświadczenia pozwalające na określenie, jakie pierwiastki chemiczne wchodzą w skład białek;
projektować i przeprowadzać doświadczenia pozwalające na identyfikację białek;
projektować i przeprowadzać doświadczenia pozwalające na wykrywanie białek w próbkach badanych substancji;
projektować i przeprowadzać doświadczenia pozwalające na zbadanie wybranych właściwości fizykochemicznych białek;
opisywać i analizować wyniki eksperymentów związanych z tematyką białek.
Jak zbudowane są białka?
BiałkaBiałka to wielkocząsteczkowe związki chemiczne o złożonej budowie, będące produktami reakcji kondensacji odpowiednich aminokwasów. „Wielkocząsteczkowość” białek przejawia się w ich rozmiarach i co za tym idzie – również w masach cząsteczkowych.
Cząsteczka białka składa się z co najmniej stu reszt cząsteczek aminokwasów, połączonych za pomocą wiązań peptydowych. Masy cząsteczkowe białek są zróżnicowane i wynoszą od około , do nawet kilku milionów jednostek masy atomowej (unitów).
Nie wszystkie aminokwasy mogą wchodzić w skład białek. Te z nich, które w reakcjach kondensacji mogą utworzyć białka, nazywamy aminokwasami białkowymi. Wzory półstrukturalne i nazwy wybranych aminokwasów białkowych zebrano w poniższej tabeli.
Nazwa aminokwasu | Wzór półstrukturalny | Nazwa aminokwasu | Wzór półstrukturalny |
|---|---|---|---|
Alanina | 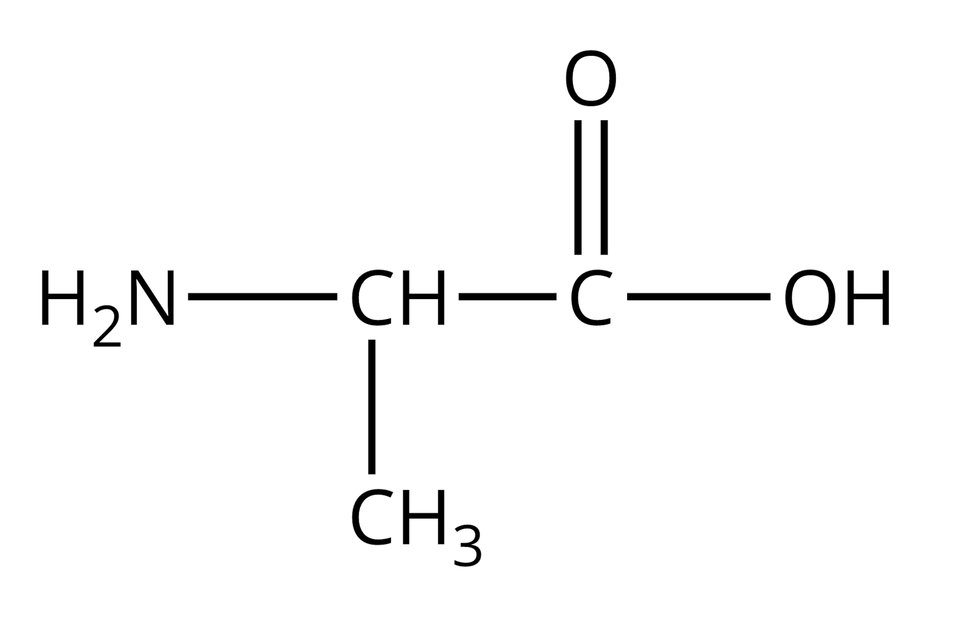 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Leucyna | 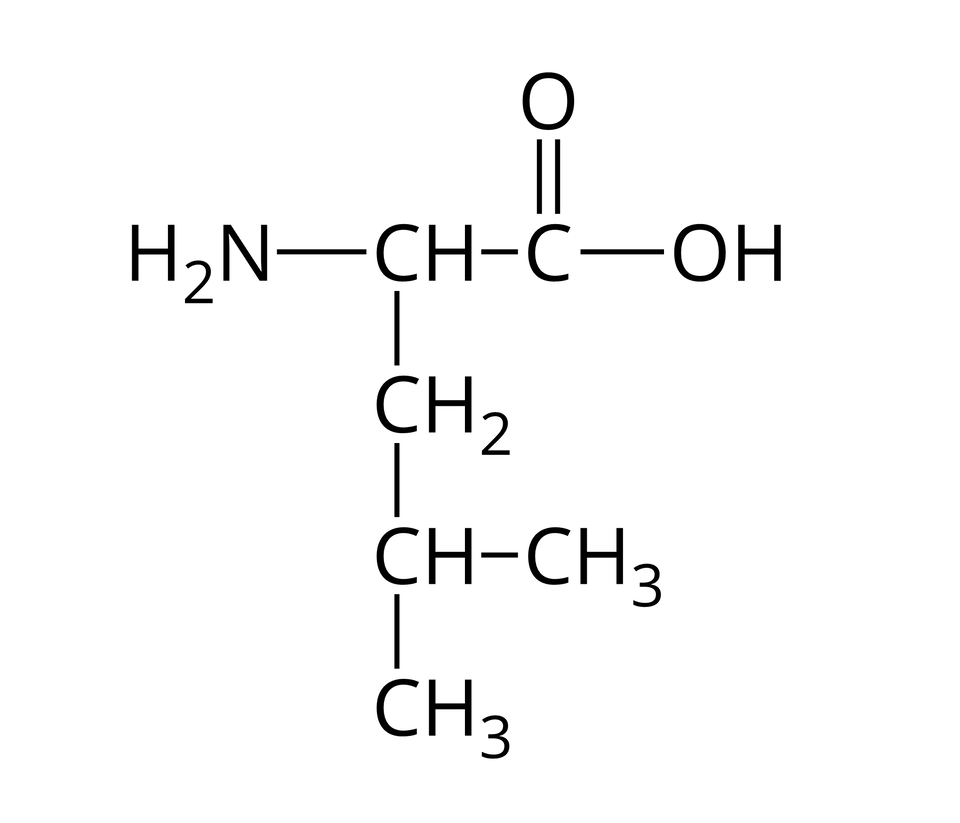 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Arginina | 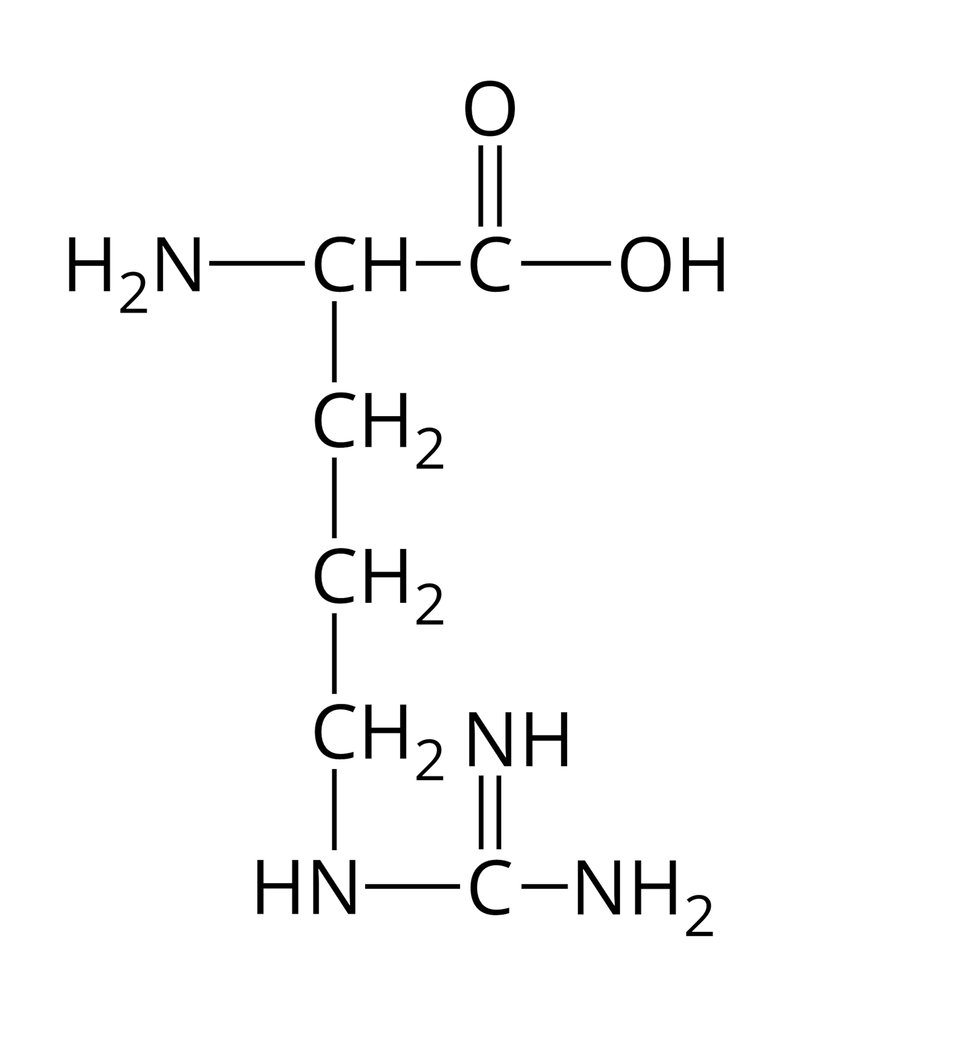 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Lizyna | 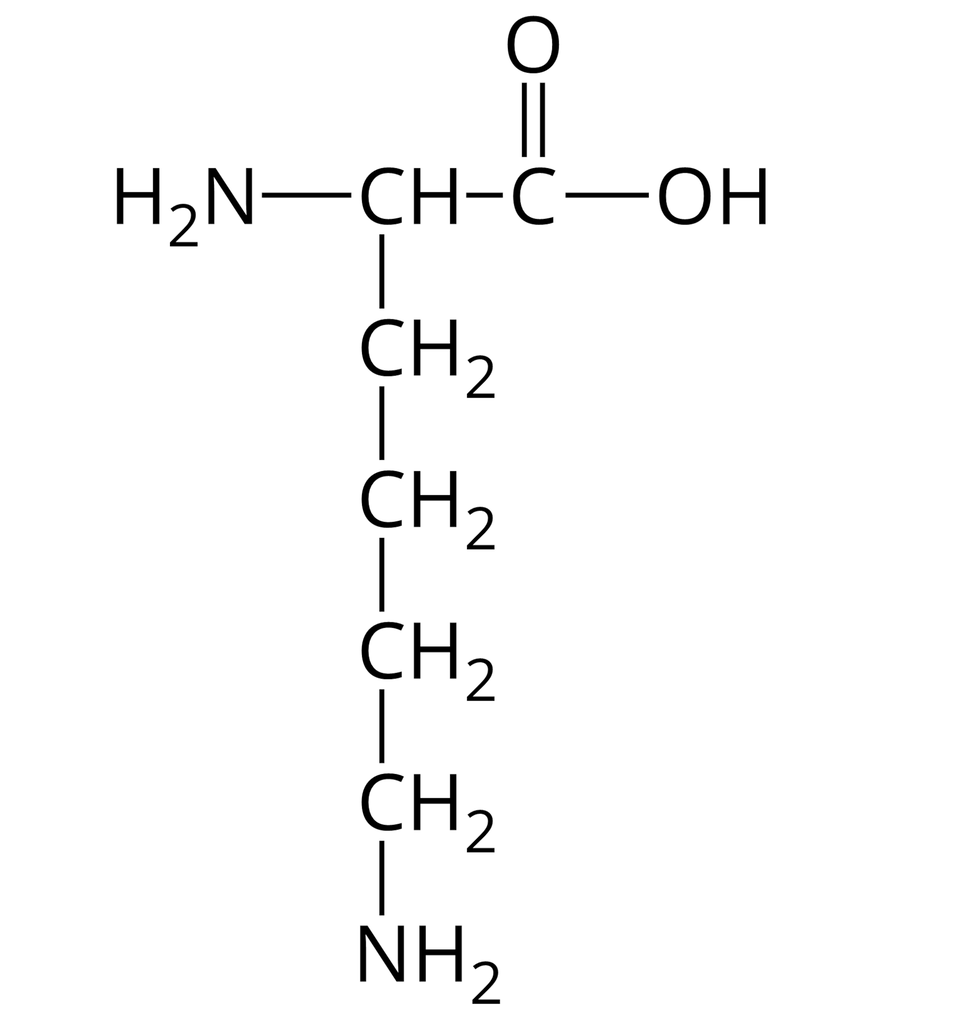 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Asparagina | 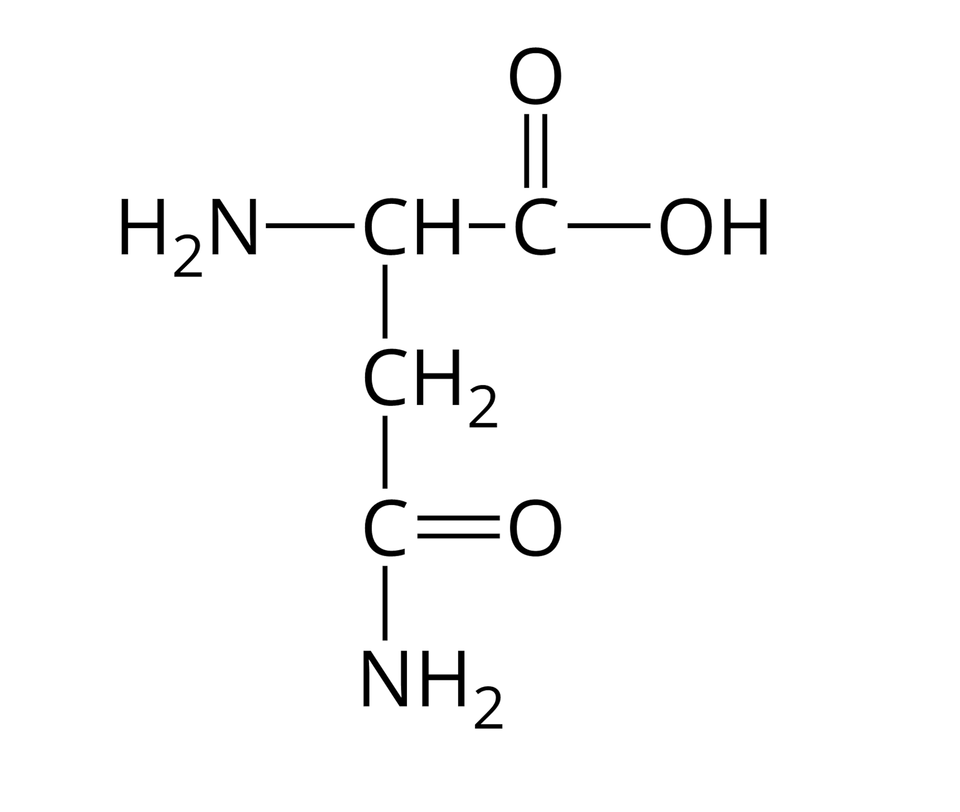 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Metionina | 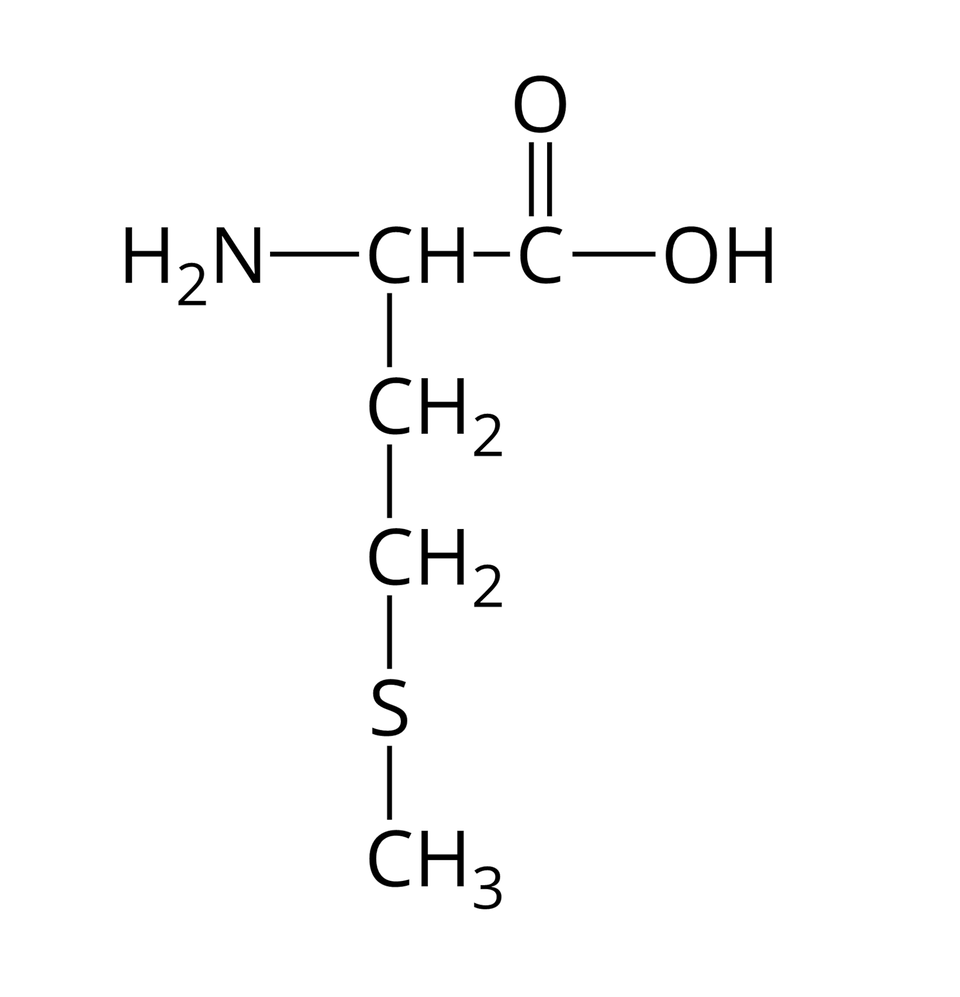 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Kwas asparaginowy | 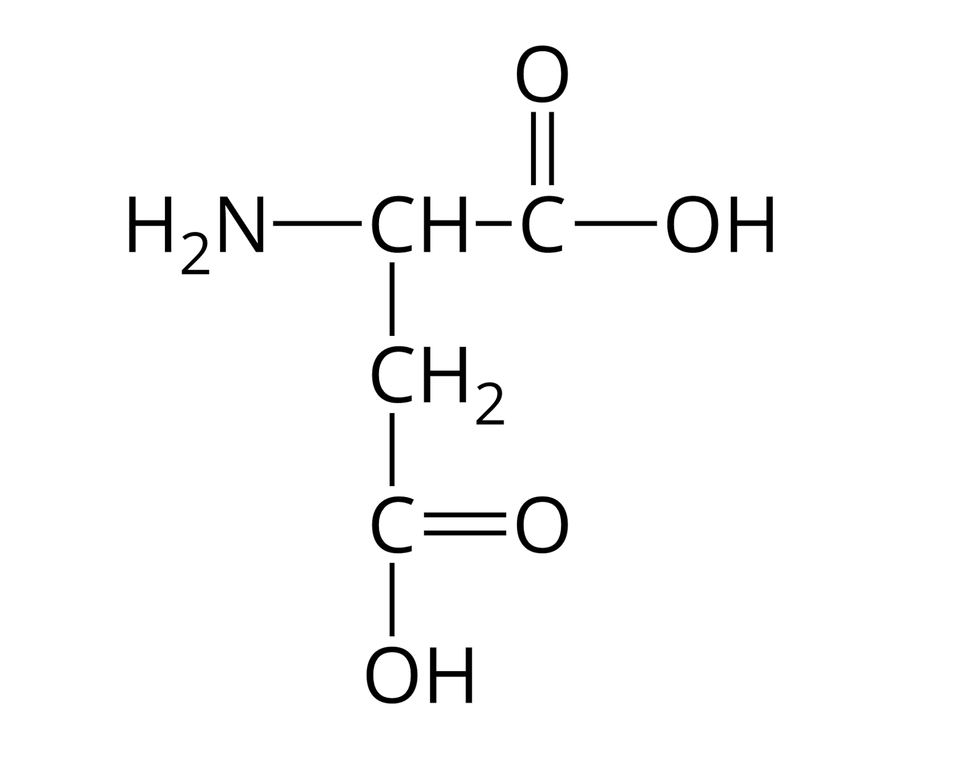 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Fenyloalanina | 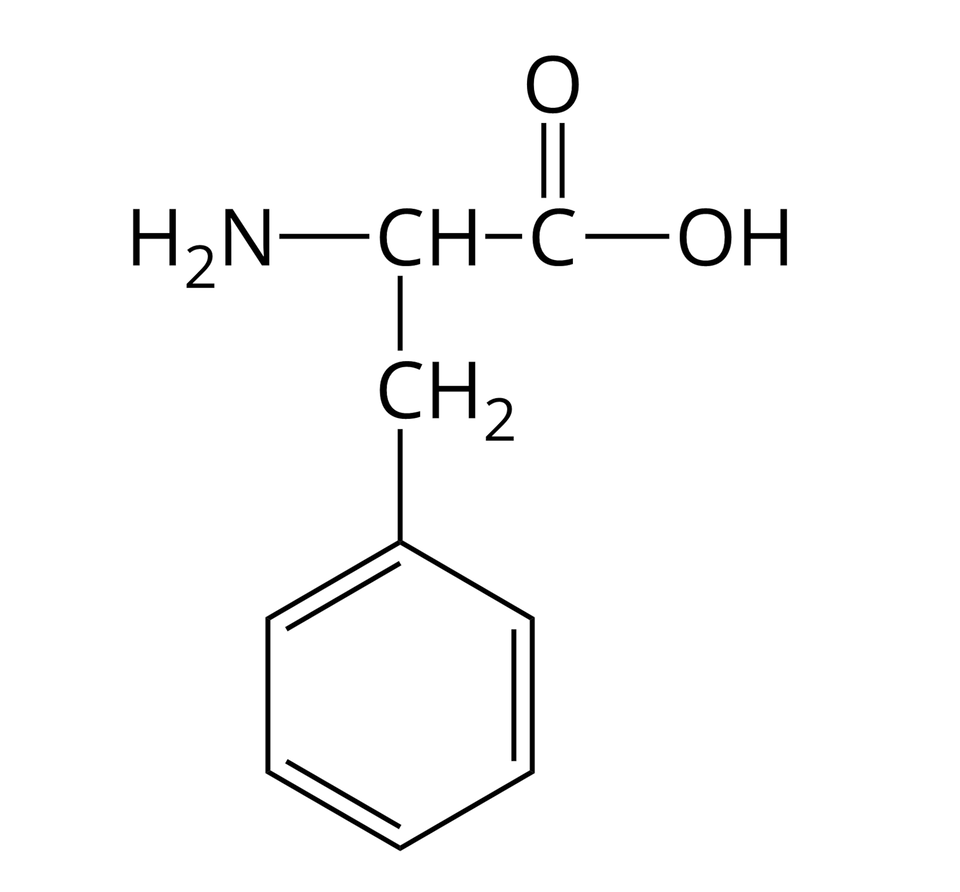 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Cysteina | 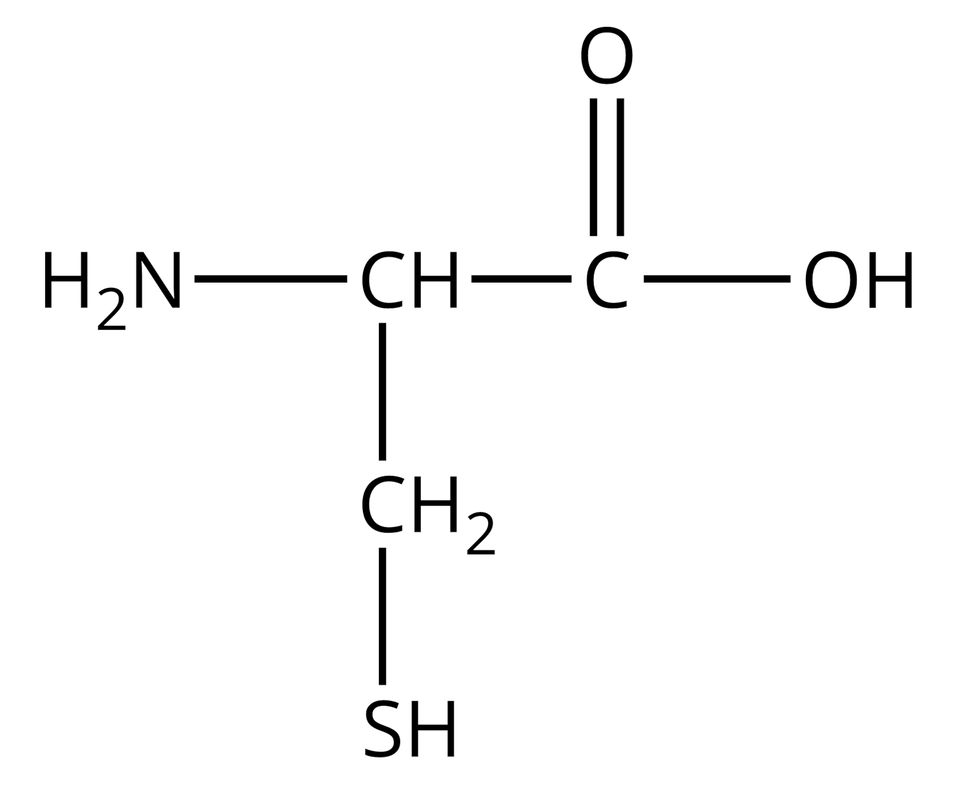 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Prolina | 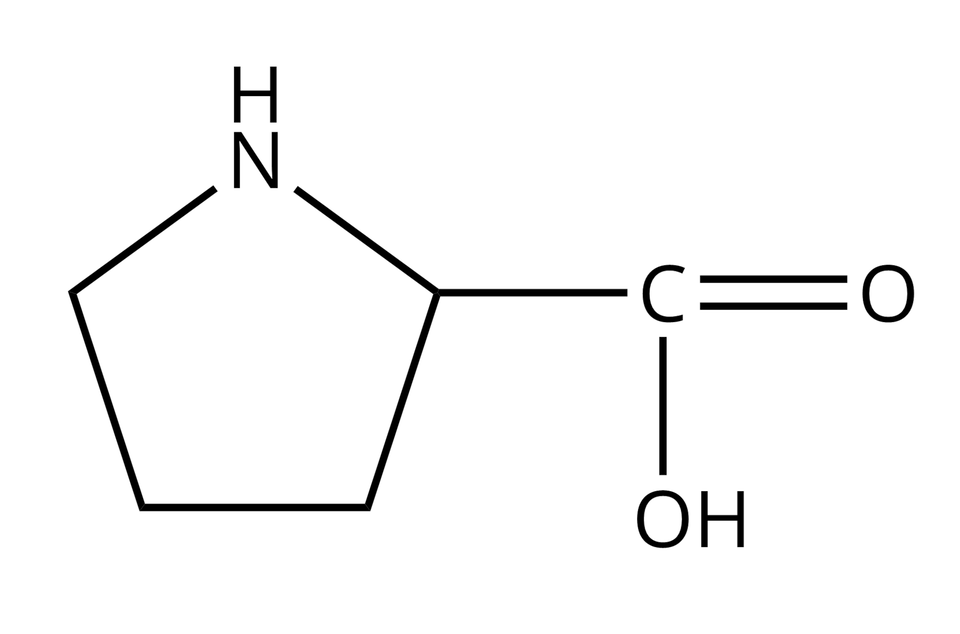 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Glicyna | 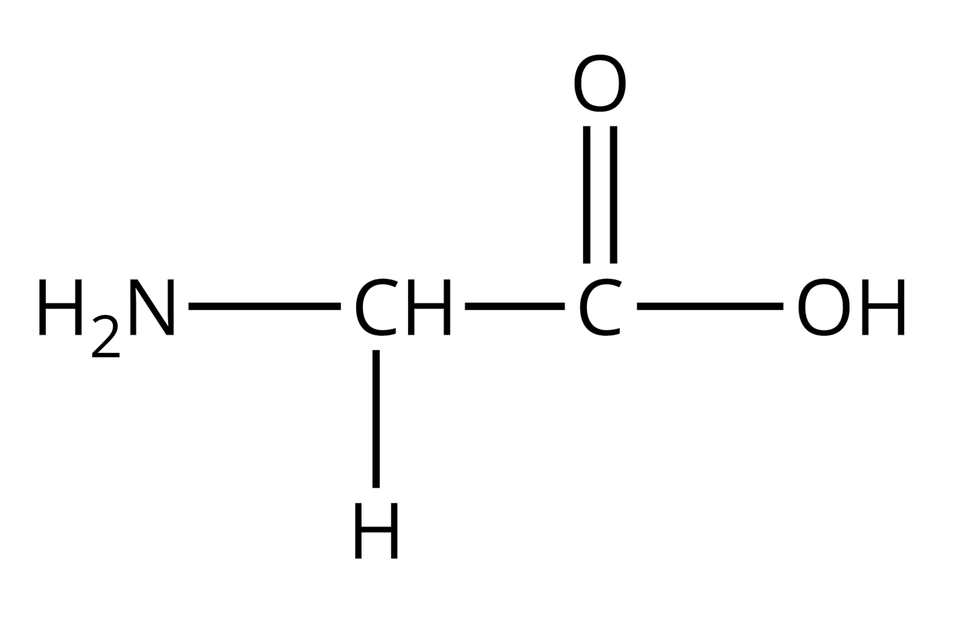 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Seryna | 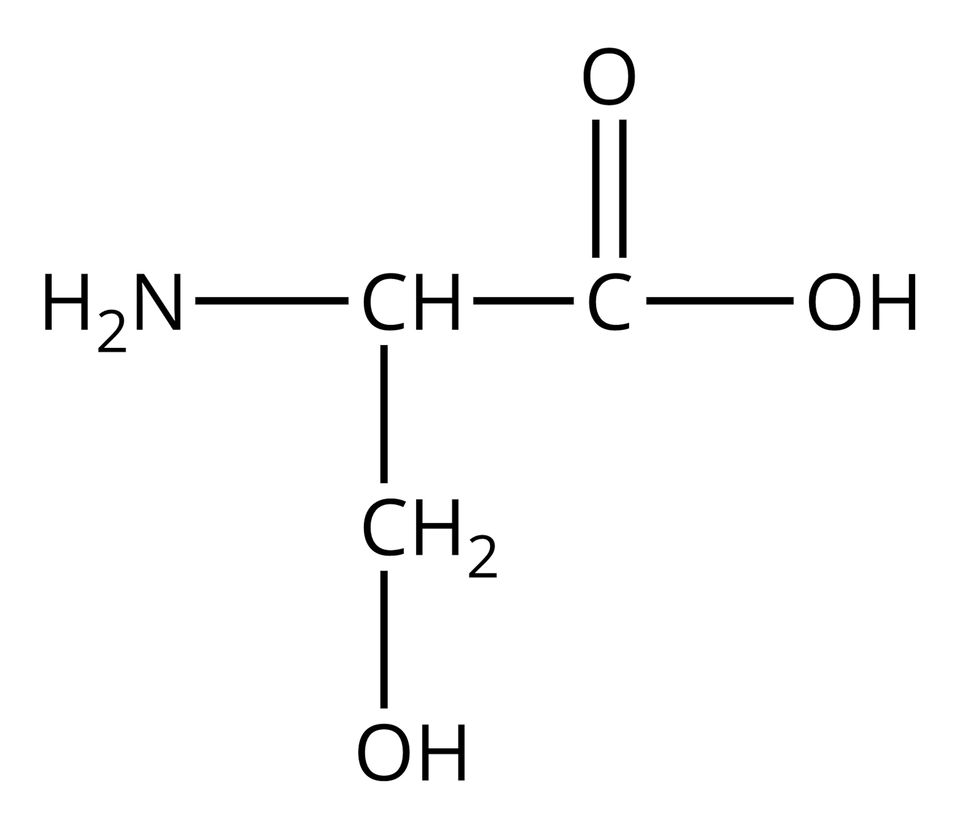 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Glutamina | 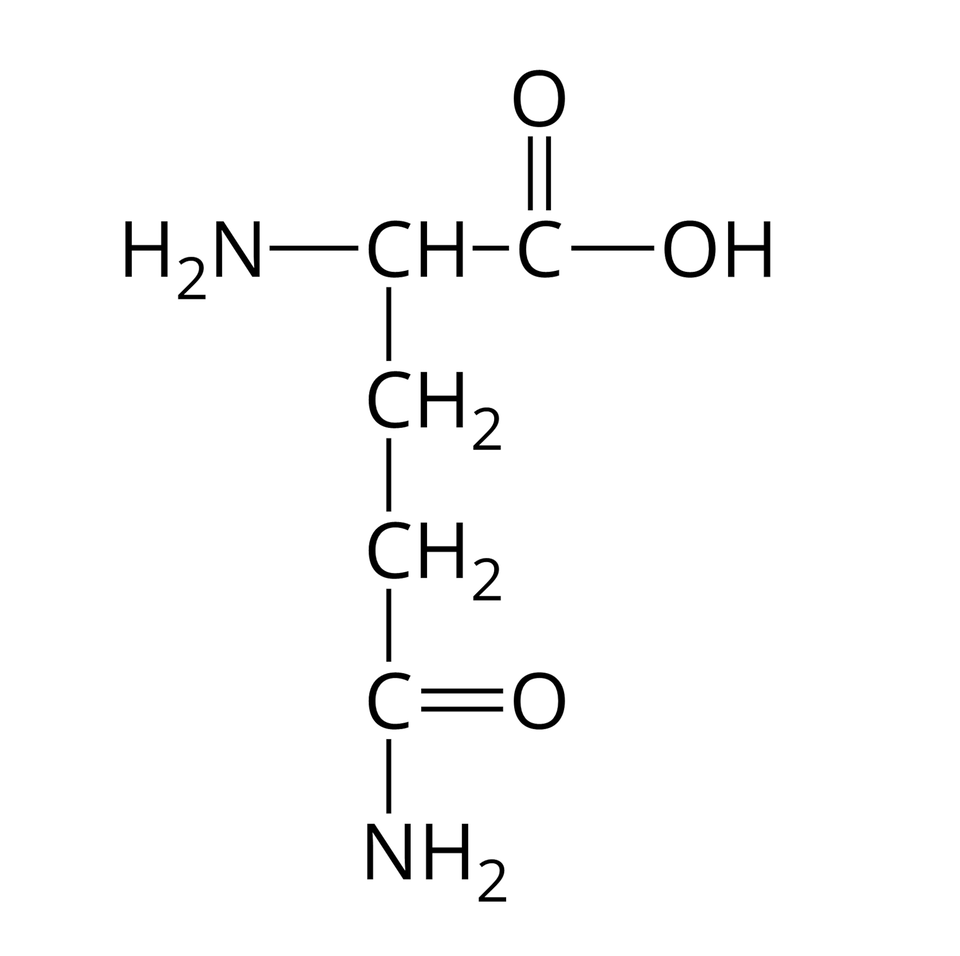 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Treonina | 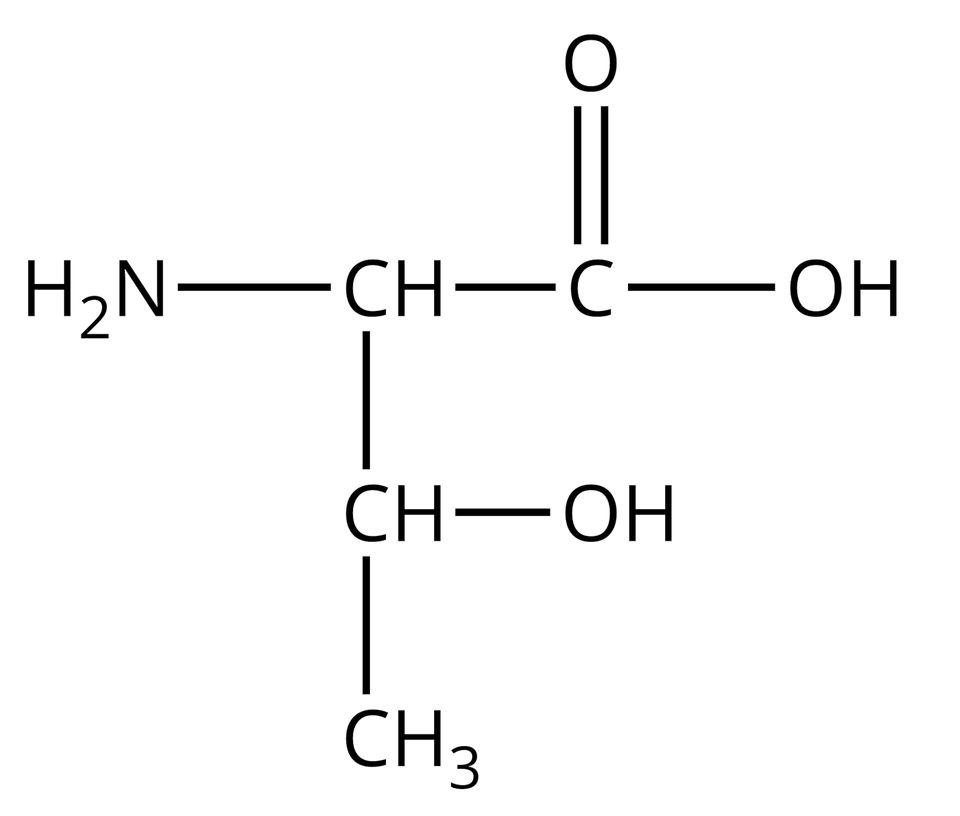 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Kwas glutaminowy | 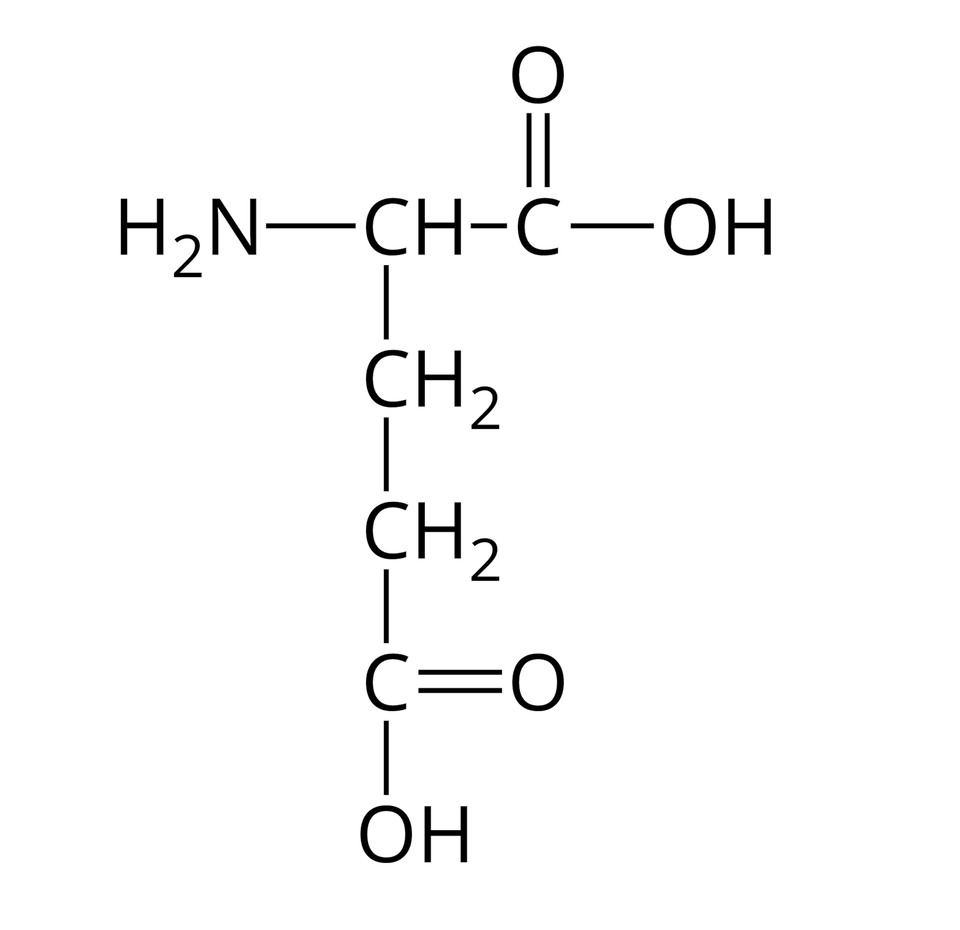 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Tryptofan | 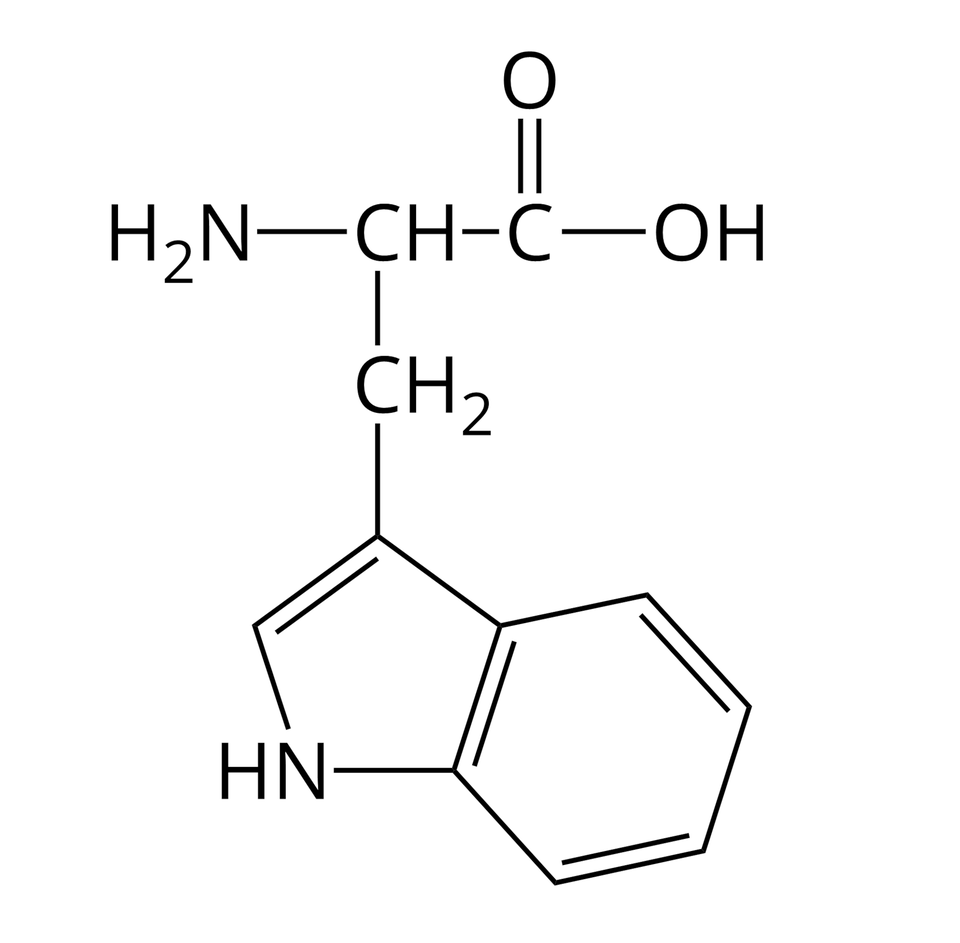 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Histydyna | 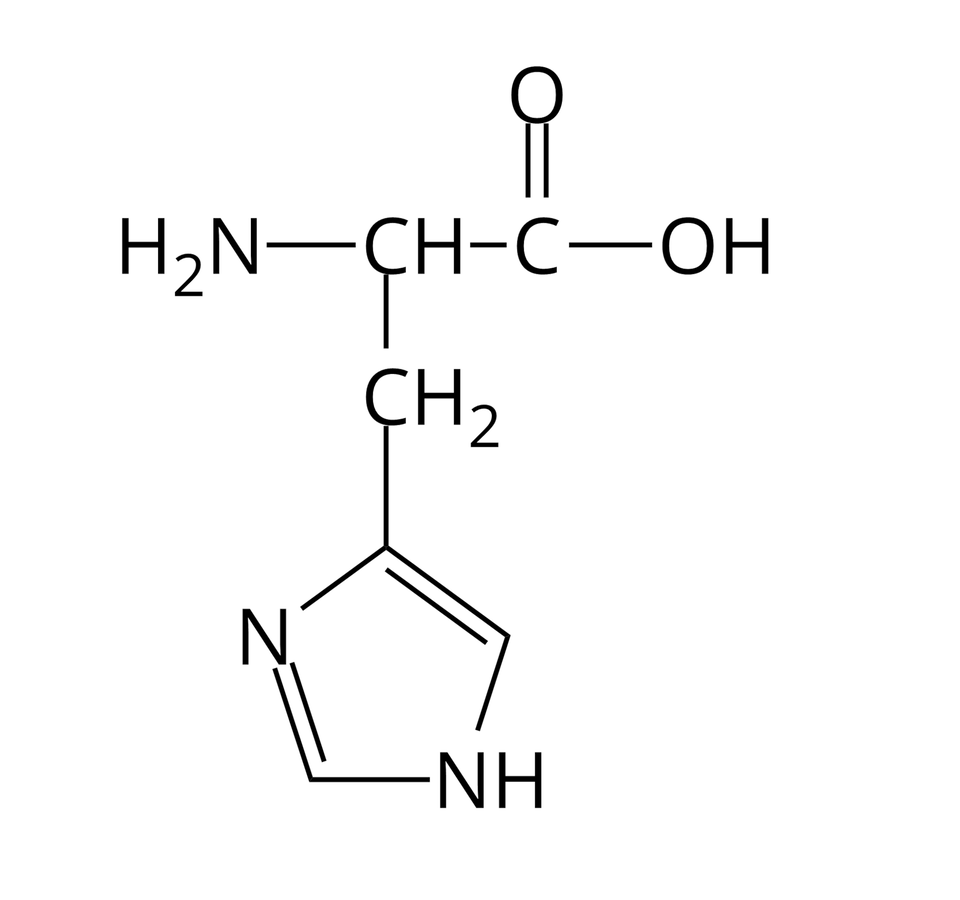 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Tyrozyna | 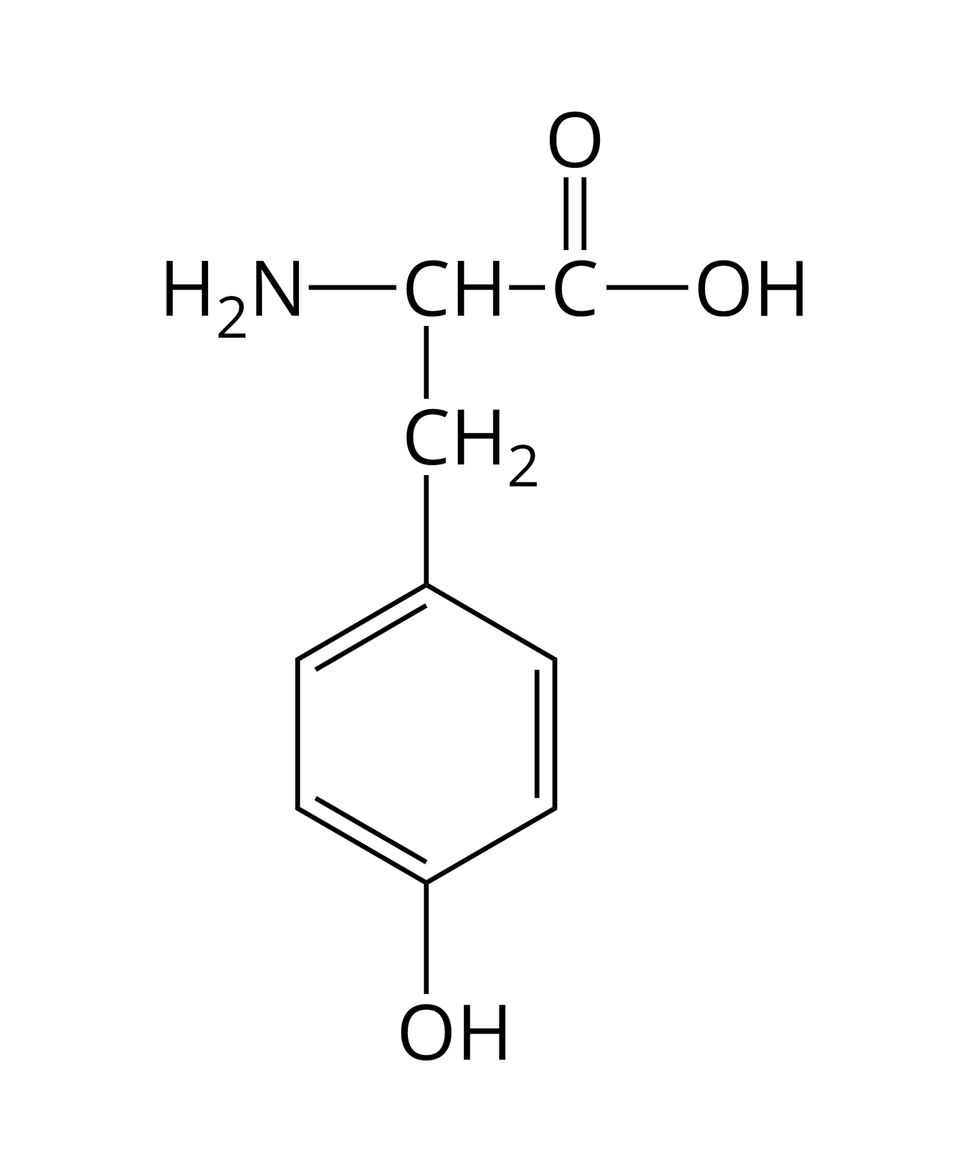 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Izoleucyna | 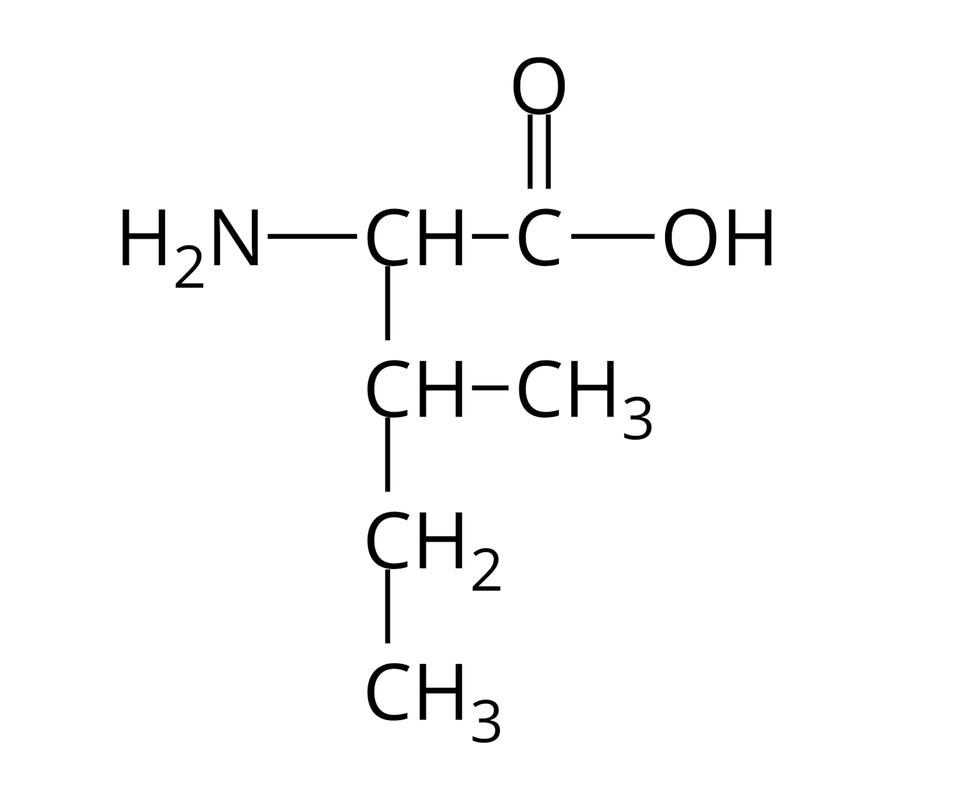 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | Walina | 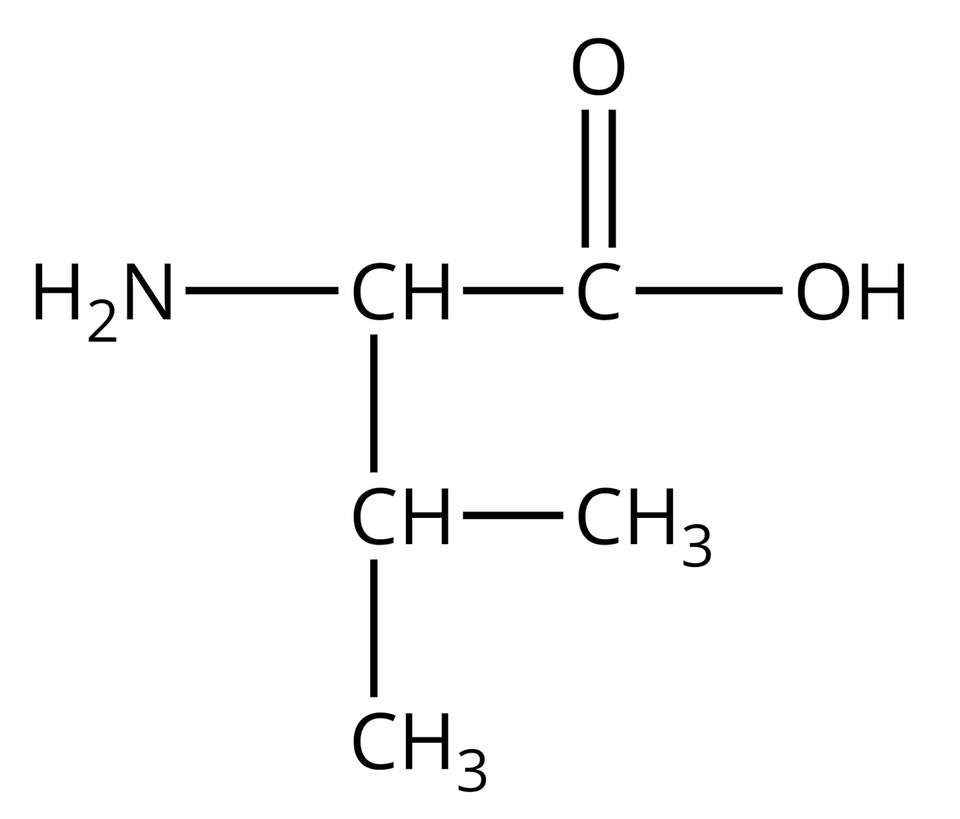 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Zwróć uwagę, że cząsteczki wszystkich aminokwasów białkowych, zamieszczonych w powyższej tabeli, zbudowane są z atomów węgla, wodoru, tlenu oraz azotu. Można zatem wnioskować, że cząsteczki białek również składają się z atomów tych samych pierwiastków chemicznych.
Pierwiastki chemiczne, które mogą wchodzić w skład białek, wymieniono na poniższym schemacie.
Na mapie myśli ukazano pierwiastki chemiczne budujące białka. Cząsteczki wszystkich białek zbudowane są z atomów: węgla, wodoru, azotu oraz tlenu. Cząsteczki niektórych białek zbudowane są również z atomów: siarki i fosforu oraz z jonów: żelaza(), magnezu i cynku.
W jaki sposób można potwierdzić obecność poszczególnych pierwiastków chemicznych w białku?
Aby potwierdzić obecność w białku węgla, wodoru i tlenu, wystarczy próbkę analizowanego białka (umieszczoną np. w probówce) ogrzewać ostrożnie w płomieniu palnika i obserwować zachodzące zmiany. W celu potwierdzenia obecności azotu w badanym białku, do wylotu probówki z ogrzewaną próbką można zbliżyć zwilżony wodą uniwersalny papierek wskaźnikowy. Jednym z produktów termicznego rozkładu białka jest bowiem amoniak, którego reakcję z wodą można opisać równaniem:
Powstające w tej reakcji aniony wodorotlenkowe powinny spowodować odpowiednią zmianę zabarwienia uniwersalnego papierka wskaźnikowego.
Jeśli w analizowanym białku zawarta jest również siarka, to podczas jego długotrwałego ogrzewania powinien być wyczuwalny charakterystyczny zapach, przypominający zapach palących się włosów. W przypadku wątpliwości, czy ten zapach faktycznie jest wyczuwalny, można do wylotu probówki z ogrzewaną próbką zbliżyć zwilżony wodą papierek ołowiowy (pasek bibuły, nasączony wodnym roztworem soli ołowiu()). Jeśli w badanym białku znajdowała się siarka, na skutek zachodzącej na powierzchni papierka ołowiowego reakcji opisanej równaniem:
papierek powinien przyjąć odpowiednie zabarwienie.
W jaki sposób można przedstawić budowę określonego białka?
Analizując budowę danego białka, nie możemy ograniczać się jedynie do podania jego składu pierwiastkowego. Budowa białek jest dużo bardziej złożona.
Do opisu budowy białek stosuje się cztery stopnie (poziomy) organizacji białka, czyli cztery struktury – pierwszorzędową, drugorzędową, trzeciorzędową i (dla niektórych białek) czwartorzędową. Opisano je krótko na poniższej grafice.
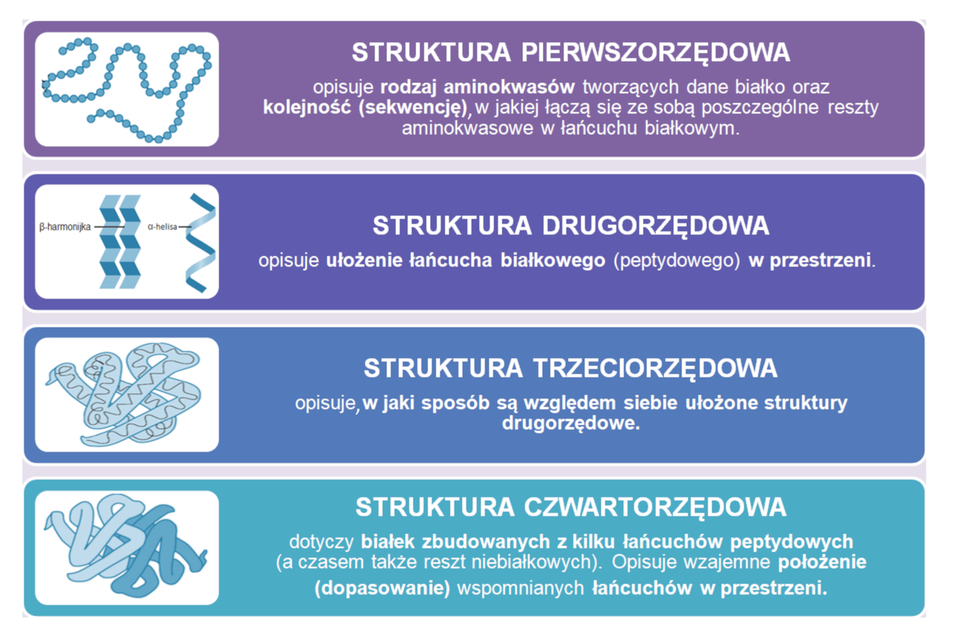
Ponieważ dokładne narysowanie budowy cząsteczki białka byłoby uciążliwe, choćby ze względu na jej rozmiary, budowę białek bardzo często przedstawia się, wykorzystując modele wstęgowe, tworzone w rozmaitych programach komputerowych.

Jak można wykryć białko?
Do identyfikacji i wykrywania białek stosuje się często dwie próby – próbę (reakcję) biuretowąpróbę (reakcję) biuretową oraz próbę (reakcję) ksantoproteinowąpróbę (reakcję) ksantoproteinową.
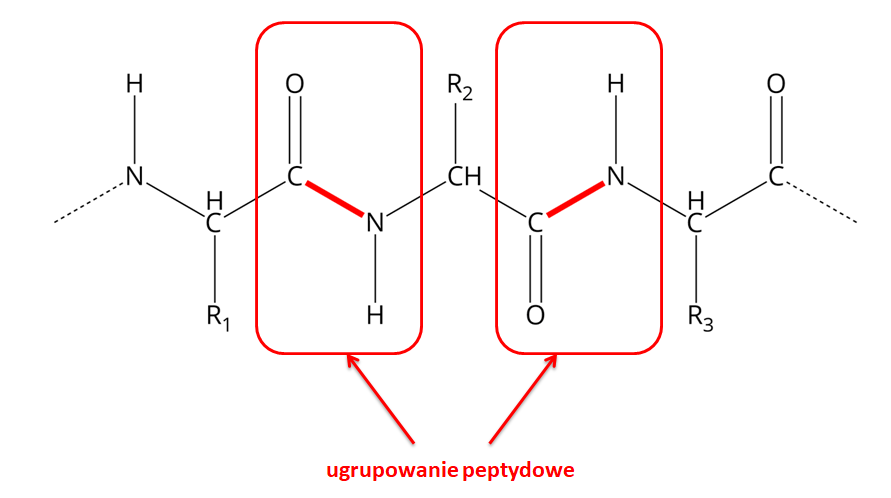
W próbie biuretowej, do identyfikacji białka wykorzystuje się zawiesinę świeżo strąconego wodorotlenku miedzi() () w środowisku zasadowym. O pozytywnym wyniku próby biuretowej świadczy pojawienie się fioletowego zabarwienia. W rzeczywistości próba ta nie pozwala na wykrycie samego białka, ale pozwala na potwierdzenie obecności w cząsteczce białka wiązań (ugrupowań) peptydowych.
Próba biuretowa
Pozytywny wynik próby biuretowej uzyskamy, poddając jej wszystkie te związki chemiczne, które w swojej strukturze posiadają co najmniej dwa wiązania peptydowe, położone bezpośrednio obok siebie lub przedzielone tylko jednym atomem węgla, tak jak w przypadku cząsteczek białek.
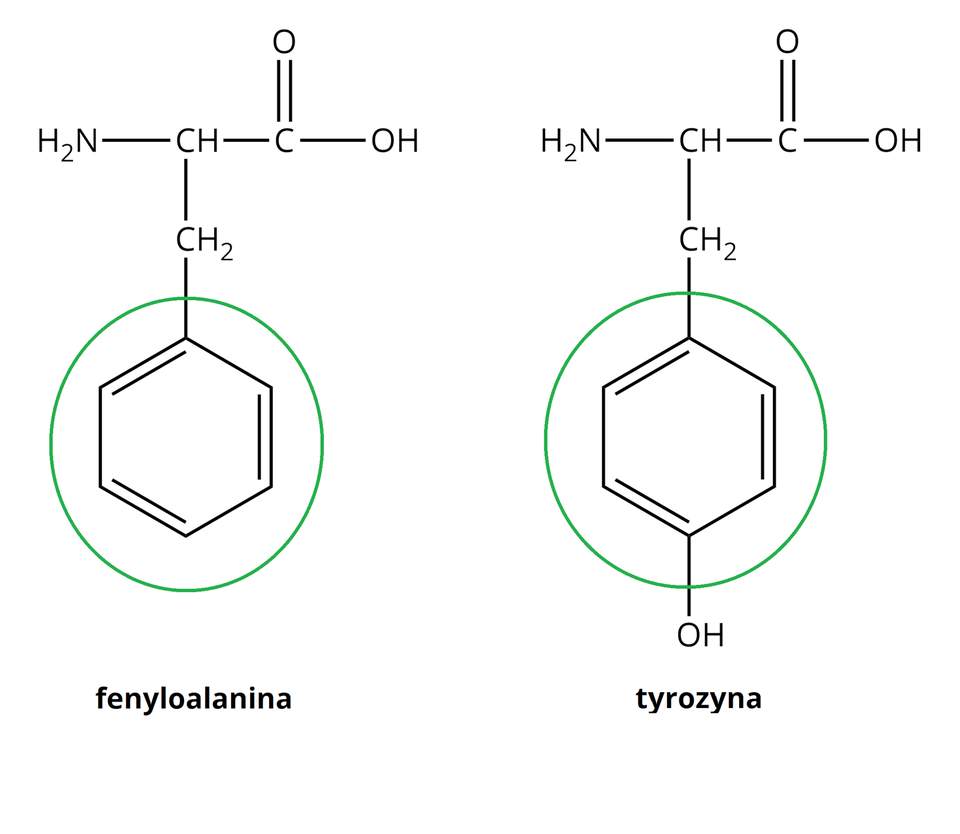
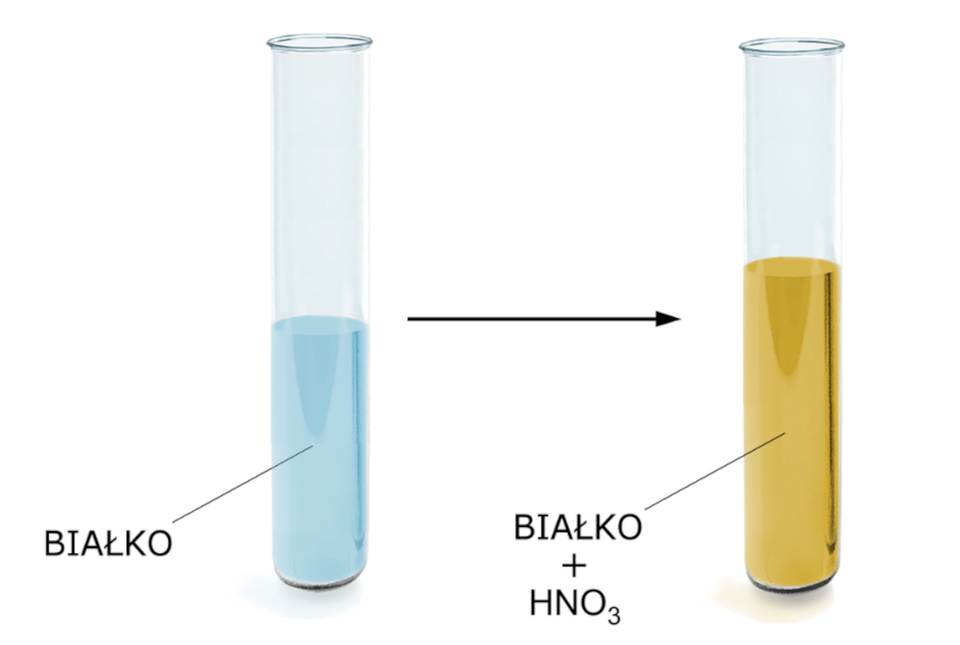
Odczynnikiem wykorzystywanym do wykrywania białek w próbie (reakcji) ksantoproteinowej jest stężony kwas azotowy() . O pozytywnym wyniku próby ksantoproteinowej świadczy pojawienie się żółtego zabarwienia. Podobnie jak próba biuretowa, również próba ksantoproteinowa nie pozwala na wykrycie samego białka. Pozytywny wynik uzyskamy wtedy, gdy w skład cząsteczki białka będą wchodziły aminokwasy, zawierające tak zwane ugrupowania aromatyczne.
Próba ksantoproteinowa.
Pomimo, że opisane próby – biuretowa i ksantoproteinowa – nie są charakterystyczne wyłącznie dla białek, są powszechnie stosowane do ich wykrywania.
Próba biuretowa nazywana jest też czasem odczynem Piotrowskiego, od nazwiska polskiego fizjologa Gustawa Piotrowskiego, który opisał ją jako pierwszy w Sama zaś nazwa „biuretowa” pochodzi od nazwy zwyczajowej najprostszego związku chemicznego, który daje pozytywny jej wynik. Związkiem tym jest biuret o wzorze:
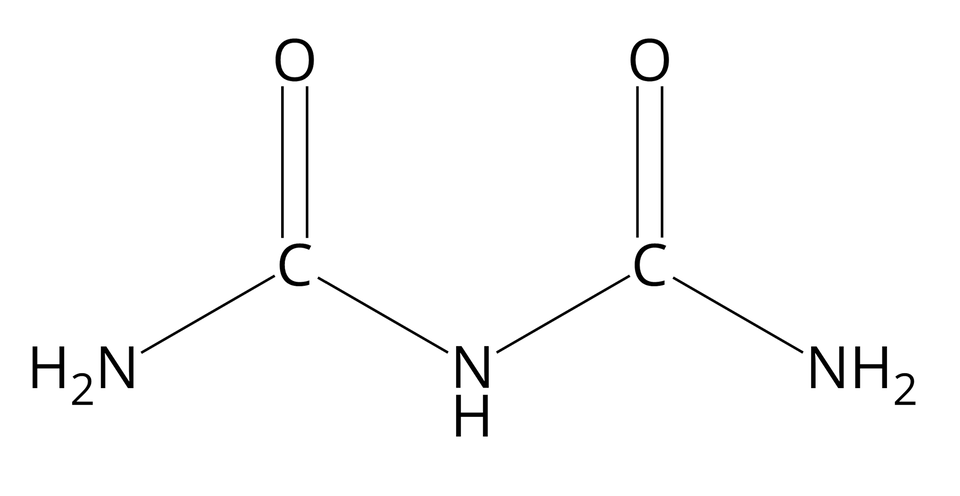
Jakie właściwości fizykochemiczne mają białka?
Białka są na ogół dobrze rozpuszczalne w wodzie. Po rozpuszczeniu w wodzie tworzą z nią roztwór koloidalny.
Charakterystycznym dla koloidów zjawiskiem fizycznym jest tak zwany efekt Tyndalla. Pokrótce zjawisko to polega na rozpraszaniu wiązki światła przechodzącej przez roztwór koloidalny na jego cząstkach. Dzięki temu obserwujemy charakterystyczny „stożek” (smugę).
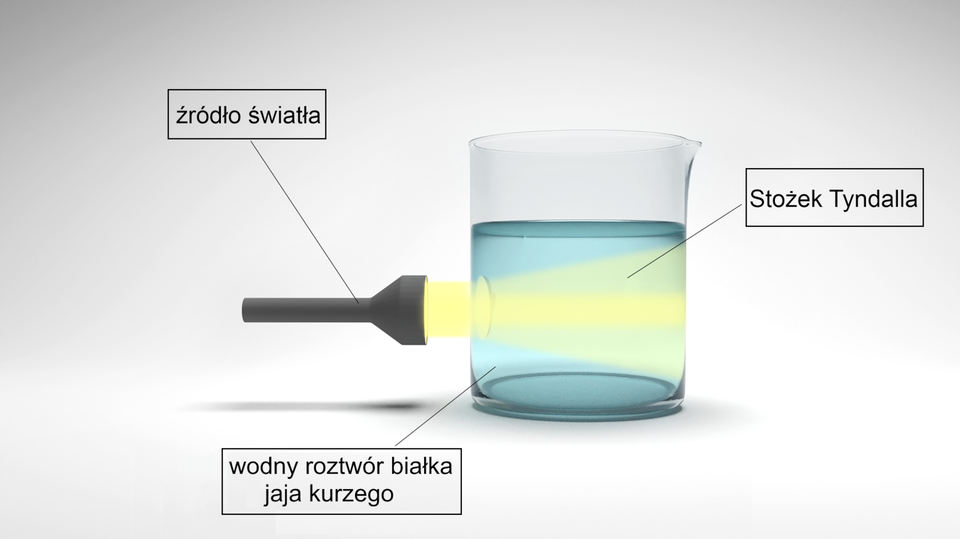
W wyniku działania niektórych czynników (zarówno fizycznych jak i chemicznych), białka ulegają tak zwanej koagulacjikoagulacji, która polega na wytrącaniu się białka z roztworu na skutek agregacji (łączenia się w większe grupy) cząsteczek białka.
W przypadku, gdy proces koagulacji nie narusza żadnej ze struktur białka, nazywamy go wysalaniemwysalaniem. Wysalanie jest procesem odwracalnym – wytrącony z roztworu osad białka można rozpuścić poprzez wprowadzenie do roztworu dodatkowej porcji wody. Proces wysalania białka (koagulacji odwracalnej) wywoływany jest między innymi przez sole metali lekkich (np. chlorek sodu).
Pod wpływem działania niektórych czynników (np. wysokiej temperatury lub soli metali ciężkich), białko ulega procesowi tak zwanej denaturacjidenaturacji. Procesu tego nie da się cofnąć (odwrócić), dlatego też nazywany jest on często koagulacją nieodwracalną. Na skutek denaturacji, zostają zniszczone przestrzenne struktury białka – czwartorzędowa (o ile białko takową posiada), trzeciorzędowa oraz drugorzędowa. To z kolei rzutuje na zmiany właściwości fizykochemicznych białka. Pierwszorzędowa struktura białka, a więc kolejność (sekwencja) aminokwasów w łańcuchu peptydowym, pozostaje nienaruszona.
Na poniższym schemacie wymieniono wybrane czynniki, które powodują koagulację białek.
Na mapie myśli ukazano wybrane czynniki powodujące koagulację białek, którą dzieli się na odwracalną i nieodwracalną. Koagulacja odwracalna zachodzi w wyniku wysalania. Nie narusza ona struktury przestrzennej białka, a jedynie niszczy otoczkę hydratacyjną (wodną) białka, która to może zostać odtworzona. Czynnikami wywołującymi proces wysalania są głównie sole metali lekkich, np. , i .
Koagulacja nieodwracalna zachodzi w wyniku denaturacji. Polega ona na niszczeniu struktury przestrzennej białka: czwarto–, trzecio– i drugorzędowej. Czynniki wywołujące proces denaturacji dzielimy na fizyczne i chemiczne. Czynniki fizyczne to ultradźwięki, podwyższona temperatura oraz promieniowanie: jonizujące, rentgenowskie, gamma i nadmierne promieniowanie UV. Czynniki chemiczne to stężone kwasy, np. , ; alkohole, np. etanol , metanol ; stężone zasady, np. wodne roztwory takie jak i ; jony metali ciężkich, np. jony miedzi() i jony rtęci() .
Procesy denaturacji białek uznawane są zazwyczaj za nieodwracalne. Okazuje się jednak, że w niektórych przypadkach, w odpowiednich warunkach, można odwrócić proces denaturacji. Przemiana taka nosi nazwę renaturacji. W wyniku renaturacji może dojść do odtworzenia się struktury drugo– i trzeciorzędowej białka. Jeśli białko przed procesem denaturacji posiadało strukturę czwartorzędową, nie ulegnie odtworzeniu. Musisz jednak wiedzieć, że proces renaturacji jest stosunkowo trudny do przeprowadzenia, a jeśli jest możliwy, to zachodzi bardzo powoli.
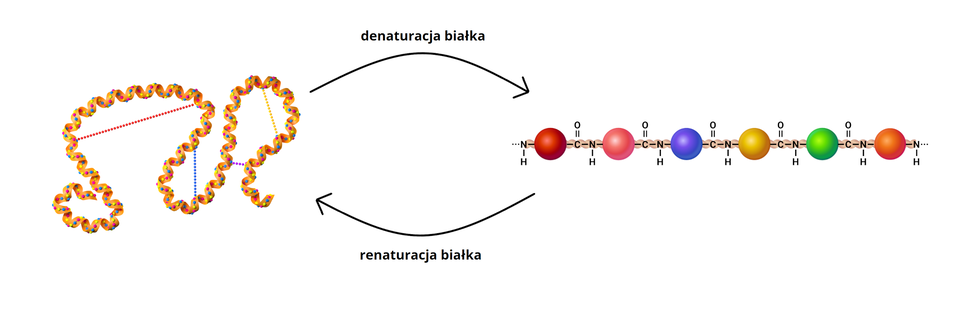
Wirtualne laboratorium
Przeprowadź eksperymenty w wirtualnym laboratorium chemicznym. Określ doświadczalnie skład pierwiastkowy białka jaja kurzego. Zbadaj wybrane właściwości fizykochemiczne białka – zwróć uwagę na procesy koagulacji białka. Na podstawie zdobytej wiedzy, zidentyfikuj białko w białku jaja kurzego oraz w mleku. Sprawdź doświadczalnie, czy w analizowanych próbkach znajduje się białko. Podczas wykonywania eksperymentów, uzupełnij dziennik laboratoryjny.
Zapoznaj się z opisem eksperymentów przeprowadzonych w wirtualnym laboratorium chemicznym. Pierwszy eksperyment polega na doświadczalnym określeniu składu pierwiastkowego białka jaja kurzego, a następny na zbadaniu wybranych właściwości fizykochemicznych białka, gdzie należy zwrócić szczególną uwagę na procesy koagulacji białka. Następny eksperyment polega na identyfikacji białka w białku jaja kurzego oraz w mleku. W ostatnim eksperymencie zostanie doświadczalnie sprawdzone, czy w analizowanych próbkach znajduje się białko. Zapoznaj się z przedstawionymi problemami badawczymi i odpowiadającymi im hipotezami, obserwacjami oraz wnioskami wyciągniętymi z eksperymentów.
Temat:
Analiza składu pierwiastkowego białek.
Problem badawczy
Jakie pierwiastki wchodzą w skład białek?
Hipoteza:
W skład białek wchodzą takie pierwiastki, jak: węgiel, wodór, tlen, azot oraz siarka.
Sprzęt laboratoryjny:
probówka – podłużne U‑kształtne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
drewniana łapa do probówek – rodzaj narzędzia wykorzystywanego w laboratorium do trzymania, na przykład kolb;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
pipeta – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
palnik – urządzenie techniczne umożliwiające podtrzymywanie płomienia spalanego gazu w kontrolowany sposób;
zapałki – drewniane patyczki nasączone substancją ułatwiającą spalanie i zakończone substancją ulegającą zapłonowi, która obecna jest w tak zwanej główce zapałki.
Odczynniki:
białko jaja kurzego;
uniwersalny papierek wskaźnikowy;
papierek ołowiowy;
woda destylowana.
Instrukcja:
Za pomocą pipety pobrano niewielką ilość białka jaja kurzego i wprowadzono ją do probówki.
Probówkę umieszczono w łapie i ogrzewano w płomieniu palnika stale nią wstrząsając.
Po chwili do wylotu probówki zbliżono zwilżone wodą destylowaną papierki: uniwersalny papierek wskaźnikowy i papierek ołowiowy.
Obserwacje:
W trakcie ogrzewania, białko jaja kurzego ścina się, stopniowo ciemnieje i ostatecznie pokrywa się czarnym nalotem. Na ściankach probówki pojawiają się krople bezbarwnej cieczy. Podczas ogrzewaniu białka wyczuwalny jest nieprzyjemny zapach, przypominający palące się włosy. Zbliżony do wylotu probówki zwilżony uniwersalny papierek wskaźnikowy zmienia zabarwienie z żółtego na zielone, a zwilżony wodą destylowaną papierek ołowiowy czernieje.
Wnioski:
Czarny nalot, który powstaje w wyniku ogrzewania, na białku jaja kurzego to węgiel. Powstająca na ściankach probówki ciecz to skroplona para wodna (cząsteczki pary wodnej utworzone są z atomów tlenu i wodoru). Zwilżony uniwersalny papierek wskaźnikowy zmienia zabarwienie w kontakcie z wydzielającym się amoniakiem (cząsteczki amoniaku zbudowane są z atomów azotu i wodoru). Czernienie papierka ołowiowego świadczy o obecności w białku siarki. Postawiona hipoteza jest zatem prawdziwa – białko zbudowane jest z węgla, tlenu, wodoru, azotu oraz siarki.
Temat:
Badanie właściwości fizykochemicznych białek.
Problem badawczy:
Które czynniki powodują odwracalną, a które nieodwracalną koagulację białka?
Hipoteza:
Koagulację odwracalną (wysalanie) białka powodują sole metali lekkich, a koagulację nieodwracalną (denaturację) – sole metali ciężkich, stężone kwasy i zasady, alkohol (etanol), detergenty oraz podwyższona temperatura. Sprzęt laboratoryjny:
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych,
probówki – podłużne U‑kształtne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
pipety – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Odczynniki:
białko jaja kurzego;
wodny roztwór siarczanu() miedzi();
stężony wodny roztwór wodorotlenku sodu;
stężony wodny roztwór chlorowodoru (kwas chlorowodorowy);
detergent;
etanol ();
(nasycony) wodny roztwór chlorku sodu;
woda destylowana;
gorąca woda.
Instrukcja:
W pierwszej części eksperymentu mając do dyspozycji gotowe roztwory chlorku oraz białka jaja kurzego, a także latarkę, przed przystąpieniem do głównego części doświadczenia sprawdź, w jaki sposób wiązka światła przechodzi przez wskazane roztwory. Wskaż różnice i nazwij zjawisko, które zaobserwowałeś.
W ośmiu probówkach umieszczono po około białka jaja kurzego (białko pobrano za pomocą pipety).
Do każdej z probówek wprowadzono około :
probówka – wodnego roztworu siarczanu() miedzi();
probówka – stężonego wodnego roztworu wodorotlenku sodu;
probówka – stężonego wodnego roztworu chlorowodoru;
probówka – detergentu;
probówka – etanolu;
probówka – (nasyconego) wodnego roztworu chlorku sodu;
probówka – gorącej wody;
probówka – wody destylowanej (o temperaturze pokojowej).
Wytrząśnięto zawartość każdej z probówek.
Do każdej z probówek dodano po około wody destylowanej.
Ponownie wytrząśnięto zawartość każdej z probówek.
Obserwacje:
Przepuszczona przez roztwór białka wiązka światła pochodząca z latarki utworzyła w objętości roztworu charakterystyczny kształt stożka, poszerzającego się w miarę oddalania od źródła światła. W przypadku roztworu chlorku sodu podany efekt nie został zaobserwowany.
Po wprowadzeniu wskazanych odczynników (punkt ) do probówek z białkiem jaja kurzego, w probówkach od do zaobserwowano wytrącanie się białego osadu (ścinanie się białka). W probówce nie zaobserwowano osadu. Po wprowadzeniu wody destylowanej do każdej z uzyskanych mieszanin zauważono, że biały osad zaniknął jedynie w probówce numer . W probówce numer w dalszym ciągu nie zaobserwowano zmian świadczących o przebiegu reakcji chemicznej.
Wnioski:
W wyniku przepuszczenia przez roztwór białka, który to jest roztworem koloidalnym, na skutek rozpraszania promieniowania na cząstkach koloidu powstaje charakterystyczny stożek. Zjawisko to to efekt Tyndalla.
Obserwowane w probówkach od do wytrącanie się osadu to proces koagulacji białka. W przypadku nasyconego wodnego roztworu chlorku sodu, koagulacja ta okazała się być odwracalna. W przypadku pozostałych odczynników (użytych we wskazanych produktach) nie zaobserwowano zaniku osadu – zatem obserwowana uprzednio koagulacja była nieodwracalna. Woda destylowana (w temperaturze pokojowej) nie spowodowała koagulacji białka. Postawiona hipoteza jest zatem prawdziwa – sole metali lekkich powodują koagulację odwracalną a koagulacja nieodwracalna może mieć miejsce pod wpływem takich czynników, jak: sole metali ciężkich, stężone kwasy i zasady, alkohol (etanol), detergenty oraz podwyższona temperatura.
Temat:
Identyfikacja białek.
Problem badawczy:
W jaki sposób można zidentyfikować białko?
Hipoteza:
Białko można zidentyfikować przeprowadzając reakcję (próbę) biuretową oraz reakcję (próbę) ksantoproteinową.
Sprzęt laboratoryjny:
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
trzy probówki – podłużne U‑kształtne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
pipety – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
statyw na probówki – - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Odczynniki:
białko jaja kurzego;
wodny roztwór siarczanu() miedzi();
wodny roztwór wodorotlenku sodu;
stężony kwas azotowy();
woda destylowana;
gorąca woda.
Instrukcja:
W dwóch probówkach umieszczono (za pomocą pipety) po około białka jaja kurzego.
Do trzeciej probówki wlano około wodnego roztworu siarczanu() miedzi() i dodano około zasady sodowej.
Uzyskaną w punkcie mieszaninę przelano do jednej z probówek z białkiem jaja kurzego. Wytrząśnięto zawartość probówki.
Do drugiej z probówek z białkiem jaja kurzego wprowadzno (za pomocą pipety) około stężonego kwasu azotowego(V). Wytrząśni zawartość probówki. Ogrzej zawartość probówki w łaźni wodnej, a następnie dodaj roztwór NaOH
Obserwacje:
Po wprowadzeniu wodnego roztworu wodorotlenku sodu do wodnego roztworu siarczanu() miedzi(), zaobserwowano wytrącanie się niebieskiego galaretowatego osadu. Po przelaniu uzyskanej mieszaniny do probówki zawierającej białko jaja kurzego, wspomniany osad roztworzył się, a w probówce pozostał fioletowy roztwór. Po wprowadzeniu stężonego kwasu azotowego() do białka jaja kurzego i ogrzaniu, zaobserwowano zmianę zabarwienia roztworu na żółty. Po dodaniu wodorotlenku sodu, nastąpiła zmiana barwy na pomarańczowo
Wnioski:
Analiza poczynionych obserwacji pozwala na stwierdzenie, że na podstawie przeprowadzonych prób można zidentyfikować białko. Próba ze świeżo strąconym wodorotlenkiem miedzi() to próba biuretowa. Pozytywny wynik tej próby świadczy o obecności w badanej substancji ugrupowań (wiązań) peptydowych. Próba ze stężonym kwasem azotowym() to próba (reakcja) ksantoproteinowa. Pozytywny jej wynik świadczy o obecności w badanej substancji ugrupowań peptydowych.
Temat:
Wykrywanie białek w badanych próbkach.
Problem badawczy:
Czy w analizowanych produktach znajduje się białko?
Hipoteza:
W każdym z analizowanych produktów znajduje się białko.
Sprzęt laboratoryjny:
pięć szkiełek zegarkowych – szklane naczynie laboratoryjne o zaokrąglonym kształcie podstawy. Służy do odważania niewielkich ilości substancji chemicznych;
pipety – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki:
stężony kwas azotowy();
niewielki kawałek twarogu;
plaster wędliny;
ptasie pióro;
kawałek materiału z jedwabiu;
kawałek materiału dżinsowego.
Instrukcja:
Każdą z badanych próbek umieszczono na osobnym szkiełku zegarkowym.
Na każdą z próbek naniesiono (za pomocą pipety) po kilka kropli stężonego kwasu azotowego().
Obserwacje:
Na każdej z badanych próbek, po naniesieniu na nie kwasu azotowego(), zaobserwowano pojawienie się żółtego zabarwienia.
Wnioski:
Odnotowane obserwacje pozwalają na stwierdzenie, że w każdym z analizowanych produktów znajduje się białko. (Przeprowadzona próba to reakcja (próba) ksantoproteinowa).
Zadaniem ucznia było zidentyfikowanie otrzymanej od nauczyciela próbki, która wyglądem przypominała białko jaja kurzego. Jedną z pierwszych prób, jakie przeprowadził uczeń było ogrzewanie próbki analizowanej substancji w płomieniu palnika. W czasie ogrzewania uczeń zaobserwował, że próbka pokryła się czarnym nalotem, a na ściankach probówki, w której ogrzewał badaną substancję, pojawiły się krople bezbarwnej cieczy. Zwilżony wodą uniwersalny papierek wskaźnikowy zbliżony do probówki z ogrzewaną próbką nie zmienił swojego zabarwienia. Zwilżony wodą papierek ołowiowy zbliżony do probówki z ogrzewaną próbką pozostał biały.
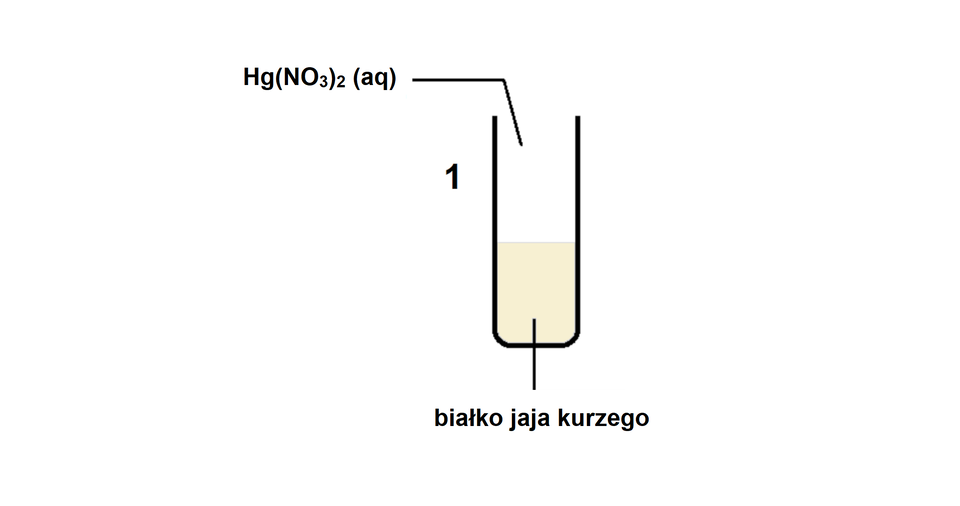
Uczeń przeprowadził doświadczenie zilustrowane na poniższym schemacie:
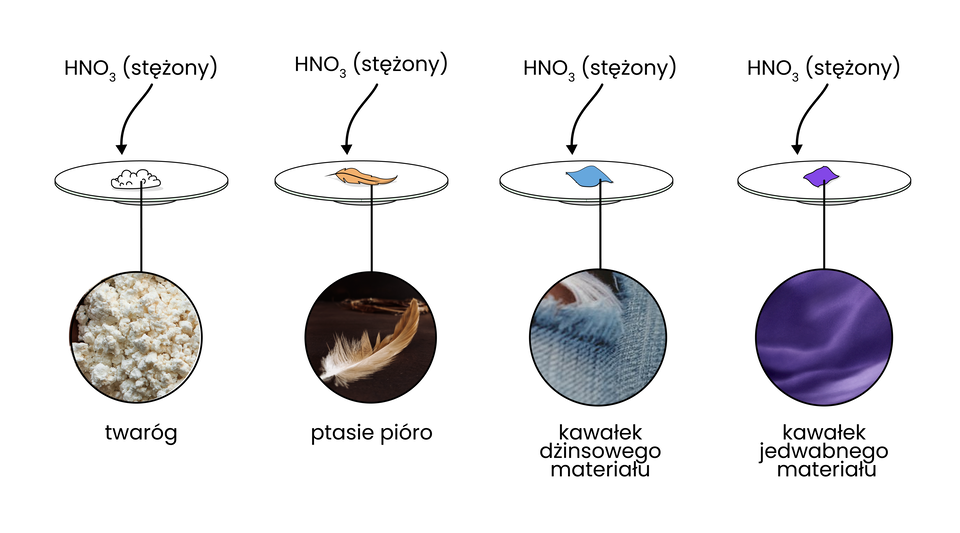
Uczeń przeprowadził doświadczenie polegające na dodaniu stężonego do czterech probówek zawierających:
probówka – twaróg;
probówka – ptasie pióro;
probówka – kawałek dżinsowego materiału;
probówka – kawałek jedwabnego materiału.
Słownik
wielkocząsteczkowe związki chemiczne, zbudowane z reszt powyżej aminokwasów połączonych wiązaniami peptydowymi; w skład białek wchodzą głównie takie pierwiastki, jak: węgiel, wodór, tlen i azot
reakcja wykorzystywana do wykrywania wiązań peptydowych w białkach i w związku z tym do wykrywania białek; zachodzi pod wpływem wodorotlenku miedzi(); pozytywny wynik tej reakcji (świadczący o obecności wiązań (ugrupowań) peptydowych) to pojawienie się fioletowego zabarwienia
reakcja wykorzystywana do wykrywania obecności niektórych białek; zachodzi pod wpływem stężonego kwasu azotowego(); pozytywny wynik tej reakcji (świadczący o obecności białka, a ściślej o obecności w białku charakterystycznych ugrupowań) to pojawienie się żółtego zabarwienia
(łac. coagulatio „ścinanie się, krzepnięcie”) proces ścinania się białka będącego koloidem; polega na zlepianiu się cząstek białka w większe skupiska (agregaty) co obserwuje się jako wytrącanie osadu
odwracalny proces koagulacji białka; polega w uproszczeniu na niszczeniu otoczki wodnej (hydratacyjnej) cząsteczek białka, która może zostać odbudowano poprzez wprowadzenie do układu nadmiaru wody; zachodzi pod wpływem niektórych soli, głównie soli metali lekkich, np. chlorku sodu
najczęściej nieodwracalny proces naruszenia struktury przestrzennej białka (koagulacja nieodwracalna); czynnikami powodującymi denaturację białka są między innymi temperatura, promieniowanie UV i czynniki mechaniczne, jak np. gwałtowne wytrząsanie (zaliczane do czynników fizycznych) oraz sole metali ciężkich, kwasy, zasady i etanol (zaliczane do czynników chemicznych)
Ćwiczenia
Uczeń przeprowadził doświadczenie, zilustrowane na poniższym schemacie.
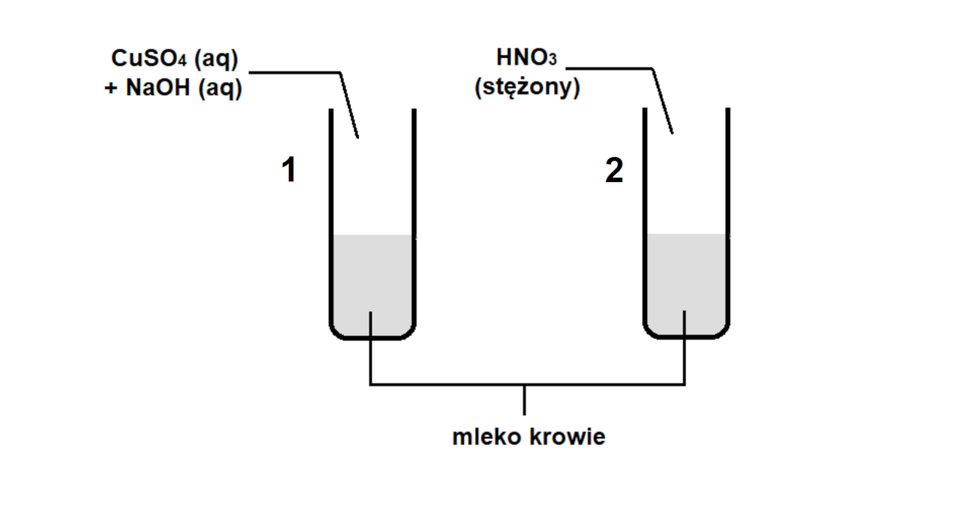
Zaproponuj problem badawczy i hipotezę do zilustrowanego powyżej doświadczenia. Napisz, jakie obserwacje powinien odnotować uczeń podczas jego wykonywania. Następnie sformułuj odpowiedni wniosek.
Przeprowadzono doświadczenie polegające na dodaniu do dwóch probówek, które zawierają mleko krowie, kolejno:
probówka – ;
probówka – .
Poniżej przedstawiono uproszczony wzór fragmentu cząsteczki pewnego białka. Określ, które z zaznaczonych na wzorze ugrupowań można wykryć, przeprowadzając próbę biuretową, a które za pomocą próby ksantoproteinowej. Do nazwy każdej z prób dopasuj odpowiadający jej numer (bądź numery) ugrupowania.
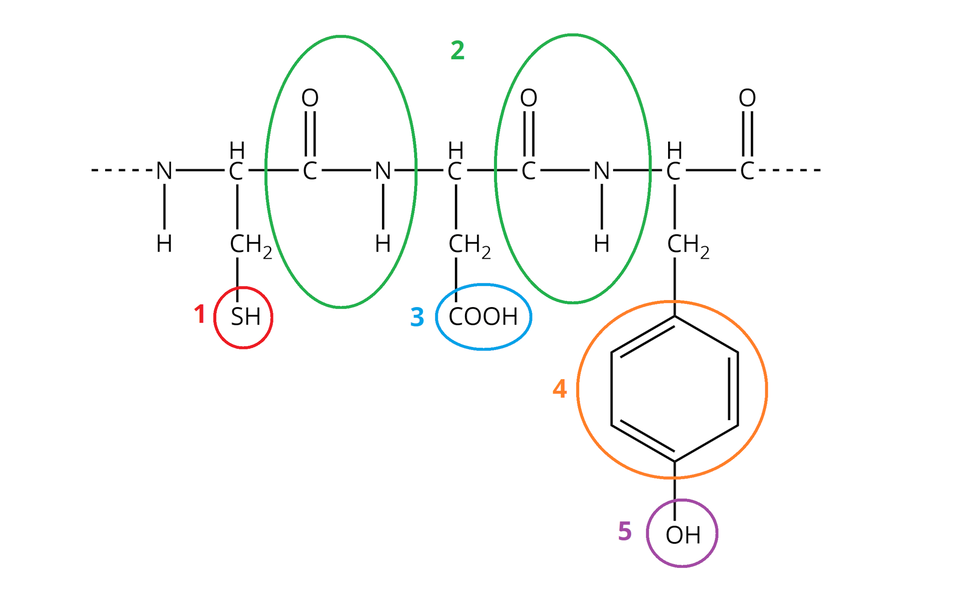
Próba (reakcja) ksantoproteinowa – ugrupowanie nr 1. jeden, 2. trzy, 3. dwa, 4. cztery, 5. pięć.
Napisz, jakie ugrupowanie w strukturze białka można wykryć za pomocą reakcji biuretowej, a jakie za pomocą reakcji ksantoproteinowej.
Bibliografia
Danikiewicz D., Chemia. Związki organiczne, Warszawa 2016, wyd. 2.
Encyklopedia PWN
Kołodziejczyk A., Naturalne związki organiczne, Warszawa 2004, s. 174‑228.
Mastalerz P., Chemia organiczna, Wrocław 2000, s. 632‑633.
Szczypiński R., Projektowanie doświadczeń chemicznych, Warszawa 2019.