Właściwości fizykochemiczne a położenie pierwiastka w układzie okresowym
Znajomość położenia pierwiastka w układzie okresowym często pozwala przewidzieć jego właściwości chemiczne i fizyczne. Wszystko za sprawą tego, że pewne z nich zmieniają się w określony sposób w grupach i okresach. Można w ten sposób w przybliżeniu okreslić właściwości pierwiastka będącego w tej samej grupie, co pierwiastek, którego właściwości znamy. Określając, że dana właściwość rośnie w grupie, mamy na myśli, że rośnie wraz ze wzrostem liczby atomowej pierwiastków stanowiących daną grupę.
Charakter metaliczny
Charakter metaliczny pierwiastków polega na łatwym oddawaniu elektronu lub elektronów walencyjnych. Proces ten zachodzi łatwo, jeśli wymaga dostarczenia niewielkiej energii, a więc dotyczy pierwiastków charakteryzujących się niską wartością energii jonizacji. Właściwości metaliczne pierwiastków bloku wynikają z faktu, że posiadają one jeden lub dwa elektrony walencyjne, czyli niewiele do odłączenia. Im dalej od jądra atomowego znajduje się elektron walencyjny, tym łatwiej go oderwać, ponieważ działają na niego słabsze siły przyciągania. Właściwości metaliczne pierwiastków bloku są związane właśnie z dużą odległością elektronów walencyjnych od jądra atomowego, w porównaniu do niemetali będących również w bloku . Charakter metaliczny, a więc również aktywność metali, rośnie dla kolejnych pierwiastków danej grupy układu okresowego.
Charakter metaliczny pierwiastków wiąże się ze zdolnością oddawania elektronu lub elektronów walencyjnych. Proces ten zachodzi łatwo, jeśli wymaga dostarczenia niewielkiej energii, a więc dotyczy pierwiastków charakteryzujących się niską wartością energii jonizacji. Jak już ustaliliśmy wcześniej, energia jonizacji (pomijając wyjątki) rośnie w okresie (biorąc pod uwagę tylko gtupy główne), a zatem charakter metaliczny maleje w okresie. Najsilniejsze właściwości metaliczne posiadają pierwiastki bloku s, nieco słabsze pierwiastki bloku d, natomiast najlżejsze pierwiastki bloku p to głównie niemetale.
Charakter niemetaliczny
Charakter niemetaliczny pierwiastków polega na łatwym przyłączaniu elektronów do powłoki walencyjnej. Proces ten zachodzi łatwo, jeśli w jego wyniku wydziela się dużo energii, a więc dotyczy pierwiastków charakteryzujących się wysoką wartością powinowactwa elektronowego. Właściwości niemetaliczne są tym silniejsze, im powłoka walencyjna jest bliżej jądra atomowego. Zatem charakter niemetaliczny i aktywność niemetali maleją w dół grupy układu okresowego.
Charakter niemetaliczny pierwiastków polega na przyłączaniu elektronów do powłoki walencyjnej. Proces ten zachodzi łatwo, jeśli w jego wyniku wydziela się dużo energii, a więc dotyczy pierwiastków charakteryzujących się wysoką wartością powinowactwa elektronowego. Najwyższe wartości powinowactwa elektronowego posiadają pierwiastki grupy. Charakter niemetaliczny rośnie zatem w stronę prawą w okresie, a więc ze wzrostem liczby atomowej.
Jak zmieniają się właściwości fizyczne i chemiczne pierwiastków w obrębie grup i okresów układu okresowego? Zapoznaj się z treścią poniższych filmów i wykorzystaj zdobytą z nich wiedzę do rozwiązania ćwiczeń.

Film dostępny pod adresem /preview/resource/R1MAiaCq2AMvw
Film nawiązujący do treści materiału dotyczącego zmian właściwości pierwiastków w obrębie grup układu okresowego.

Film dostępny pod adresem /preview/resource/R1X3G1CUaBM0Z
Film nawiązujący do treści materiału dotyczącego zmian właściwości pierwiastków w obrębie okresów układu okresowego.
Uwzględniając struktury elektronowe atomów, odpowiedz, dlaczego energia jonizacji magnezu jest wyższa od energii jonizacji glinu.
Połącz w pary pierwiastki z odpowiadającymi im wartościami promieni atomowych.

Uzupełnij poniższe zdania dotyczące charakteru metalicznego. Wstaw odpowiednie słowa, wybierając z poniższych.
Uszereguj metale: , , według:
Poniżej przedstawiono fragment układu okresowego pierwiastków z zaznaczonymi wartościami elektroujemności wg skali Paulinga, przedstawiający atomy znajdujące się w 2. okresie. Wstaw strzałki, których groty będą przedstawiały w prawidłowym kierunku wzrost danej właściwości fizycznej.
Zaznacz poprawne stwierdzenia.
Odpowiedz na pytanie. Dlaczego wraz ze wzrostem liczby atomowej reaktywność metali w okresie maleje?
Pierwsza energia jonizacji atomu węgla jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą od pierwszej energii jonizacji atomu krzemu, ponieważ im mniejszy promień atomowy, tym energia jonizacji jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą. Atom selenu posiada 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą wartość energii jonizacji od atomu siarki, ponieważ im większy promień atomowy, tym wartość energii jonizacji jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą.
Poniżej przedstawiono fragment układu okresowego pierwiastków.
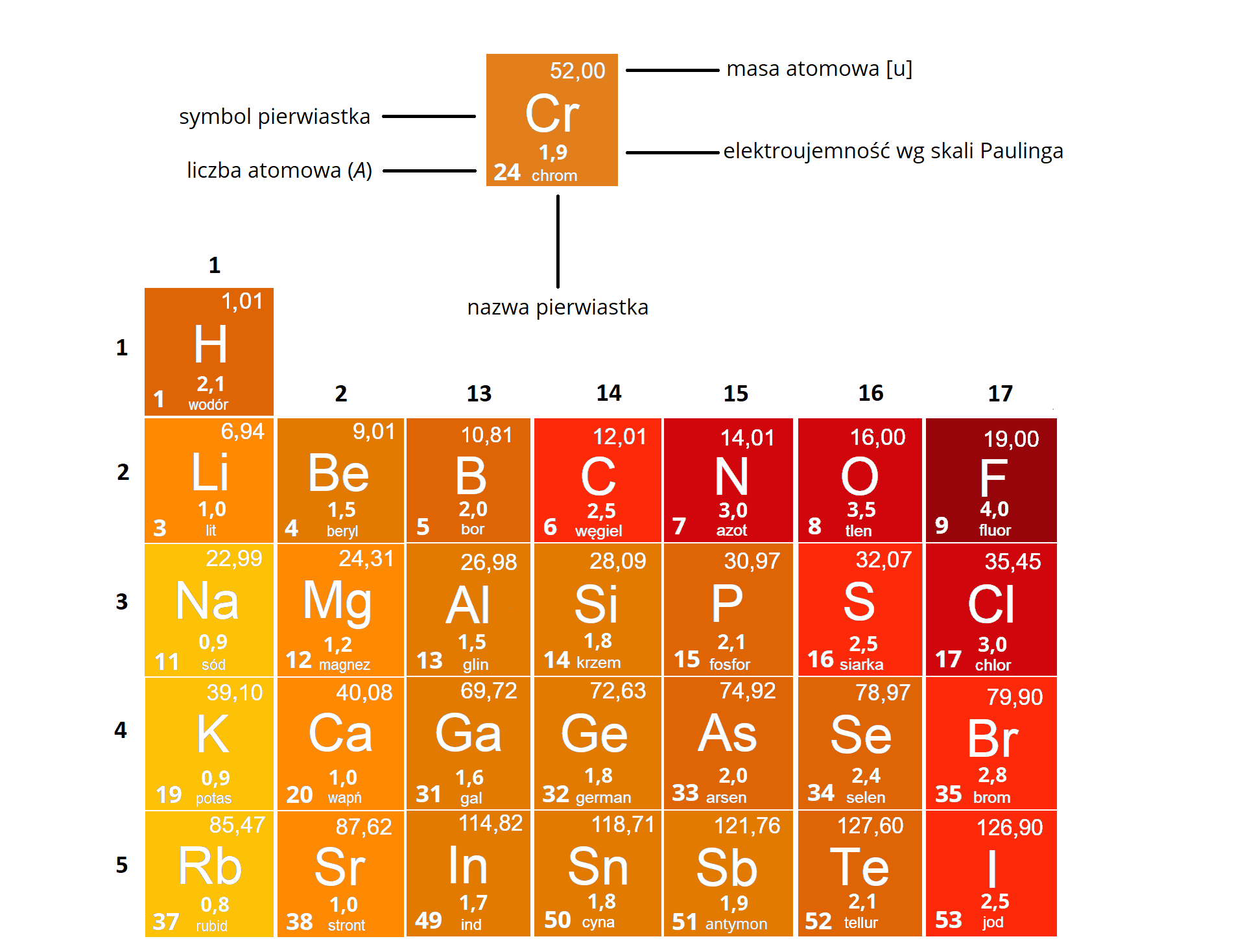
Spośród pierwiastków widocznych na załączonym fragmencie układu okresowego wybierz te, które spełniają wymienione poniżej właściwości. W puste pola wpisz symbole pierwiastków.
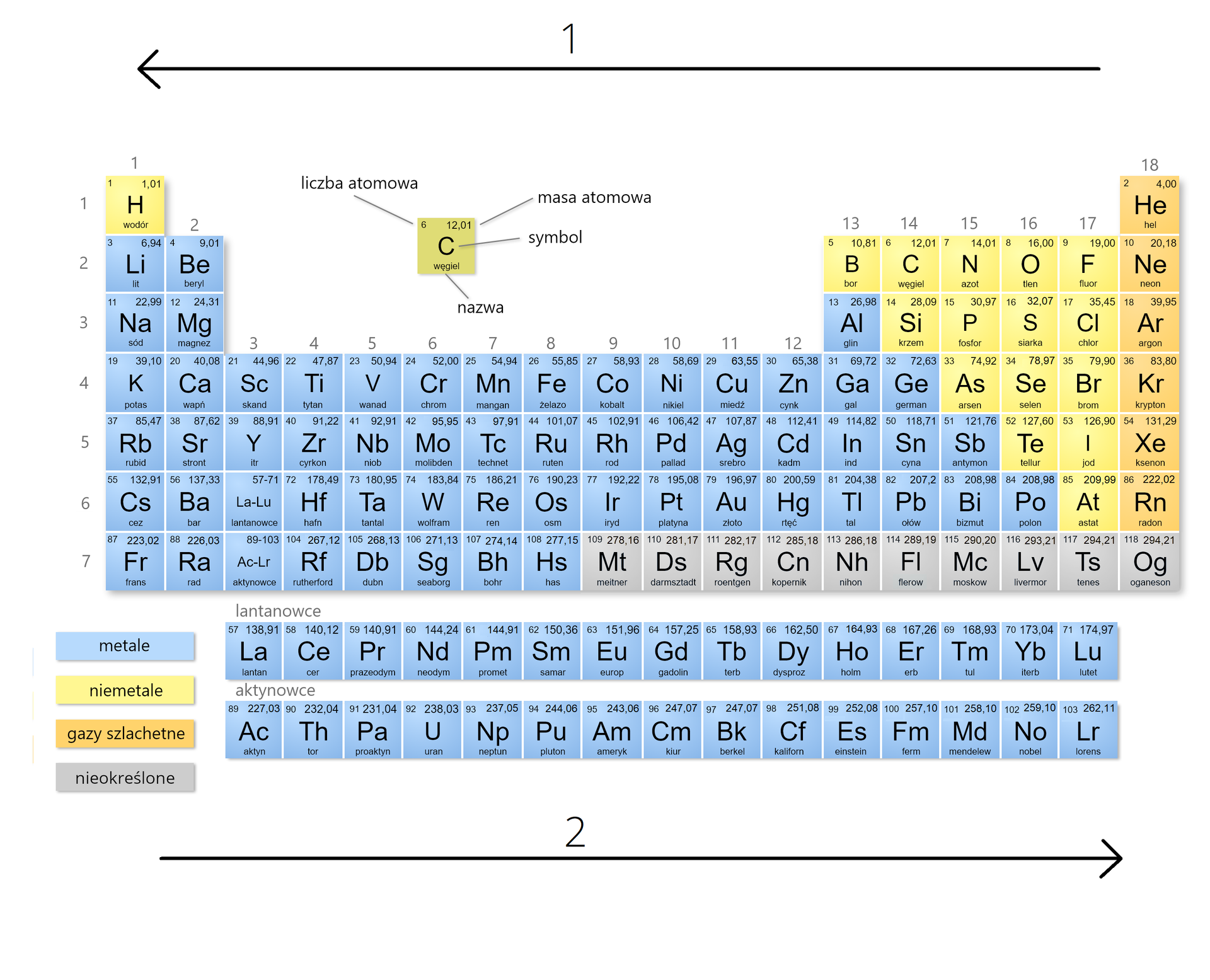
Strzałki na rysunku przedstawiają zmiany właściwości pierwiastków na tle układu okresowego. Na podstawie rysunku uzupełnij poniższą tabelę dotyczącą zmiany niektórych właściwości pierwiastków. W rozważaniach należy wziać pod uwagę tylko pierwiastki grup głównych, 1., 2. i 13.-17.
Zapoznaj się z opisem rysunku. Strzałki przedstawiają zmiany właściwości pierwiastków na tle układu okresowego. Na podstawie rysunku uzupełnij poniższą tabelę dotyczącą zmiany niektórych właściwości pierwiastków. W rozważaniach należy wziać pod uwagę tylko pierwiastki grup głównych , , od do .
Pierwsza energia jonizacji atomu węgla jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą od pierwszej energii jonizacji atomu krzemu, ponieważ im mniejszy promień atomowy, tym energia jonizacji jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą. Atom selenu posiada 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą wartość energii jonizacji od atomu siarki, ponieważ im większy promień atomowy, tym wartość energii jonizacji jest 1. maleje, 2. większa, 3. mniejszą, 4. mniejszy, 5. większa, 6. większy, 7. zwiększa się, 8. mniejszy, 9. mniejsza, 10. większa, 11. mniejsza, 12. mniejsza, 13. mniejszy, 14. mniejszy, 15. większy, 16. wzrasta, 17. większy, 18. zmniejsza się, 19. większy, 20. większą.
Strzałki na rysunku przedstawiają kierunek wzrostu właściwości pierwiastków i grupy układu okresowego. Na podstawie rysunku zaznacz odpowiednie komórki tabeli dotyczącej zmian niektórych właściwości pierwiastków.
Strzałki na rysunku przedstawiają kierunek wzrostu właściwości pierwiastków i grupy układu okresowego. Na podstawie opisu rysunku zaznacz odpowiednie komórki tabeli dotyczącej zmian niektórych właściwości pierwiastków.

Sporządź mapę pojęciową, która podsumuje jak zmieniają się różne właściwości pierwiastków w układzie okresowym. Przenalizuj poniższy układ okresowy porównując właściwości poszczególnych pierwiastków w obrębie grup i okresów i przedstaw wynik analizy za pomocą mapy pojęciowej
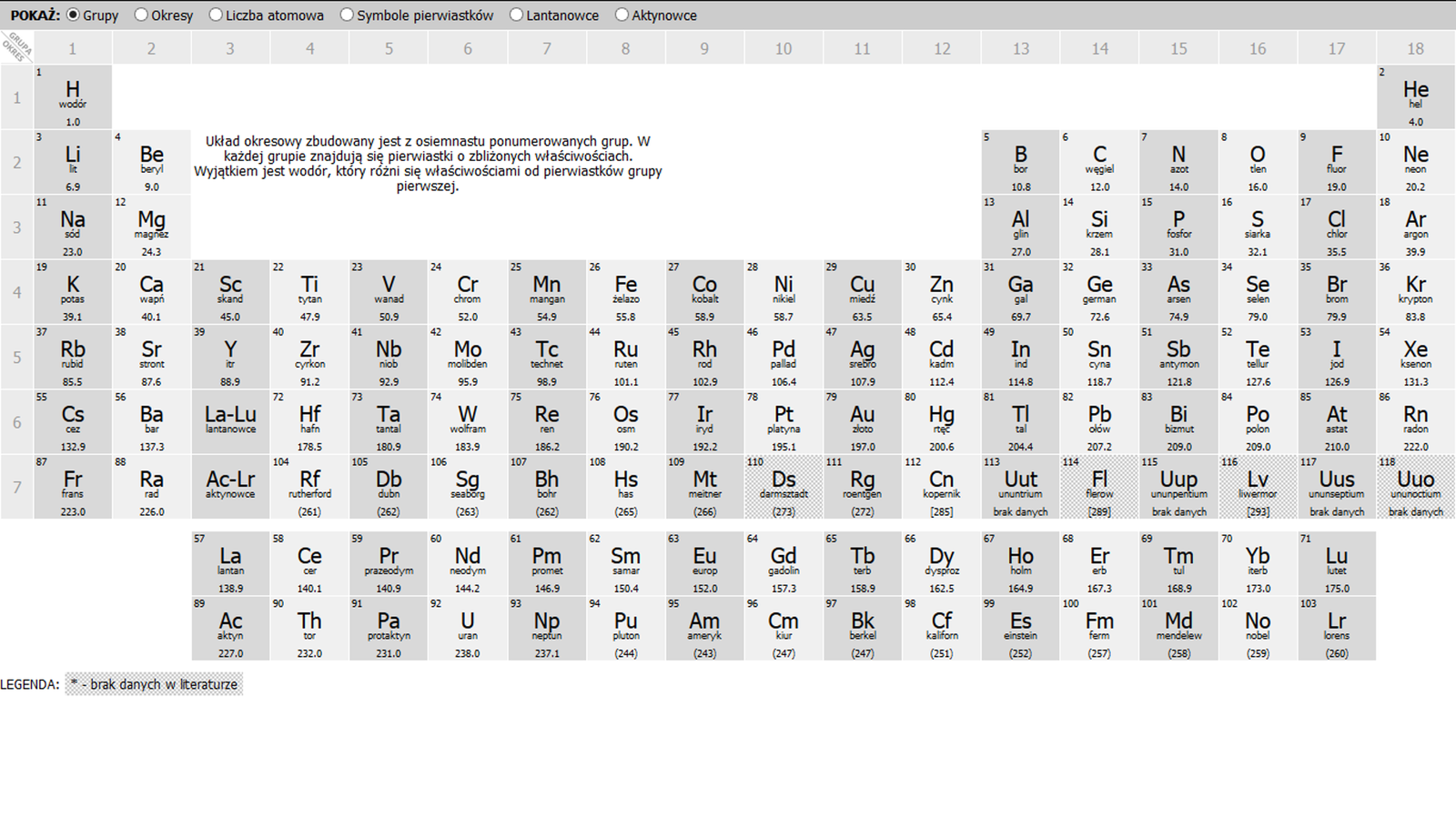
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1UQODR6T