Choroby genetyczne człowieka
Przyczyną przewlekłej białaczki szpikowej jest wymiana (translokacja) fragmentów długich ramion chromosomu 9 i chromosomu 22. W jej wyniku chromosom 22 występuje w skróconej postaci – nazywany jest chromosomem Philadelphia.
Zespoły aberracji chromosomowych u człowieka
Wymienisz choroby człowieka wywołane przez aberracje chromosomowe liczbowe i strukturalne.
Określisz na podstawie analizy rodowodu podłoże genetyczne chorób człowieka: zespół Klinefeltera, zespół Turnera, zespół Downa.
Trwałość gatunku oraz prawidłowe funkcjonowanie organizmu zależą od integralności materiału genetycznego – zarówno pod względem liczby, jak i struktury chromosomów. Choć mechanizmy podziałów komórkowych (mitozy i mejozy) cechują się niezwykłą precyzją, sporadyczne błędy w ich przebiegu prowadzą do powstania aberacji chromosomowych. Skutki takich zmian bywają drastyczne: od obumarcia zarodka na wczesnym etapie rozwoju, po wystąpienie złożonych zespołów wad wrodzonych u noworodków.
Aberracje chromosomowe liczbowe
Zmiany w liczbie chromosomów zazwyczaj prowadzą do poważnych zaburzeń rozwojowych: aneuploidii i poliploidii.
Poliploidia, polegająca na zwielokrotnieniu całego zestawu chromosomów (np. triploidia), jest dla człowieka wadą letalną – zarodki nią obciążone obumierają na etapie życia prenatalnego. Inaczej jest w przypadku aneuploidii, czyli zmiany liczby tylko pojedynczych chromosomów. Choć wiele z nich również kończy się poronieniem, niektóre pozwalają na urodzenie dziecka i jego dalszy rozwój. Do najczęściej spotykanych aneuploidii należą trisomie (obecność dodatkowego chromosomu w parze) oraz monosomie (brak jednego z chromosomów homologicznych
Aneuploidalność jest na ogół skutkiem nondysjunkcji - zaburzenia polegającego na nieprawidłowym rozejściu się chromosomów w anafazie podziału mejotycznego.
Aneuploidie mogą dotyczyć zarówno chromosomów płci jak i autosomów. Przykładami takich zaburzeń są:
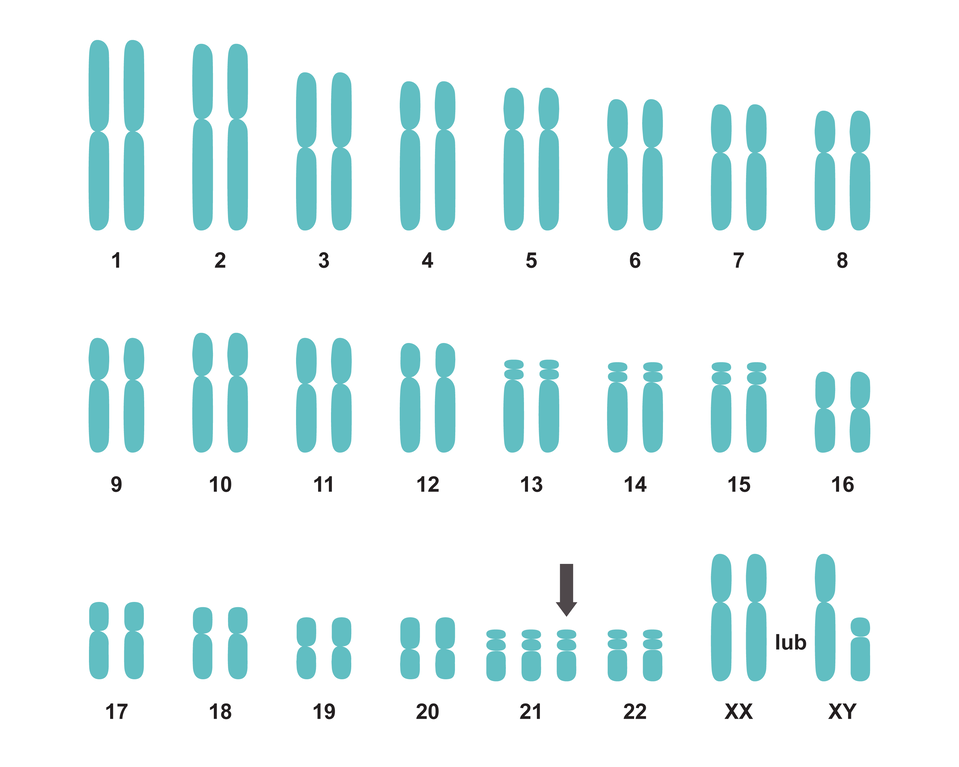
zespół Downa - aneuploidia autosomalna,
zespół Klinefeltera - aneuploidia chromosomów płci;
zespół Turnera - aneuploidia chromosomów płci..
Kariotypy osób z zespołem Downa: 47,XY,+21 (kariotyp męski), 47,XX,+21 (kariotyp żeński).
Częstość występowania tej choroby szacuje się na 1 przypadek na 750 żywych urodzeń.
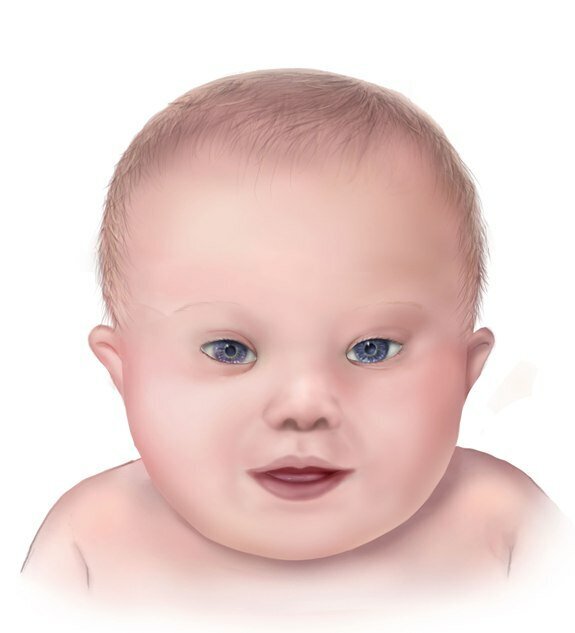
Do typowych objawów zespołu Downa zalicza się:
pojedynczą bruzdę dłoniową (zamiast podwójnej bruzdy) na jednej lub obu dłoniach;
migdałowaty kształt oczu wynikający z fałd nad powiekami;
krótsze kończyny;
osłabione napięcie mięśniowe oraz wystający język;
częstsza niż u dzieci zdrowych zapadalność na ciężkie zapalenie płuc;
występowanie wrodzonych wad serca;
upośledzenie umysłowe.
Ryzyko wystąpienia zespołu Downa związane jest głównie z wiekiem matki – im jest ona starsza, tym wyższe jest prawdopodobieństwo wystąpienia choroby u dziecka. Dojrzewanie komórek rozrodczych kobiet trwa znacznie dłużej niż plemników u mężczyzn. W połączeniu z potencjalną ekspozycją na toksyczne substancje powoduje to częstsze występowanie nondysjunkcji prowadzących do powstania komórki jajowej z dodatkowym chromosomem 21 pary.
Kariotyp osób z zespołem Klinefeltera: 47,XXY.
Częstość występowania tej choroby szacuje się na 1 przypadek na 1000 urodzonych chłopców.

Do typowych objawów zespołu Klinefeltera zalicza się:
skąpe owłosienie ciała;
ginekomastię (rozwój piersi) spowodowaną obniżonym stężeniem testosteronu;
niedorozwój członka i jąder, przerost prostaty;
dłuższe niż u osób zdrowych kończyny, dłonie i stopy;
bezpłodność.
Osoby z zespołem Klinefeltera są niezdolne do spłodzenia potomstwa, ze względu na brak zdolności produkcji plemników. Leczenie testosteronem wpływa na rozwinięcie wtórnych cech płciowych, ale bezpłodność jest regułą. Niekiedy występuje u nich także obniżony potencjał umysłowy.
Kariotyp osób z zespołem Turnera: 45,X0.
Częstość występowania tej choroby szacuje się na 1 przypadek na 5000 urodzonych dziewczynek.

Do typowych objawów zespołu Turnera zalicza się:
niski wzrost (dorosłe kobiety osiągają wzrost od 125 do 150 cm);
krępą budowę ciała;
płetwowatość szyi z niską linią owłosienia;
krótkie palce u stóp i dłoni;
krótką klatkę piersiową;
niedorozwój wtórnych cech płciowych (krótka pochwa, mała macica);
pierwotny brak miesiączki;
słabo wykształcone sutki.
Rozwój umysłowy jest przeważnie prawidłowy. Osoby chore są bardziej podatne na osteoporozę, cukrzycę, choroby tarczycy.
Osoby z zespołem Turnera są kobietami, najczęściej bezpłodnymi (rzadko możliwe jest zajście w ciążę). Wiek matki nie ma związku z częstotliwością występowania choroby.
Kariotyp osób z zespołem Edwardsa: 47,XY,+18 (kariotyp męski) lub 47,XX,+18 (kariotyp żeński).
Częstość występowania tej choroby szacuje się na 1 przypadek na 5000 żywych urodzeń.
Do typowych objawów zespołu Edwardsazalicza się:
małogłowie;
wystającą potylicę;
wady strukturalne serca;
wady nerek i jelit;
rozszczep wargi lub podniebienia;
szeroki rozstaw oczu;
deformację stóp;
nie w pełni rozwinięte kciuki;
brak kości promieniowej
U większości płodów, u których diagnozuje się zespół Edwardsa, występują wady letalne. Ryzyko urodzenia dziecka z zespołem Edwardsa wzrasta z wiekiem matki.
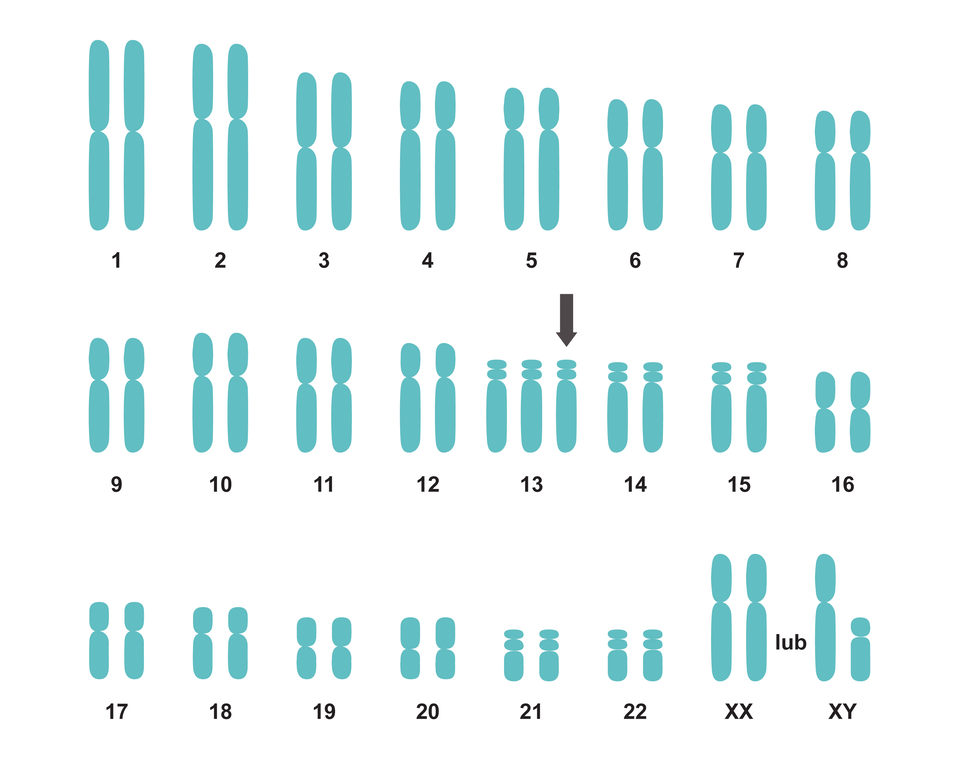
Kariotyp osób z zespołem Pataua: 47,XY,+13 (kariotyp męski) lub 47,XX,+13 (kariotyp żeński).
Częstość występowania tej choroby szacuje się na 1 przypadek na 8000 żywych urodzeń.
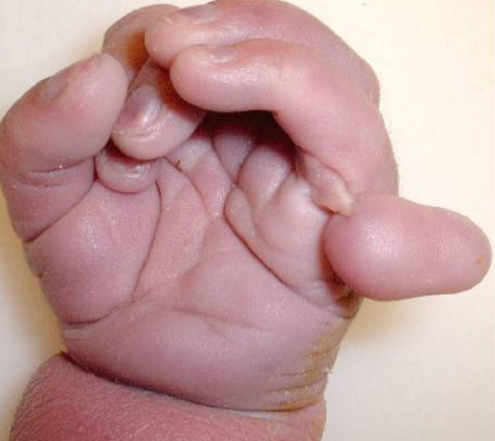
Do typowych objawów zespołu Pataua zalicza się:
bardzo niską wagę urodzeniową;
ubytki skóry na głowie;
zdeformowaną twarz (rozszczepy);
nieprawidłowo wykształcone oczy (tzw. cyklopia) i nos (jego brak);
wady układów krążenia, nerwowego, wydalniczego;
anomalie kończyn (np. polidaktylia).
Przy trisomii 13 chromosomu występuje zwiększone ryzyko poronienia lub urodzenia martwego dziecka. Około 70% dzieci z zespołem Pataua umiera w ciągu pierwszego roku życia, 30% w ciągu 2 lat. Ryzyko urodzenie dziecka z zespołem Pataua wzrasta wraz wiekiem matki.
Aberracje strukturalne chromosomów
Aberracje strukturalne są następstwem pęknięć chromosomów. Pęknięcie to oznacza przerwanie obu nici DNA. Przerwane nici mogą zostać na powrót połączone dzięki mechanizmom naprawczym komórki, które jednak w przypadku podwójnych pęknięć często zawodzą.
Większość uszkodzeń w budowie chromosomów to przypadkowe błędy, które powstają nagle w plemnikach lub komórkach jajowych. Dlatego najczęściej nie są one dziedziczone po rodzicach. Tylko niewielka ich część jest przekazywana z pokolenia na pokolenie: wówczas rodzice mogą być nosicielami wady, sami nie mając żadnych objawów chorobowych. Do uszkodzenia struktury chromosomu może również dojść na etapie rozwoju zarodka, a nawet w trakcie dorosłego życia. Czynnikami sprzyjającymi powstawaniu tych wad są, m.in. promieniowanie jonizujące oraz mutageny chemiczne.
Przykładem choroby będącej następstwem aberracji strukturalnej jest przewlekła białaczka szpikowa.
Mikrodelecje to zaburzenia strukturalne chromosomów polegające na utracie ich bardzo niewielkiego fragmentu. Są niezauważalne w obrazie mikroskopowym chromosomów i wykrywalne jedynie przy użyciu bardziej skomplikowanych analiz. Nawet takie mało rozległe zmiany mogą mieć duży wpływ na zdrowie i funkcjonowanie organizmu obciążonego wadą.
Diagnostyka zespołów chromosomowych
Jedną z metod wykrywania mutacji chromosomowych są badania cytogenetyczne. Polegają one na analizie kariotypu – oceniana jest liczba oraz struktura chromosomów komórek badanego organizmu.
Kariotyp i jego analiza
Kariotyp to kompletny zestaw chromosomów komórki somatycznej organizmu. U każdego zdrowego człowieka składa się on z 46 chromosomów, z których połowę dziedziczymy po matce, a połowę po ojcu. Prawidłowy zapis kariotypu kobiet to 46,XX, natomiast dla mężczyzn – 46,XY.
Analizę kariotypu człowieka wykonuje się najczęściej z komórek somatycznych, przede wszystkim z limfocytów krwi obwodowej. Wyizolowane komórki poddaje się hodowli i stymuluje do podziałów mitotycznych, a następnie dodaje się kolchicynękolchicynę, która zatrzymuje podziały w stadium metafazy – momencie, w którym chromosomy są najbardziej skondensowane i najlepiej widoczne. Po umieszczeniu komórek w roztworze hipotonicznym pęcznieją one, co powoduje rozsunięcie chromosomów i ułatwia ich obserwację. Następnie materiał jest barwiony w celu uwidocznienia charakterystycznego wzoru prążków, a sfotografowane chromosomy zestawia się w pary homologiczne według wielkości i kształtu, układając je od największych do najmniejszych, tworząc kariotyp.
Przeprowadź obserwację w wirtualnym laboratorium „Sporządzenie kariotypu na przykładzie cebuli i podstawy jego analizy”. Następnie wykonaj polecenie.
Przeprowadź obserwację w laboratorium. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz wyniki i wnioski.
Temat: Sporządzanie i analiza kariotypu cebuli zwyczajnej (Allium cepa)
Problem naukowy: Z ilu chromosomów i jakiego typu składa się kariotyp cebuli zwyczajnej (Allium cepa)?
Hipoteza: Kariotyp cebuli zwyczajnej (Allium cepa) złożony jest z 10 chromosomów metacentrycznych.
Sprzęt laboratoryjny:
pipety;
szalki Petriego;
mikroskop.
Materiały i odczynniki:
cebula
1 M kwas chlorowodorowy (HCl)
substancja stymulująca podziały komórkowe
kolchicyna
barwnik acetokarmina
Instrukcja wykonania obserwacji:
Odetnij fragment cebuli, umieść go na szalce Petriego i wytraw ściany komórkowe za pomocą 1 M HCl.
Przenieś komórki na nową szalkę i dodaj substancję stymulującą podziały komórkowe.
Przenieś komórki na nową szalkę i dodaj kolchicynę.
Przenieś komórki na szalkę z roztworem hipotonicznym i zalej barwnikiem.
Obserwuj komórki pod mikroskopem i zrób zdjęcie chromosomów.
Dopasuj chromosomy w pary, żeby utworzyć kariotyp.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDHB7LAKC
Laboratorium 1
Przeprowadzono obserwację.
Temat: Sporządzanie i analiza kariotypu cebuli zwyczajnej (Allium cepa)
Problem naukowy: Z ilu chromosomów i jakiego typu składa się kariotyp cebuli zwyczajnej?
Hipoteza: Kariotyp cebuli zwyczajnej (Allium cepa) złożony jest z 10 chromosomów metacentrycznych.
Sprzęt laboratoryjny: probówki, skalpel, mikroskop, szalki Petriego, zlewka.
Materiały i odczynniki: cebula, 1 M kwas chlorowodorowy HCl, substancja stymulująca podziały komórkowe, kolchicyna, barwnik acetokarmina.
Instrukcja wykonania obserwacji:
1. Odcięto fragment cebuli, umieszczono go na szalce Petriego i wytrawiono ściany komórkowe za pomocą 1 M HCl.
2. Przeniesiono komórki na nową szalkę i dodano substancję stymulującą podziały komórkowe.
3. Przeniesiono komórki na nową szalkę i dodano kolchicynę.
4. Przeniesiono komórki na szalkę z roztworem hipotonicznym i zalano barwnikiem.
5. Obserwowano komórki pod mikroskopem i zrobiono zdjęcie chromosomów.
6. Dopasowano chromosomy w pary, żeby utworzyć kariotyp.
Szczegóły obserwacji 1.
Kwas chlorowodorowy jest stosowany do perforacji ścian komórkowych, aby odczynniki wykorzystywane w kolejnych krokach procedury kariotypowania mogły wniknąć do komórek.
Szczegóły obserwacji 2.
Kolchicyna jest alkaloidem pozyskiwanym z nasion ziemowitu jesiennego (Colchicum autumnale). Wiążąc się z tubuliną, uniemożliwia powstawanie wrzeciona podziałowego, przez co blokuje przebieg cyklu komórkowego w metafazie.
Szczegóły obserwacji 3.
Acetokarmina jest barwnikiem używanym do wybarwiania kwasów nukleinowych, ponieważ wiąże się specyficznie z DNA, jednocześnie nie zabarwiając cytoplazmy. Ponadto jest mniej toksyczna oraz tańsza niż inne barwniki wykorzystywane do barwienia materiału genetycznego.
Wyniki:
Cebula zwyczajna (Allium cepa) ma 8 par chromosomów, w tym 4 pary chromosomów metacentrycznych, 3 pary chromosomów submetacentrycznych oraz 1 parę chromosomów akrocentrycznych.
Wnioski:
Kariotyp cebuli zwyczajnej złożony jest z 16 chromosomów, które różnią się od siebie budową i lokalizacją centromeru.
Weryfikacja hipotezy:
Hipoteza okazała się błędna.
Znaczenie analizy kariotypu
Analiza kariotypu osób starających się o dziecko pozwala na określenie występowania wad genetycznych bądź zespołu aberracji chromosomowych, które mogą być dziedziczone lub przyczyniać się do niepłodności lub nawet bezpłodności pary. Osoba, u której wykazano tego typu wadę, otrzymuje informacje o dziedziczeniu zmiany w kariotypie (prawdopodobieństwie urodzenia zdrowego potomka) oraz o możliwości leczenia lub innego rodzaju pomocy i wsparcia.
Wskazania do badania kariotypu:
wiek przyszłej matki powyżej 35 roku życia
poronienia nawracające;
martwe urodzenie;
trudności z poczęciem dziecka;
bezpłodność;
wystąpienie nowotworów;
przypadek choroby genetycznej w rodzinie;
duże odchylenie od normy w parametrach nasienia;
liczba plemników poniżej 5 mln/ml;
brak plemników w nasieniu.
W przypadku par, u których występuje problem z poczęciem dziecka, analiza kariotypu pozwala wykluczyć genetyczne przyczyny bezpłodności, a w przypadku wykrycia nieprawidłowości – pozwala określić, czy problem leży po stronie mężczyzny czy kobiety. Dzięki temu możliwe jest powzięcie odpowiednich działań w dalszych staraniach o potomstwo.
Analiza kariotypu przeprowadzana jest rutynowo w ramach badań prenatalnych, co umożliwia wykrycie nieprawidłowości w liczbie i strukturze chromosomów dziecka już na etapie ciąży. Daje to rodzicom i lekarzom czas na przygotowanie się do specjalistycznej opieki po narodzinach.
Podsumowanie
Aberracje liczbowe:
- obejmują aneuploidie (zmiana liczby pojedynczych chromosomów) oraz euploidie (zmiana liczby całych zestawów chromosomów),
- najczęściej powstają w wyniku nondysjunkcji chromosomów podczas mejozy.Przykłady chorób spowodowanych aberracjami liczbowymi:
- Zespół Downa (trisomia 21) – 47,XX,+21 lub 47,XY,+21; ryzyko wzrasta wraz z wiekiem matki.
- Zespół Klinefeltera – 47,XXY; dotyczy mężczyzn i prowadzi m.in. do bezpłodności.
- Zespół Turnera – 45,X0; dotyczy kobiet, często wiąże się z bezpłodnością, przy prawidłowym rozwoju intelektualnym.Aberracje strukturalne:
- są skutkiem pęknięć chromosomów i błędnej naprawy DNA,
- mogą powstawać pod wpływem promieniowania jonizującego i mutagenów chemicznych,
- najczęściej pojawiają się de novo, rzadziej są dziedziczne,Przykłady chorób spowodowanych aberracjami strukturalnymi:
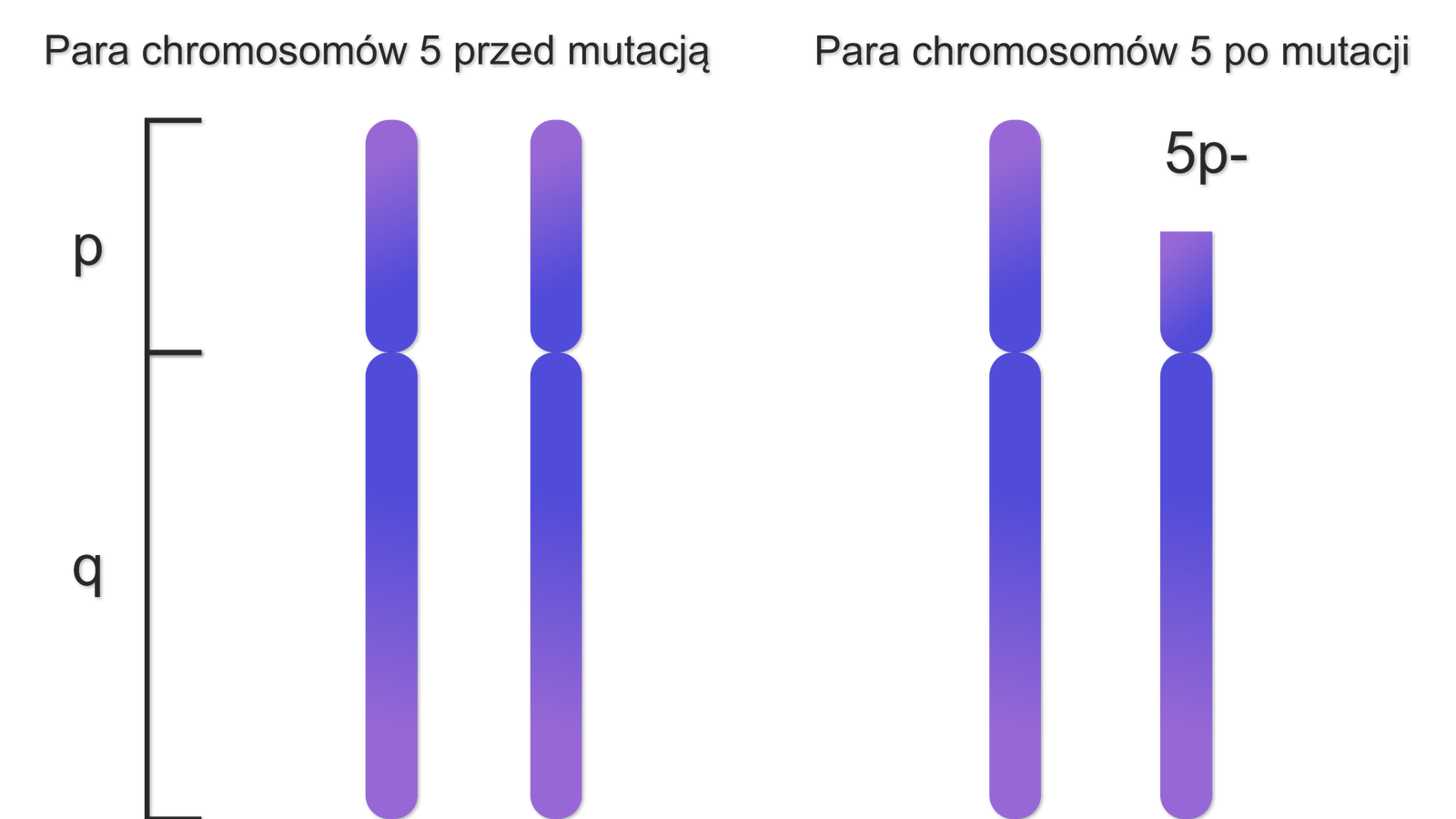
- Zespół cri du chat– spowodowany delecją krótkiego ramienia chromosomu 5; objawia się charakterystycznym płaczem niemowlęcia przypominającym miauczenie kota, opóźnieniem rozwoju i niepełnosprawnością intelektualną.
- Przewlekła białaczka szpikowa – związana z translokacją między chromosomami 9 i 22, tzw. chromosom Filadelfia; prowadzi do powstania genu fuzyjnego BCR‑ABL kodującego nieprawidłową kinazę tyrozynową, co skutkuje niekontrolowanymi podziałami komórek szpiku.Kariotyp to pełny zestaw chromosomów w diploidalnej komórce somatycznej; u człowieka prawidłowy kariotyp wynosi 46 chromosomów (46,XX u kobiet i 46,XY u mężczyzn).
Analiza kariotypu umożliwia ocenę liczby i budowy chromosomów oraz wykrycie aberracji chromosomowych, które mogą prowadzić do wad rozwojowych, chorób genetycznych, niepłodności lub poronień.
Znaczenie analizy kariotypu:
- opiera się m.in. na analizie kariotypu,
- pozwala ocenić ryzyko urodzenia dziecka z wadą genetyczną,
- jest szczególnie zalecane przy problemach z płodnością, poronieniach, chorobach genetycznych w rodzinie lub u kobiet po 35. roku życia.Badania kariotypu pomagają rozpoznać genetyczne przyczyny chorób, zaplanować dalsze leczenie oraz świadomie przygotować się do rodzicielstwa.
Ćwiczenia utrwalające
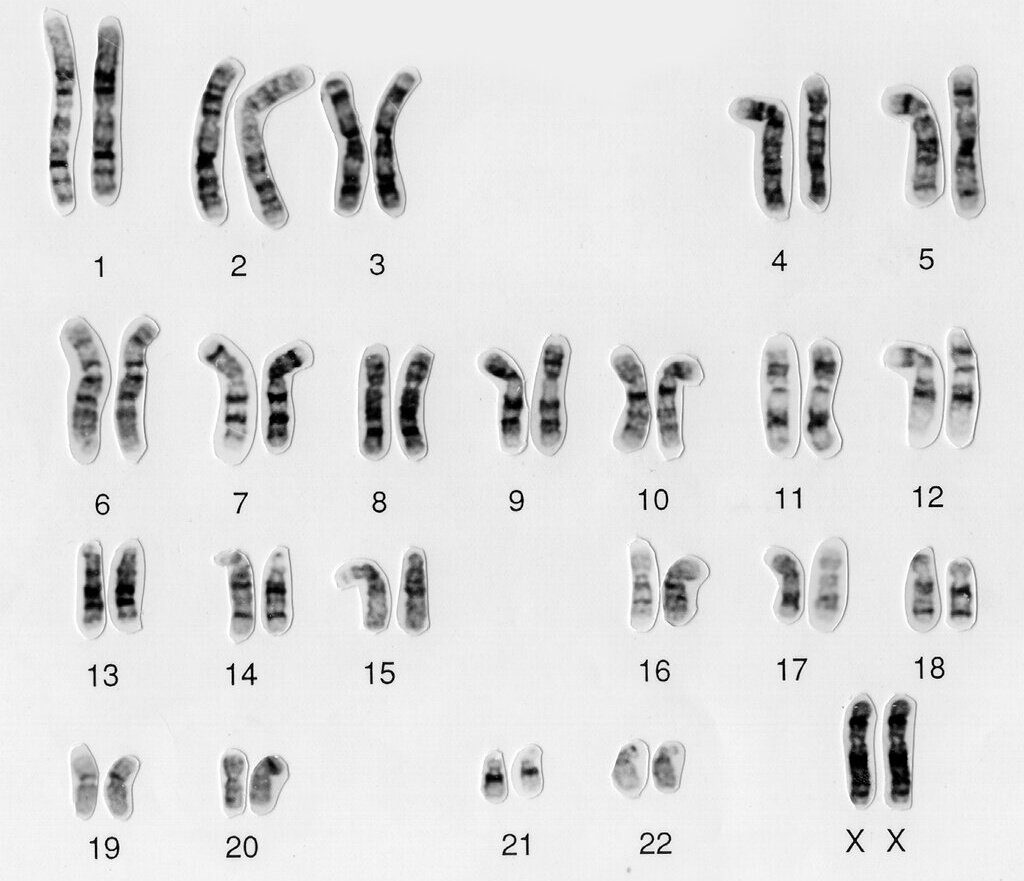
Ilustracja przedstawia kariotyp, który zawiera dwadzieścia dwie pary chromosomów. Ostatnia para to chromosom XY lub XX. W parze dwudziestej pierwszej są trzy krótkie chromosomy.

Wróć do polecenia na stronie „Na dobry początek” i dopisz brakujące definicje. Pamiętaj, żeby nie kopiować słownika, ale wyjaśnić każde słowo kluczowe w miarę możliwości swoimi słowami.