Składniki organiczne
Białka
Opiszesz budowę aminokwasów.
Dowiesz się, jak powstają wiązania peptydowe.
Poznasz budowę chemiczną białek oraz ich właściwości fizykochemiczne i biologiczne.
Białka należą do najbardziej zróżnicowanych cząsteczek w organizmach żywych. Są niezbędne do prawidłowego funkcjonowania wszystkich komórek, tkanek i narządów. Białka zbudowane są z aminokwasów, które łączą się ze sobą w różnorodne sekwencje, tworząc unikalne struktury. Dzięki tej różnorodności białka pełnią szereg kluczowych funkcji w organizmach, takich jak kataliza reakcji chemicznych, transport substancji, czy obrona przed patogenami.
Aminokwasy - budowa i właściwości
Aminokwasy to związki organiczne występujące powszechnie we wszystkich organizmach żywych. Spośród ponad 300 poznanych aminokwasów wyróżnia się 20 będących składnikami białek. Pozostałe występują w komórkach w stanie wolnym w tzw. puli aminokwasowej, różnej dla poszczególnych tkanek i organizmów.
Cząsteczka aminokwasu zawiera centralnie umieszczony atom węgla, wokół którego rozmieszczone są cztery różne podstawniki:
grupa aminowa (–NHIndeks dolny 22)
grupa karboksylowa (–COOH)
atom wodoru
łańcuch boczny (-R)
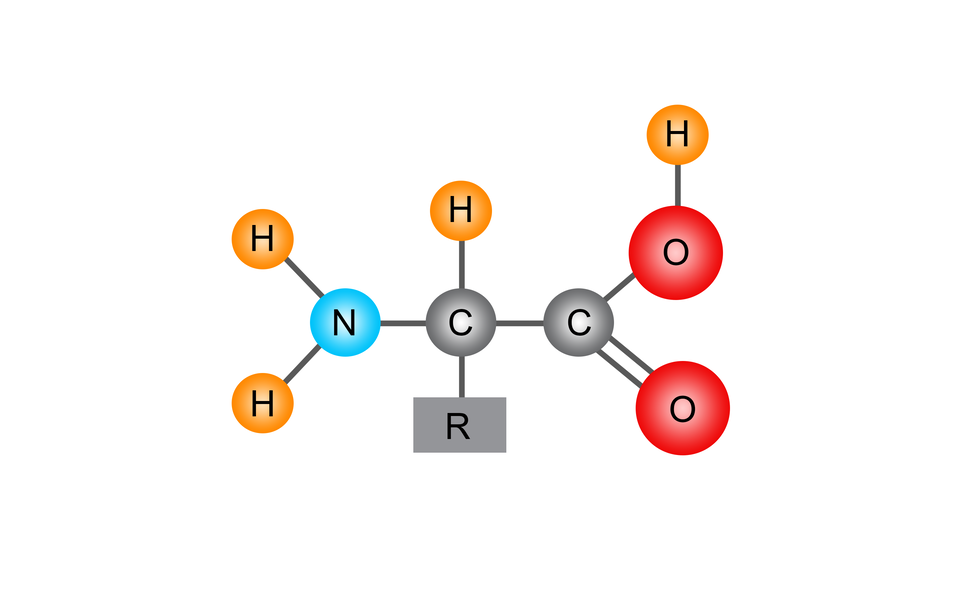
Aminokwasy to pochodne węglowodorów zbudowane ze związanych kowalencyjnie z atomem węgla: grupy aminowej (–NH2), grupy karboksylowej (–COOH), atomu wodoru oraz specyficznego łańcucha bocznego (R).
Rodzaj łańcucha bocznego decyduje o właściwościach fizycznych i chemicznych aminokwasów.
Tworzenie wiązań peptydowych
W cząsteczkach białek aminokwasy połączone są ze sobą wiązaniami peptydowymi, które powstają między grupą karboksylową jednego aminokwasu, a grupą aminową drugiego. Reakcja prowadząca do wytworzenia wiązania peptydowego jest reakcją kondensacji, a jej produktem ubocznym jest woda.
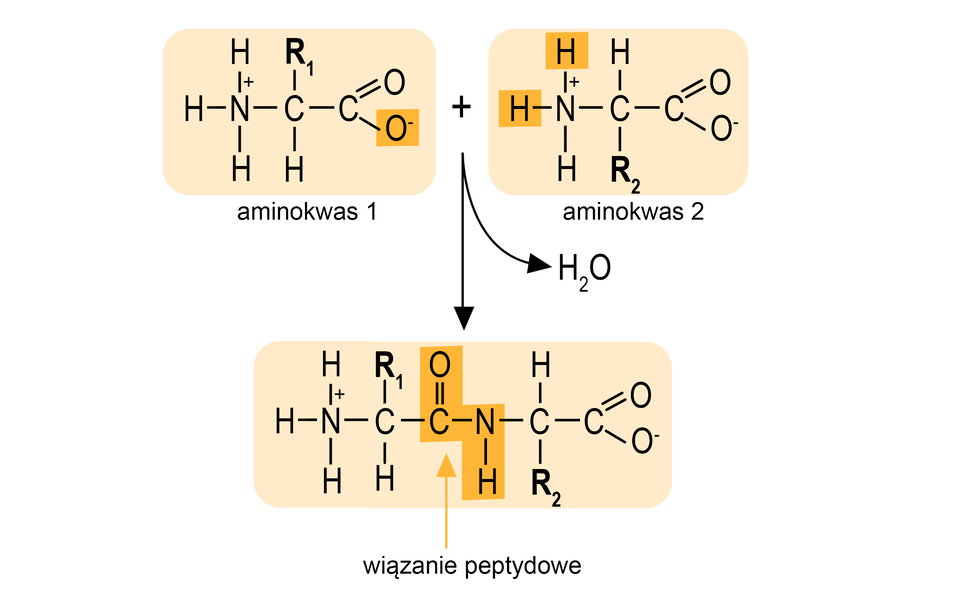
Wiązanie peptydowe występuje pomiędzy atomem azotu z grupy aminowej (–NHIndeks dolny 22) a atomem węgla z grupy karboksylowej (–COOH).
Peptydy i białka
W rezultacie połączenia się aminokwasów przez wiązanie peptydowe powstaje peptyd. Jeśli łączą się dwa aminokwasy, produktem jest dipeptyd, przyłączenie kolejnego aminokwasu tworzy tripeptyd, a następnego - tetrapeptyd. W ten sposób powstają oligopeptydy, czyli krótkie łańcuchy zbudowane z 2 do 10 reszt aminokwasowych. Te utworzone z od 11 do 100 reszt aminokwasowych nazywa się polipeptydami. Łańcuchy aminokwasów utworzone z co najmniej 101 reszt aminokwasów nazywane są białkami. Na jednym końcu każdego łańcucha peptydowego znajduje się wolna grupa aminowa (N‑koniec), a na drugim wolna grupa karboksylowa (C‑koniec).
Białka w organizmie powstają z udziałem 20. aminokwasów. Łączą się one ze sobą w różnych kombinacjach, dzięki czemu tworzą różnorodne białka.
Podział białek
Ze względu na skład białka dzieli się na proste i złożone.
Białka proste zbudowane są wyłącznie z aminokwasów, natomiast białka złożone zawierają w składzie dodatkowe, nieaminokwasowe składniki. Nieaminokwasowy składnik, zwany grupą prostetyczną, może być związkiem organicznym, metalem lub połączeniem obu tych elementów.
Rodzaje białek złożonych
Ze względu na kształt białka dzieli się na globularne i fibrylarne.
Białka globularne mają kształt kulisty lub sferoidalny. Zbudowane są z silnie pofałdowanych lub pozwijanych łańcuchów peptydowych. Są rozpuszczalne w wodzie lub wodnych roztworach kwasów, zasad i soli; w roztworach często tworzą koloidy. Stanowią większość białek występujących w organizmach, pełniąc różne funkcje. Do białek globularnych należą albuminyalbuminy, globulinyglobuliny oraz histonyhistony.
Białka fibrylarne charakteryzują się wydłużoną, włóknistą strukturą, co nadaje im dużą wytrzymałość mechaniczną i sprężystość. Są praktycznie nierozpuszczalne w wodzie i roztworach soli i odporne na działanie kwasów i zasad. Białka fibrylarne występują w dużych ilościach w tkance łącznej, np. keratyna - główny budulec wytworów rogowych naskórka (włosów, paznokci) oraz elastyna i kolagen nadające m.in. elastyczność i wytrzymałość skórze oraz ścięgnom.
Właściwości fizykochemiczne białek
Koagulacja białek
Koagulacja polega na łączeniu cząstek, naturalnie występujących w stanie rozproszonym, w większe skupienia - agregaty. Jest to proces przejścia od rozproszonego stanu koloidalnego (wodnego roztworu białek nazywanego zolemzolem) do stabilniejszej i bardziej zwartej struktury nazywanej żelemżelem.
Proces ten zachodzi pod wpływem: dodania elektrolitów, środków odwadniających (np. aceton), działań mechanicznych (np. wstrząsanie, mielenie, ucieranie), wysalaniawysalania przez soli metali lekkich lub odparowywania.
Proces odwrotny do koagulacji to peptyzacja. Polega on na rozpuszczeniu żelu w wodzie i powstaniu zolu (roztworu koloidalnego).

Denaturacja białek
Denaturacja białka to zaburzenie struktury łańcuchów polipeptydowych. Proces ten zachodzi pod wpływem różnych czynników fizycznych i chemicznych – zostały one wyszczególnione na poniższym schemacie.
- Nazwa kategorii: Czynniki wywołujące denaturację{color=#F16472}
- Nazwa kategorii: Czynniki fizyczne{color=#FF3399}
- Nazwa kategorii: temperatura{color=#FF66CC}
- Nazwa kategorii: ciśnienie{color=#FF66CC}
- Nazwa kategorii: ultradźwięki{color=#FF66CC}
- Nazwa kategorii: promieniowania ultrafioletowe{color=#FF66CC}
- Nazwa kategorii: promieniowania rentgenowskie{color=#FF66CC}
- Nazwa kategorii: promieniowania jonizujące{color=#FF66CC} Koniec elementów należących do kategorii Czynniki fizyczne{color=#FF3399}
- Nazwa kategorii: Czynniki chemiczne{color=#FFCC33}
- Nazwa kategorii: kwasy{color=#FFCC66}
- Nazwa kategorii: zasady{color=#FFCC66}
- Nazwa kategorii: mocznik{color=#FFCC66}
- Nazwa kategorii: niektóre rozpuszczalniki organiczne{color=#FFCC66}
- Nazwa kategorii: detergenty jonowe{color=#FFCC66}
- Nazwa kategorii: sole metali ciężkich{color=#FFCC66} Koniec elementów należących do kategorii Czynniki chemiczne{color=#FFCC33}
- Elementy należące do kategorii Czynniki wywołujące denaturację
- Elementy należące do kategorii Czynniki fizyczne
- Elementy należące do kategorii Czynniki chemiczne
Denaturacja to proces powodujący zmianę nie tylko struktury białka, ale także jego właściwości biologicznych (np. utratę aktywności enzymatycznej) i fizykochemicznych (zmniejszenie rozpuszczalności i wytrącenie z roztworu, rozpad na mniejsze podjednostki).
Znaczenie biologiczne białek
Podsumowanie
Aminokwasy
Aminokwasy to związki organiczne zbudowane z grupy aminowej (-NH2), grupy karboksylowej (-COOH), atomu wodoru oraz specyficznego łańcucha bocznego (-R).
Budowa białek
Białka są związkami organicznymi zbudowanymi z aminokwasów połączonych wiązaniami peptydowymi (-CO‑NH-).
Rodzaj i kolejność aminokwasów decydują o strukturze, właściwościach fizykochemicznych i biologicznych białka.
Podział białek
Białka proste – zbudowane wyłącznie z aminokwasów (np. albuminy, histony).
Białka złożone – zawierają dodatkowe grupy niebiałkowe, np. cukry (glikoproteiny), metale (metaloproteiny) lub lipidy (lipoproteiny).
Wpływ czynników fizykochemicznych na białka
Koagulacja – przejściowa zmiana struktury białka pod wpływem soli (np. wysalanie albumin).
Denaturacja – zmiana struktury białka pod wpływem wysokiej temperatury, kwasów, zasad, alkoholi, promieniowania UV itp.
Biologiczne znaczenie białek
Albuminy – transport substancji we krwi, regulacja ciśnienia osmotycznego.
Globuliny – funkcja odpornościowa (przeciwciała).
Histony – białka zasadowe połączone z DNA w jądrze komórkowym.
Kolagen – składnik tkanki łącznej, zapewnia wytrzymałość skóry i ścięgien.
Keratyna – buduje włosy, paznokcie, skórę.
Hemoglobina – transport tlenu w erytrocytach.
Mioglobina – magazynuje tlen w mięśniach.
Ćwiczenia utrwalające
Wróć do polecenia na stronie „Na dobry początek” i dopisz brakujące definicje. Pamiętaj, żeby nie kopiować słownika, ale wyjaśnić każde słowo kluczowe w miarę możliwości swoimi słowami.