Stopnie utlenienia
Stopień utlenienia
Stopień utlenienia to pojęcie umowne (zapisywane cyfrą rzymską). W przypadku pierwiastka danego związku chemicznego będzie to liczba dodatnich lub ujemnych ładunków elementarnych, jakie przypisalibyśmy atomom tego pierwiastka, gdyby wszystkie wiązania utworzone przez atom były jonowe.
Reguły obliczania stopni utlenienia
Atomy (cząsteczki) pierwiastków w stanie wolnym mają zawsze stopień utlenienia równy zero.
Suma stopni utlenienia wszystkich atomów, wchodzących w skład cząsteczki, równa jest zero.
Suma stopni utlenienia wszystkich atomów, wchodzących w skład jonu, równa jest ładunkowi jonu.
Suma stopni utlenienia w jonie wynosi‑II, ponieważ:
Gdzie:
stopień utlenienia siarki wynosi VI;
stopień utlenienia tlenu wynosi -II.
Fluor w związkach ma zawsze stopień utlenienia równy -I.
Tlen w związkach ma na ogół stopień utlenienia równy -II, ale w nadtlenkach (np. ) stopień ten wynosi -I, w ponadtlenkach (np. ) -½, a w cząsteczce fluorku tlenu () II.
Wodór w związkach, w większości przypadków, ma stopień utlenienia równy I, ale w wodorkach litowców i berylowców stopień ten wynosi -I.
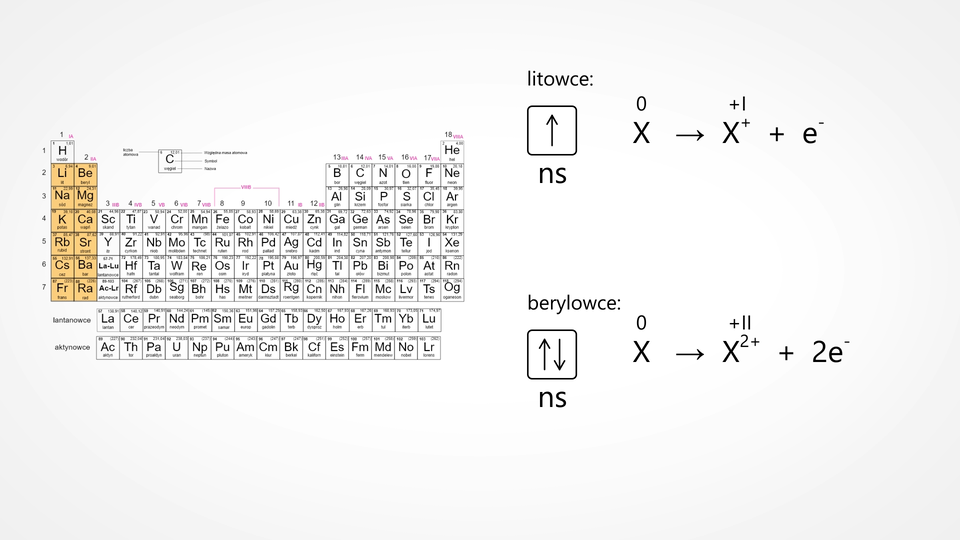
Litowce w związkach chemicznych mają zawsze stopień utlenienia I, a berylowce II.
Atomy metali w związkach przyjmują dodatnie stopnie utlenienia.
W cząsteczce związku chemicznego dodatni stopień utlenienia ma atom o niższej elektroujemności, a ujemny – atom o wyższej elektroujemności (czyli bardziej elektroujemny).

Wykorzystanie stopni utlenienia
Znajomość stopni utlenienia jest istotna z punktu widzenia reakcji chemicznych, zachodzących z wymianą elektronów, tzw. reakcji redoks. Zmiany stopnia utlenienia sygnalizują, że nastąpiła wymiana elektronów między atomami. Wśród reakcji redoks wymienić można reakcje spalania, wymiany pojedynczej oraz niektóre reakcje syntezy i analizy.
Czy wiesz, jak ważną rolę może odgrywać określenie stopni utlenienia związków? Zapoznaj się z poniższą grafiką interaktywną, ilustrującą różnice między związkami chromu na różnym stopniu utlenienia. W zależności od stopnia utlenienia, właściwości związków mogą ulegać zmianom. Po analizie schematu rozwiąż ćwiczenia.
Czy wiesz, jak ważną rolę może odgrywać określenie stopni utlenienia związków? Zapoznaj się z opisem grafiki interaktywnej, przedstawiającej różnice między związkami chromu na różnym stopniu utlenienia. W zależności od stopnia utlenienia, właściwości związków mogą ulegać zmianom. Po zapoznaniu się ze schematem rozwiąż ćwiczenia.
Chrom na pewnym stopniu utlenienia ma negatywny wpływ na stan naszego zdrowia. Jest dla nas szkodliwy. Podaj, o który stopień utlenienia chodzi i jakie mogą być skutki kontaktu ze związkami chromu właśnie na tym stopniu utlenienia. Jak myślisz, dlaczego warto zdefiniować stopnie utlenienia w związkach?
Rozpisz stopnie utleniania w heksahydroksochromianie(III) sodu.
Zapoznaj się z filmem pt. „Jak przewidzieć typowe stopnie utlenienia pierwiastka?”, a następnie rozwiąż ćwiczenia sprawdzające.
Film dostępny pod adresem /preview/resource/RJA8tXFoGTiyk
Film nawiązujący do treści materiału dotyczącej przewidywania stopni utlenienia pierwiastków.
Atom pierwiastka X może przyjmować stopnie utlenienia od wartości 0 do wartości +IV, a atom pierwiastka Y może przyjmować stopnie utlenienia od wartości -IV do wartości +IV. Do jakich grup układu okresowego pierwiastków chemicznych należą pierwiastki X i Y?