Utleniacz, reduktor, reakcja redoks
Reakcje utleniania i redukcji
Reakcje utleniania‑redukcji (reakcje redoks) to takie, w których dochodzi do zmiany stopnia utlenienia atomu w danym reagencie. W celu wyjaśnienia, czym jest reakcja utleniania‑redukcji, zdefiniujmy najpierw oddzielnie proces utleniania i proces redukcji.
Jak zmieniają się stopnie utlenienia atomów pierwiastków chemicznych w reakcji syntezy chlorku magnezu?
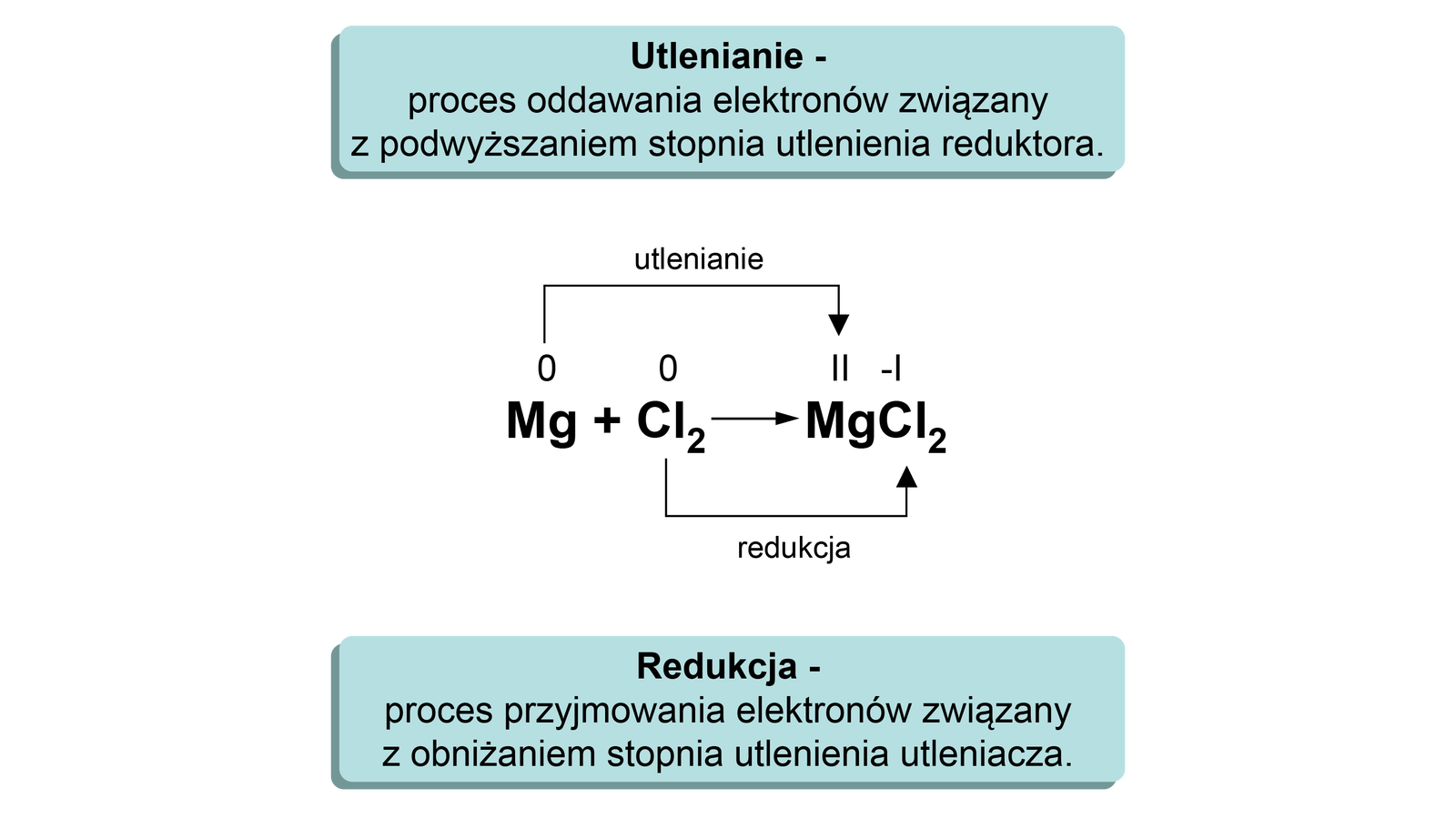
Analizę problemu postawionego w pytaniu warto rozpocząć od określenia stopni utlenienia atomów w poszczególnych reagentach. Równanie można zatem zapisać w postaci:
Z równania wynika, że atom magnezu podwyższył swój stopień utlenienia z do , natomiast atom chloru obniżył swój stopień utlenienia z do -. Zapiszmy teraz schematy procesów utleniania i redukcji:
W każdej reakcji utleniania‑redukcji liczba elektronów oddanych w procesie utleniania musi być równa liczbie elektronów pobranych w procesie redukcji. Jest to tzw. bilans elektronowy reakcji. Bilans ten, równy sumie elektronów pobranych i oddanych, powinien wynosić zero.
Z zapisów tych wynika, że:
1. W procesie utleniania reduktor () zwiększył swój stopień utlenienia (z na ) i oddał (dwa) elektrony.
2. W procesie redukcji utleniacz () obniżył swój stopień utlenienia (z na -) i przyjął (jeden) elektron.
Wymiana elektronów w omawianej reakcji zachodzi pomiędzy reduktorem, który oddaje elektrony, a pobierającym elektrony utleniaczem. Reakcje te nie mogą przebiegać niezależnie, ponieważ elektrony oddane (przez atomy magnezu) w reakcji utleniania są pobrane (przez atomy chloru) w reakcji redukcji.
Przeanalizuj równania reakcji redoks przedstawione w poniższym filmie samouczku, a następnie rozwiąż ćwiczenia.

Film dostępny pod adresem /preview/resource/RJ23gwEvZONjC
Film nawiązujący do treści materiału - dotyczą analizy równań reakcji redoks.
Określ stopnie utlenienia atomów pierwiastków w poniższym równaniu.
Wskaż utleniacz i reduktor w poniższej reakcji redoks. W tym celu zaznacz pole utleniacz/reduktor o określonym kolorze. Następnie kliknij na wybrany reagent, aby pokolorować element w ramce. Po pokolorowaniu obu elementów, sprawdź poprawną odpowiedź.
Dana jest reakcja opisana następującym równaniem:
Ile wynosi liczba oddanych elektronów w procesie utlenienia, jeżeli reduktorem jest metaliczny cynk?