Przewidywanie kierunku reakcji redoks
Jak przewidzieć przebieg reakcji redoks?
Znając wartości potencjałów standardowych półogniw, można przewidzieć przebieg (kierunek) reakcji redoks. Potencjały standardowe półogniw są zebrane w tablicach fizykochemicznych.
Im bardziej ujemny potencjał standardowy półogniwa, tym postać zredukowana jest silniejszym reduktorem, a więc chętniej się utlenia (układ chętniej oddaje elektrony).
Im bardziej dodatni potencjał standardowy półogniwa, tym postać utleniona jest silniejszym utleniaczem – łatwiej dochodzi do reakcji redukcji (układ chętniej przyjmuje elektrony).
Oznacza to, że w każdej reakcji chemicznej musi zostać spełniony warunek:
Innymi słowy: znajomość wartości potencjałów standardowych półogniw różnego rodzaju pozwala na przewidywanie:
czy dana reakcja utlenienia‑redukcji zajdzie w rzeczywistości (w warunkach standardowych);
jaki będzie kierunek reakcji chemicznej (w warunkach standardowych).
Poza tym im większa jest różnica potencjałów standardowych półogniw, tym bardziej prawdopodobna jest dana reakcja chemiczna.
Jak będzie przebiegała reakcja redoks, w której biorą udział atomy żelaza i srebra? Zapisz równanie reakcji utleniania i redukcji. Podaj reduktor i utleniacz.
Podane są następujące potencjały standardowe półogniw:
Korzystając z podanych potencjałów standardowych półogniw, przewidujemy przebieg reakcji redoks. Wiemy, że potencjał utleniacza jest większy od potencjału reduktora, a więc:
postać utleniona srebra () będzie przyjmowała elektrony, czyli się redukowała – utleniaczem będzie ;
postać zredukowana żelaza () będzie oddawała elektrony, czyli się utleniała – reduktorem będzie .
Reakcja utleniania:
Reakcja redukcji:
Liczba elektronów oddanych przez reduktor i przyjętych przez utleniacz musi być jednakowa, dlatego należy dokonać bilansu elektronowo‑jonowego. W tym przypadku wszystkie elementy równania reakcji redukcji należy pomnożyć przez 2.
Bilans elektronowo‑jonowy:
Następnie dodajemy do siebie stronami równanie utleniania i redukcji. Przebieg reakcji redoks jest następujący:
Na czym polega reguła zegara?
Przebieg reakcji redoks można także przewidzieć, korzystając z reguły zegara na podstawie z poniższego schematu.
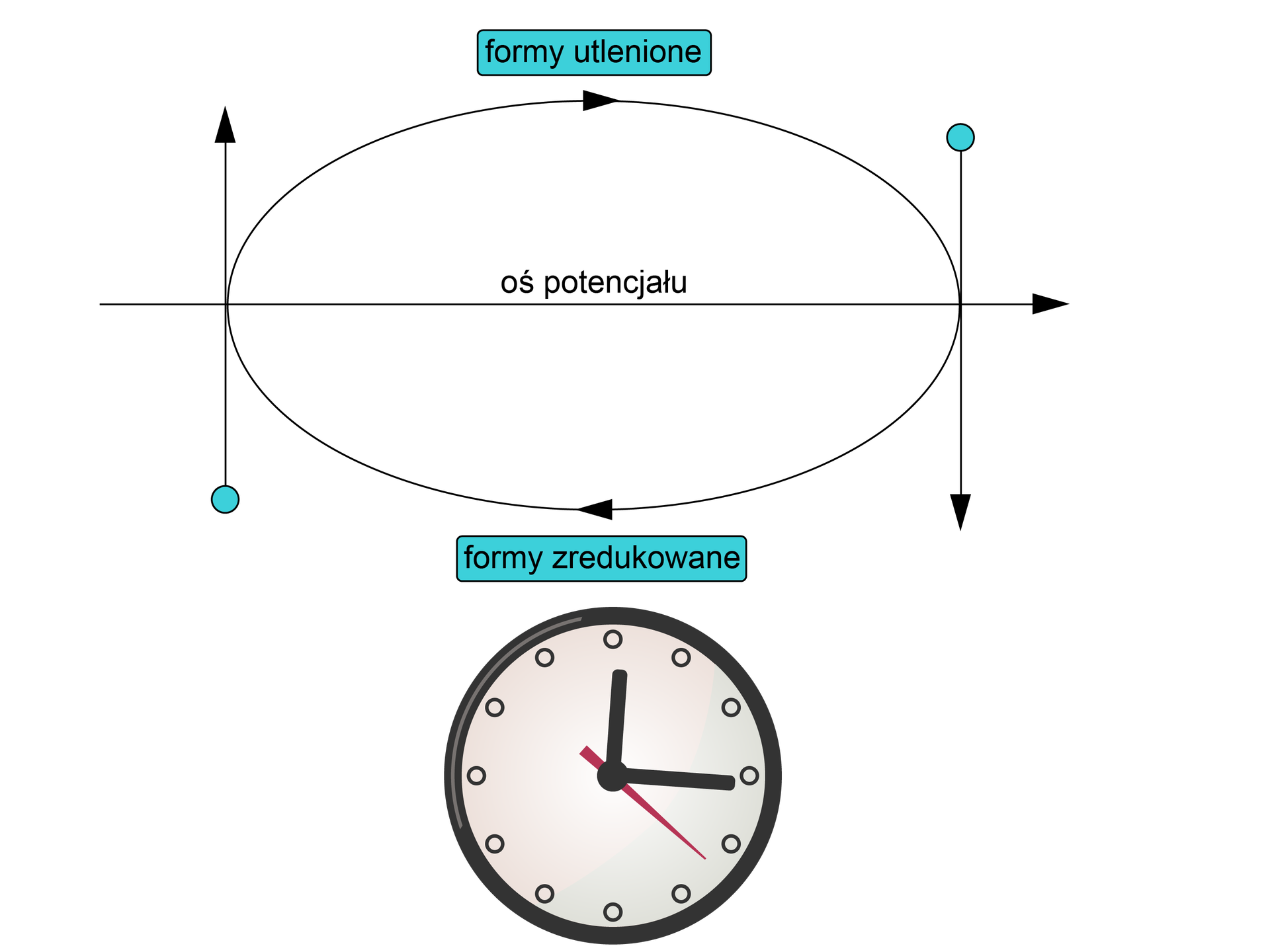
Układanie schematu należy rozpocząć od narysowania osi liczbowej, na której zaznacza się wartości potencjałów standardowych półogniw. Do miejsc zaznaczenia wartości potencjałów rysuje się proste prostopadłe. Nad osią należy zapisać formy utlenione, a pod osią formy zredukowane. Strzałki oznaczające kierunek przebiegu reakcji, zgodnie z ruchami wskazówek zegara, wskazują, że forma musi w trakcie reakcji przekształcić się w formę , a forma w formę .
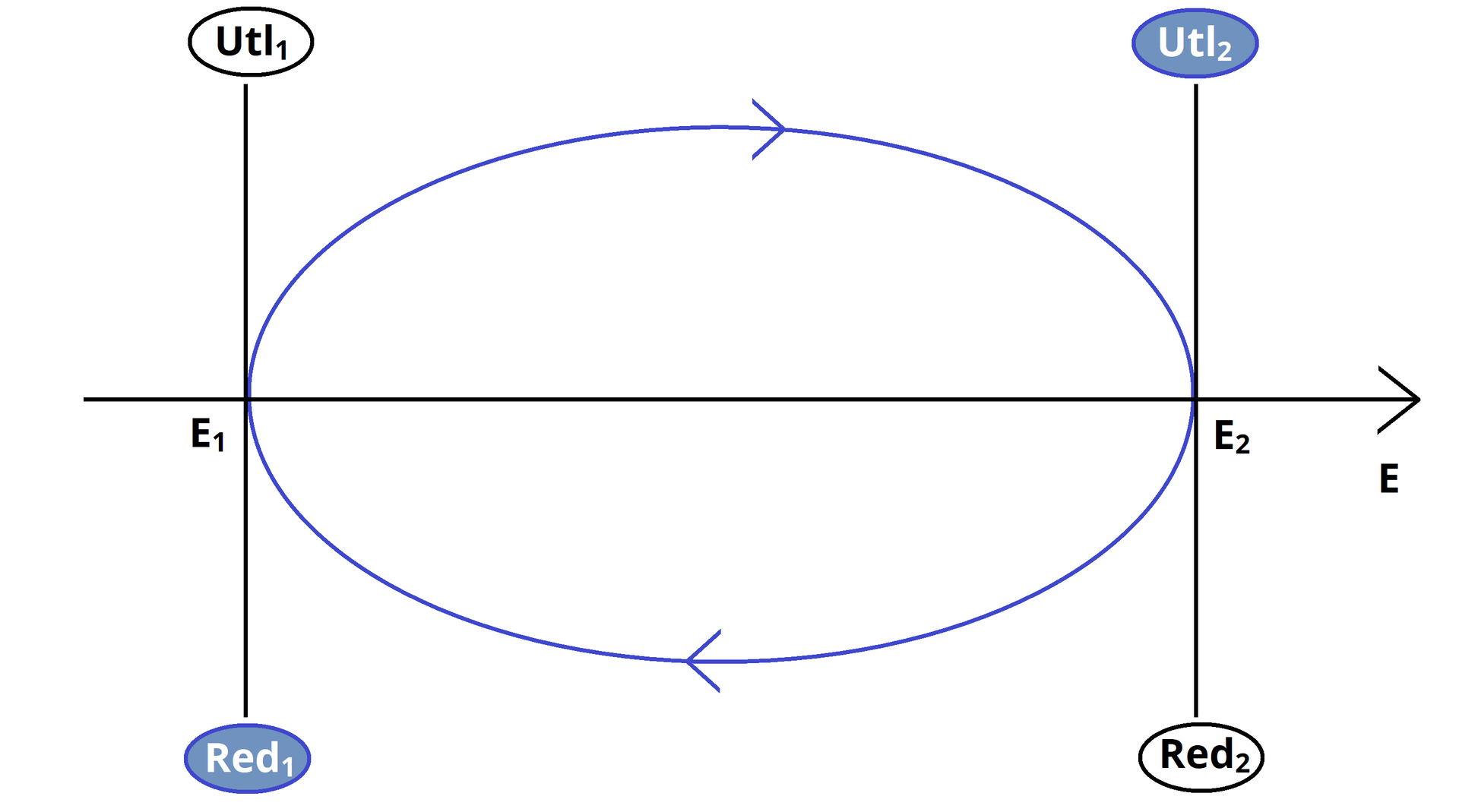
Przebieg reakcji redoks jest następujący:
Jak będzie przebiegała reakcja redoks, w której biorą udział atomy miedzi i srebra? Rozwiązując zadanie, skorzystaj z reguły zegara.
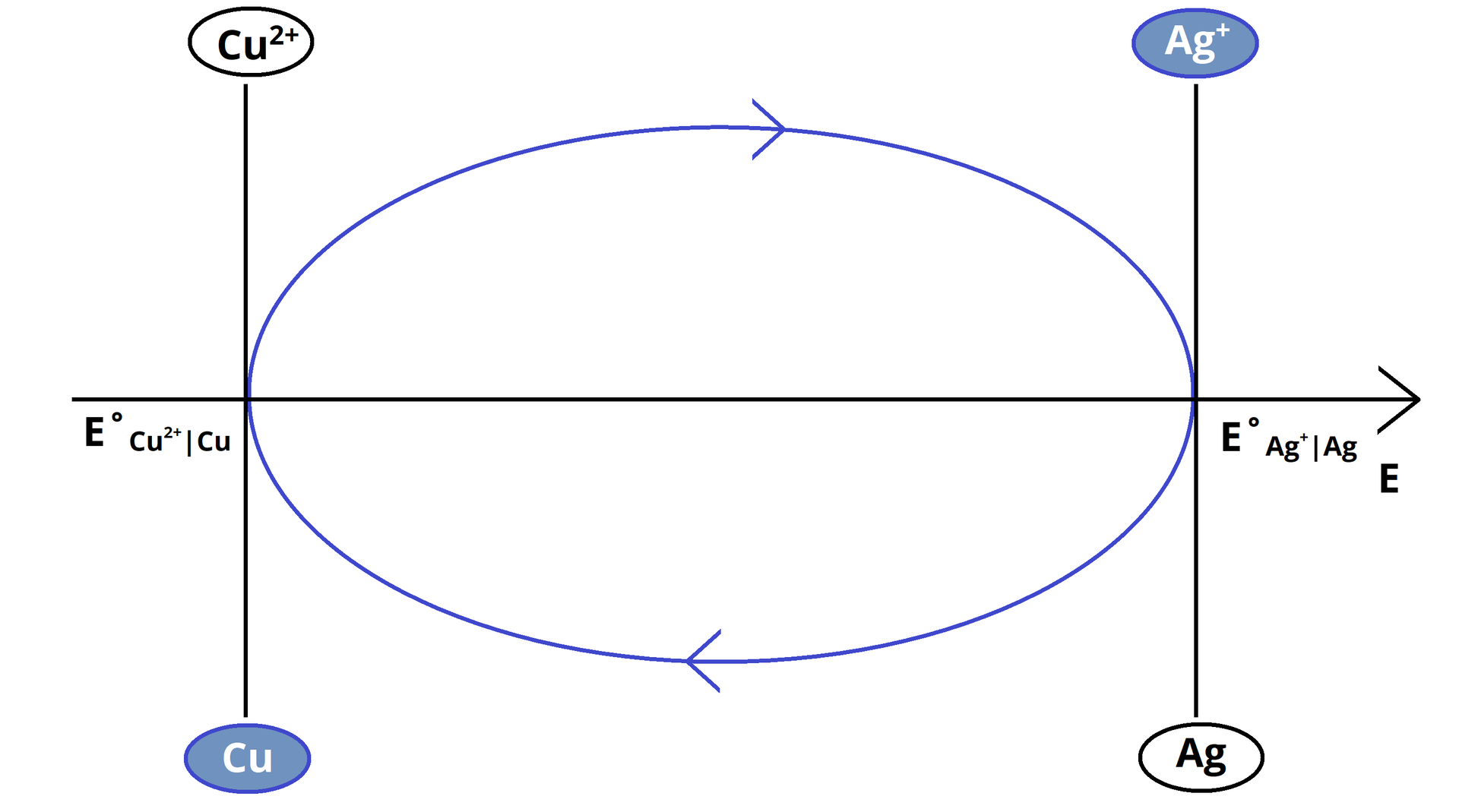
Przebieg reakcji redoks (po uwzględnieniu bilansu elektronowo‑jonowego):
Reguła zegara pozwala przewidzieć przebieg reakcji redoks, jednak nie uwzględnia współczynników stechiometrycznych. Należy więc samemu zbilansować równanie reakcji tak, aby po prawej i lewej stronie równania reakcji liczba moli danej substancji oraz ładunki były równe.
Potencjały standardowe półogniw są zebrane w tablicach fizykochemicznych.
półogniwo | równanie reakcji przebiegającej na półogniwie | [V] |
|---|---|---|
-3,04 | ||
-2,93 | ||
-2,91 | ||
-2,84 | ||
-2,71 | ||
-2,36 | ||
-1,97 | ||
-1,66 | ||
-1,18 | ||
-0,83 | ||
-0,76 | ||
-0,74 | ||
-0,44 | ||
-0,40 | ||
-0,28 | ||
-0,23 | ||
-0,15 | ||
-0,14 | ||
-0,13 | ||
-0,04 | ||
0,00 | ||
+0,07 | ||
+0,15 | ||
+0,15 | ||
+0,22 | ||
+0,27 | ||
+0,34 | ||
+0,40 | ||
+0,52 | ||
+0,54 | ||
+0,77 | ||
+0,80 | ||
+0,85 | ||
+1,09 | ||
+1,22 | ||
+1,23 | ||
+1,33 | ||
+1,36 | ||
+1,50 | ||
+1,51 | ||
+1,51 | ||
+1,72 | ||
+1,78 | ||
+1,92 | ||
+2,87 |
Tabela potencjałów standardowych półogniw w temperaturze 25°C.
Indeks dolny Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010 oraz L. Jones, P. Atkins, Chemia ogólna: cząsteczki, materia, reakcje, tłum. J. Kuryłowicz, Warszawa 2012. Indeks dolny koniecNa podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010 oraz L. Jones, P. Atkins, Chemia ogólna: cząsteczki, materia, reakcje, tłum. J. Kuryłowicz, Warszawa 2012.
Zapoznaj się z filmem samouczkiem, a następnie zweryfikuj zdobytą wiedzę poprzez rozwiązanie ćwiczeń.

Film dostępny pod adresem /preview/resource/RlJPkaMfIADta
Film nawiązujący do treści materiału dotyczącej potencjałów standardowych a reakcji redoks oraz czy można przewidzieć samorzutny przebieg reakcji na ich podstawie.
W poniższej tabeli przedstawiono równania reakcji elektrodowych oraz odpowiadające im wartości potencjałów standardowych dwóch półogniw redoks:
Równanie reakcji elektrodowej | Potencjał standardowy, V |
Korzystając z danych zawartych w tabeli, napisz sumaryczne równanie reakcji, która zachodzi w pracującym ogniwie zbudowanym z analizowanych półogniw.
W poniższej tabeli zestawiono potencjały standardowe wybranych półogniw metalicznych.
Półogniwo | E°, V |
Przeanalizuj dane zawarte w tabeli, a następnie wykonaj punkty 1 i 2.
Wskaż te kationy zawarte w tabeli, względem których cynk może pełnić funkcję reduktora.
Napisz równania odpowiednich reakcji redoks pomiędzy atomami cynku a kationami wskazanymi przez Ciebie w poprzednim punkcie.
Spróbuj teraz przewidzieć kierunek reakcji redoks w praktyce. W tym celu przeprowadź doświadczenia w poniższym wirtualnym laboratorium oraz wykonaj ćwiczenia pod nim zawarte.
Wykonaj zgodnie z instrukcją doświadczenia dotyczące przewidywania przebiegu reakcji redoks, na podstawie potencjałów standardowych półogniw, a następnie zapisz obserwacje, wyniki i wnioski. Dodatkowo, w zeszycie do lekcji chemii zapisz odpowiednie równania reakcji redoks. Wskaż w nich utleniacz i reduktor.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1Q2TDTBA
Szafa laboratoryjna
Zapoznaj się z opisem doświadczenia dotyczącego przewidywania przebiegu reakcji redoks, na podstawie potencjałów standardowych półogniw. Na koniec rozwiąż krótkie zadanie sprawdzające.
Analiza doświadczenia: Przewidywanie przebiegu reakcji redoks na podstawie potencjałów standardowych półogniw.
Problem badawczy: Czy można przewidzieć przebieg reakcji redoks na podstawie potencjałów standardowych półogniw?
Hipoteza: Na podstawie potencjałów standardowych półogniw można przewidzieć przebieg reakcji redoks.
Reagenty:
- HCl (1 mol na decymetr sześcienny)
- siarczan() miedzi() CuSO₄ (1 mol na decymetr sześcienny)
- siarczan() cynku ZnSO₄ (1 mol na dm³)
Sprzęt laboratoryjny:
- zlewki - naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych
- cylindry miarowe - podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy
- druciki metalowe (dwa miedziane i dwa cynkowe).
Wykonanie:
Część .
1. Na środku stołu laboratoryjnego postawiono dwie zlewki.
2. Za pomocą cylindra miarowego do każdej zlewki dodano 10 centymetrów sześciennych kwasu chlorowodorowego.
3. Do pierwszej zlewki (po lewej stronie) dodano drucik cynkowy, a do drugiej zlewki (po prawej stronie) drucik miedziany.
Część .
4. Na środku stołu laboratoryjnego postawiono dwie zlewki.
5. Za pomocą cylindra miarowego do pierwszej zlewki (po lewej stronie) dodano 10 centymetrów sześciennych roztworu siarczanu() miedzi().
6. Za pomocą cylindra miarowego do drugiej zlewki (po prawej stronie) dodano 10 centymetrów sześciennych roztworu siarczanu() cynku.
7. Do pierwszej zlewki (po lewej stronie) dodano drucik cynkowy, a do drugiej zlewki (po prawej stronie) drucik miedziany.
Obserwacje:
Po umieszczeniu drucika cynkowego w zlewce, zawierającej kwas chlorowodorowy, wydzielają się pęcherzyki gazu, a drucik się roztwarza.
Po umieszczeniu drucika miedziowego w zlewce, zawierającej kwas chlorowodorowy, nie obserwuje się żadnych zmian.
Po umieszczeniu drucika cynkowego w zlewce, zawierającej wodny roztwór siarczanu() miedzi(), drucik pokrywa się ceglastoczerwonym nalotem, a roztwór zmienia barwę z niebieskiej na bezbarwną.
Po umieszczeniu drucika miedziowego w zlewce, zawierającej wodny roztwór siarczanu() cynku, nie obserwuje się żadnych zmian.
Wyniki:
Miedź nie ulega reakcji utleniania zarówno w kontakcie z kwasem chlorowodorowym, jak i w kontakcie z siarczanem() cynku. Z kolei cynk ulega reakcji utleniania zarówno w kontakcie z kwasem chlorowodorowym, jak i z siarczanem() miedzi().
Wnioski:
Cynk ulega reakcji utleniania, wypierając wodór z kwasu, czego skutkiem jest wydzielanie się gazowego wodoru oraz roztwarzanie cynkowego drutu. Cynk utlenia się także w kontakcie z siarczanem() miedzi(), co skutkuje wytrącaniem się metalicznej miedzi i zmianą barwy roztworu, wskutek wypierania miedzi z siarczanu() miedzi() z wytworzeniem siarczanu() cynku. Miedź z kolei nie ulega reakcji w żadnym wypadku. Zdolność do utleniania jest więc bezpośrednio skorelowana z potencjałem standardowym półogniw, bowiem im niższa jest wartość tego potencjału, tym większa skłonność danego metalu do utleniania. Miedź nie może w proponowanych doświadczeniach ulegać utlenieniu, ponieważ potencjał półogniwa, w którym powinna zajść redukcja, jest w obu przypadkach niższy niż potencjał półogniwa miedziowego.
Hipoteza została potwierdzona.