Aldehydy i ketony- właściwości
Aldehydy - właściwości fizyczne
Najprostszy aldehydy – metanal (formaldehyd)– w temperaturze pokojowej jest gazem, pozostałe zaś człony szeregu homologicznego w zależności od liczby atomów węgla, są cieczami lub ciałami stałymi. Aldehydy zawierające w cząsteczkach do siedmiu atomów węgla, mają charakterystyczną ostrą woń, a zawierające więcej niż siedem atomów węgla w cząsteczce – mają przyjemny zapach.
W szeregu homologicznym nasyconych aldehydów łańcuchowych systematycznie rosną temperatury wrzenia i topnienia oraz gęstość, maleje natomiast rozpuszczalność w wodzie. Temperatury wrzenia nasyconych aldehydów są niższe niż odpowiednich alkoholi, co jest wynikiem braku asocjacji cząsteczek tych związków.
Właściwości fizyczne wybranych n‑aldehydów przedstawia poniższa tabela.
Aldehyd | TIndeks dolny TT [°C] | TIndeks dolny WW [°C] | Właściwości fizyczne w temp. pokojowej | Wzór półstrukturalny |
|---|---|---|---|---|
formaldehyd (metanal) | -90,2 | -19,10 | bezbarwny gaz o charakterystycznym ostrym zapachu drażniącym błony śluzowe, bardzo dobrze rozpuszczalny w wodzie – wodny roztwór to formalina, oraz eterze i etanolu; łatwo polimeryzuje |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
acetaldehyd (etanal) | -123,0 | 20,70 | łatwopalna, bezbarwna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie, etanolu, eterze i benzynie |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
heksanal | -56,0 | 131,0 | ciecz o nieprzyjemnym zapachu, słabo rozpuszczalna w wodzie, rozpuszczalna w rozpuszczalnikach organicznych | 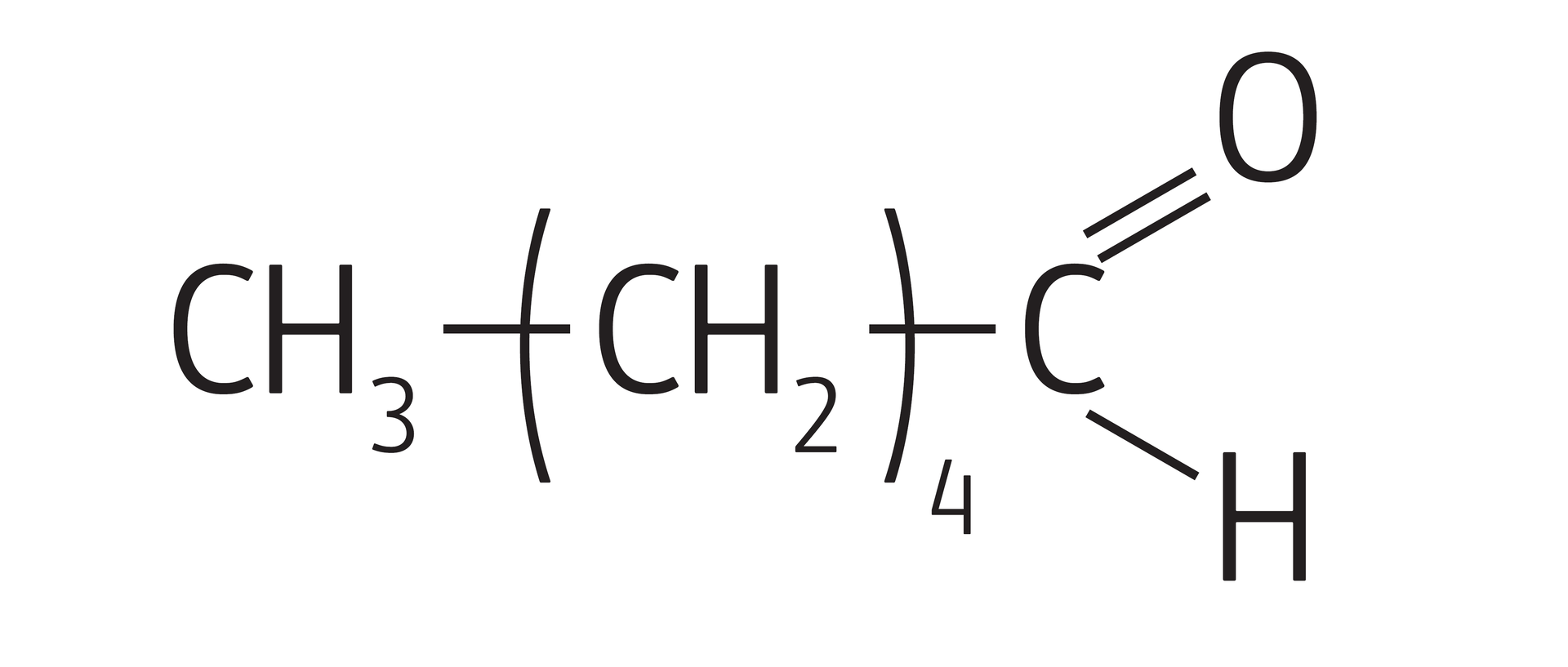 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
oktanal | -25,4 | 170,0 | nierozpuszczalna w wodzie ciecz o zapachu przypominającym cytrynę lub róże, rozpuszczalna w rozpuszczalnikach organicznych |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Indeks dolny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010. Indeks dolny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010.
Zmiany właściwości fizycznych aldehydów w szeregu homologicznym

Ketony – właściwości fizyczne
Ketony nasycone, o prostych łańcuchach węglowych, są cieczami o niższych temperaturach wrzenia, niż odpowiadające im alkohole. Podobnie jak w przypadku aldehydów, związane jest to z brakiem asocjacji cząsteczek tych związków. W szeregu homologicznym ketonów, wraz ze wzrostem długości łańcucha, rosną temperatury wrzenia i topnienia.
Właściwości fizyczne wybranych ketonów zestawiono w poniższej tabeli.
Keton | TIndeks dolny TT [°C] | TIndeks dolny WW [°C] | Właściwości fizyczne w temperaturze pokojowej | Wzory półstrukturalne |
|---|---|---|---|---|
propan‑2‑on (aceton) | -94,7 | 56,20 | bezbarwna, lotna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie, eterze dietylowym i alkoholu metylowym |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
butan‑2‑on | -86,7 | 79,6 | bezbarwna, lotna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
pentan‑3‑on | -39,0 | 101,7 | bezbarwna, lotna, palna ciecz o charakterystycznym zapachu, z powietrzem tworzy mieszaniny wybuchowe |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Indeks dolny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010. Indeks dolny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010.
Zmiany właściwości fizycznych ketonów w szeregu homologicznym

Na podstawie powyższych tabel podsumuj zdobyte informacje i sporządź tabelę, w której porównasz właściwości fizyczne ketonów i aldehydów.
Odróżnianie aldehydów i ketonów
Aldehydy i ketony posiadają charakterystyczne grupy funkcyjne – ketonową i aldehydową. Różnica między aldehydem a ketonem polega na obecności atomu wodoru przyłączonego do grupy karbonylowej w aldehydzie. W ketonach atom wodoru nie występuje. W ketonach zamiast niego występuje reszta oznaczona R', pod czym może kryć się np. grupa alkilowa.
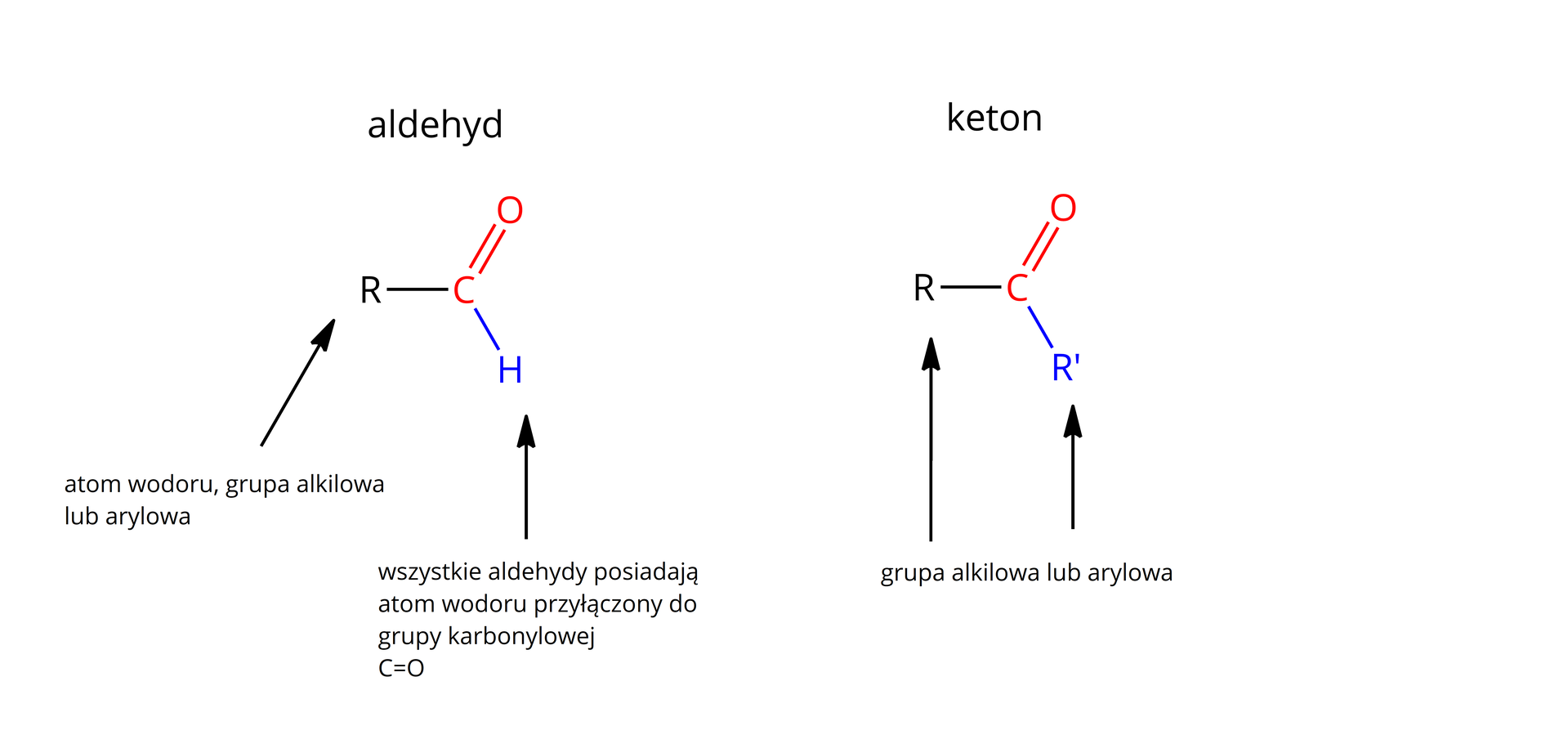
To właśnie różnice w budowie aldehydów i ketonów warunkują różnice w ich właściwościach chemicznych. W laboratorium, aby szybko sprawdzić, czy mamy do czynienia z aldehydem czy ketonem, wykorzystuje się proste reakcje charakterystyczne, omówione w dalszej części lekcji.
Próba Trommera
Próbę Trommera warto wykonać za każdym razem, kiedy trzeba sprawdzić, czy badany związek wykazuje właściwości redukujące. Aldehydy są związkami redukującymi, ponieważ posiadają grupę aldehydową. Dają więc pozytywny wynik próby Trommera. Ketony z kolei nie wykazują właściwości redukujących, ponieważ nie posiadają atomu wodoru przy grupie karbonylowej. Odczynnik Trommera przygotowuje się, dodając wodny roztwór wodorotlenku sodu do wodnego roztworu siarczanu miedzi . Otrzymany niebieski koloidalny osad wodorotlenku miedzi ogrzewa się następnie z badanym związkiem w środowisku zasadowym. W przypadku pozytywnego wyniku testu, miedź z stopnia utlenienia redukuje się do .
Próba Tollensa
Próba Tollensa nazywana jest inaczej próbą lustra srebrowego ze względu na produkt reakcji podczas pozytywnego wyniku próby – metaliczne srebro osadzające się na ściankach probówki. Również wykonuje się ją w celu oznaczenia jakościowego związku o właściwościach redukujących. Jest to reakcja opierająca się na utlenianiu i redukcji. Prowadzona jest w lekko zasadowym środowisku. Do wykonania próby Tollensa wykorzystuje się odczynnik Tollensa, czyli roztwór zawierający jony diaminasrebra , powstały przez dodanie wody amoniakalnej do roztworu azotanu srebra. W reakcji ze związkiem redukującym jon diaminasrebra redukuje się do metalicznego srebra.
W celu odróżnienia aldehydów i ketonów przeprowadza się reakcje charakterystyczne dla danych grup związków. Przedstawione laboratorium umożliwia wykonanie próby Tollensa dla przedstawicieli obu grup – propan--onu (acetonu) oraz formaldehydu. Przeprowadź eksperyment, sformułuj problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.
Szafa laboratoryjna
Odróżnianie aldehydów i ketonów z wykorzystaniem odczynnika Tollensa
Odróżnianie aldehydów od ketonów.
Problem badawczy:
Jak można odróżnić aldehydy od ketonów?
Hipoteza:
Aldehydy od ketonów można odróżnić za pomocą próby Tollensa.
Sprzęt laboratoryjny:
łaźnia wodna – naczynie wypełnione wodą, służące do ogrzewania lub schładzania innych naczyń laboratoryjnych wraz z ich zawartością.
zlewka () – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
probówki – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki:
roztwór azotanu srebra;
roztwór formaldehydu – metanalu (formalina);
propan--on (aceton);
roztwór amoniaku.
Przebieg doświadczenia:
Przygotowano łaźnię wodną: włączono palnik, umieszczono nad nim trójnóg, postawiono na trójnogu zlewkę wypełnioną wodą.
Do dwóch czystych probówek wlano po roztworu azotanu srebra.
Do każdej z probówek dodawano kroplami roztwór amoniaku do czasu, aż rozpuścił się wytrącający się początkowo osad tlenku srebra.
Do pierwszej probówki wlano roztworu formaldehydu.
Do drugiej probówki wlano propan--onu (acetonu).
Wstrząśnięto probówkami i wstawiono je do gorącej łaźni wodnej.
Obserwacje:
W probówce z formaldehydem na ścianach probówki pojawił się srebrny osad.
W probówce z acetonem nie pojawił się srebrny osad.
