Fluorowcopochodne węglowodorów
Fluorowcopochodne węglowodorów - nazewnictwo
Przez bardzo długi czas naukowcy uważali, że obecność organicznych związków halogenopochodnych w środowisku naturalnym jest spowodowana jedynie działalnością człowieka. Jednak to nieprawda. Naukowcy ustalili obecność ponad dwóch tysięcy różnych związków zawierających fluor, chlor, brom i jod, które występują naturalnie. Zdecydowanie więcej można znaleźć w organizmach morskich (algi czy skorupiaki) niż lądowych. Co ciekawe, da się je również spotkać w znanych i ogólnie dostępnych roślinach, takich jak pomidory, ziemniaki czy mandarynki i pomarańcze. Oczywiście, powstające związki organiczne fluorowcopochodnych występują w bardzo niewielkich ilościach i w dużym rozproszeniu, przez co pozyskiwanie ich z tych źródeł jest mało efektywne i nieopłacalne, w porównaniu do laboratoryjnych metod otrzymywania.
Aby lepiej zrozumieć właściwości tych związków, przeanalizuj teraz ich budowę oraz zasady nazewnictwa chlorowcopochodnych.
Czy wiesz, w jaki sposób tworzy się nazwy halogenopochodnych węglowodorów? Czy wiesz, od czego zależy kolejność numerowania atomów węgla w cząsteczkach tych pochodnych? Czy wiesz, jak nazwać związek, który zawiera nieidentyczne atomy halogenów w cząsteczce? Zapoznaj się z poniższą animacją, a następnie wykonaj zadania.

Film dostępny pod adresem /preview/resource/R1ZFSpAwR4Yiy
Film przedstawiający jak tworzy się nazwy halogenopochodnych węglowodorów.
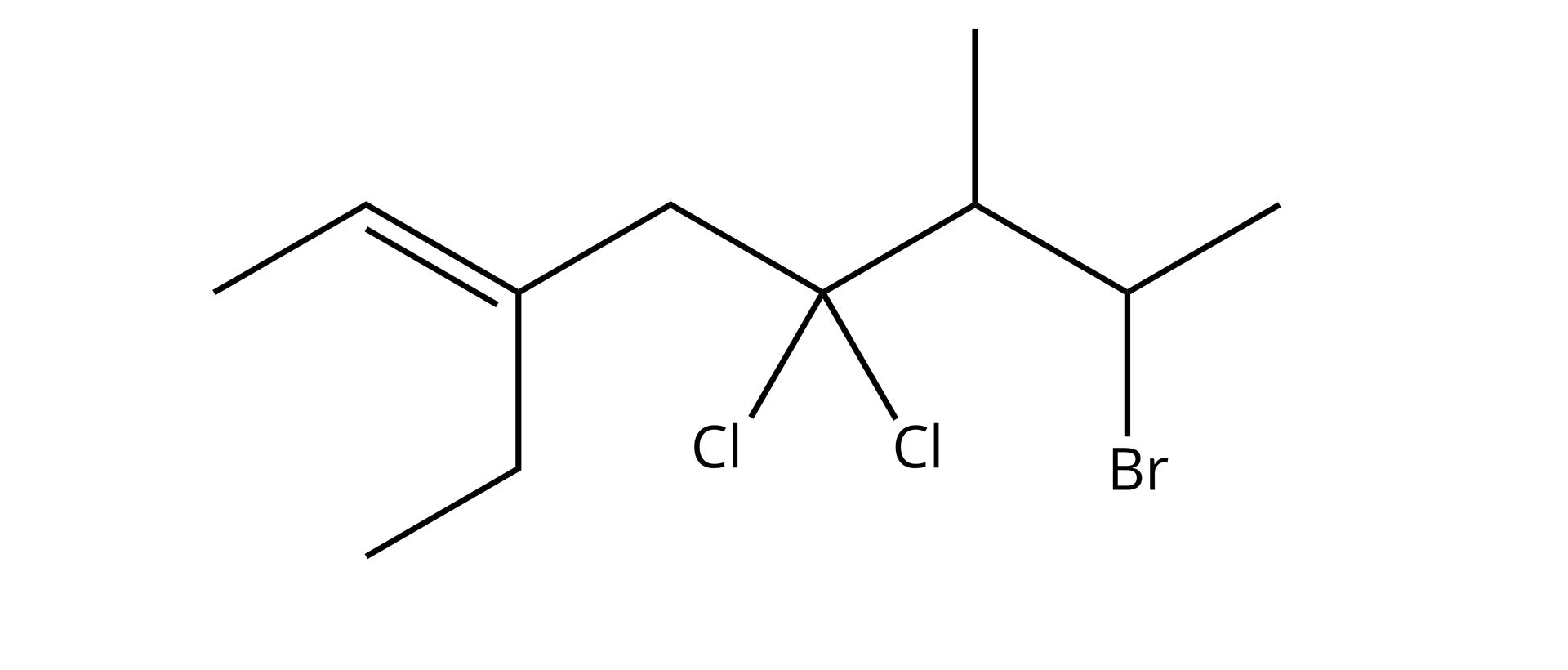
Podaj nazwę cząsteczki z uwzględnieniem izomerii geometrycznej (E/Z).
Otrzymywanie halogenków alkilowych
Halogenki alkilowe na skalę laboratoryjną otrzymać można z różnego rodzaju substratów:
z węglowodorów nasyconych (alkanów), poprzez substytucję rodnikową;
Jest to jedna z podstawowych metod otrzymywania halogenków alkilowych i znajduje zastosowanie przede wszystkim w produkcji najprostszych halogenków (głównie pochodnych metanu). Są one otrzymywane w bezpośredniej reakcji metanu z chlorem, pod wpływem działania światła lub ogrzewania. Wówczas powstaje mieszanina chlorometanu, dichlorometanu, trichlorometanu i tetrachlorometanu, rozdzielana następnie na drodze destylacji frakcjonowanej.
W przypadku alkanów o dłuższym łańcuchu węglowym, halogenowanie może prowadzić do powstania mieszanin, których nie da się tak łatwo rozdzielić. Podczas tych reakcji produkt główny powstaje na skutek podstawienia wodoru atomem fluorowca przy węglu o wyższej rzędowości.
z węglowodorów aromatycznych (arenów), poprzez substytucję elektrofilową, w obecności katalizatora;

z węglowodorów nienasyconych, poprzez addycjęaddycję do wiązań wielokrotnych;
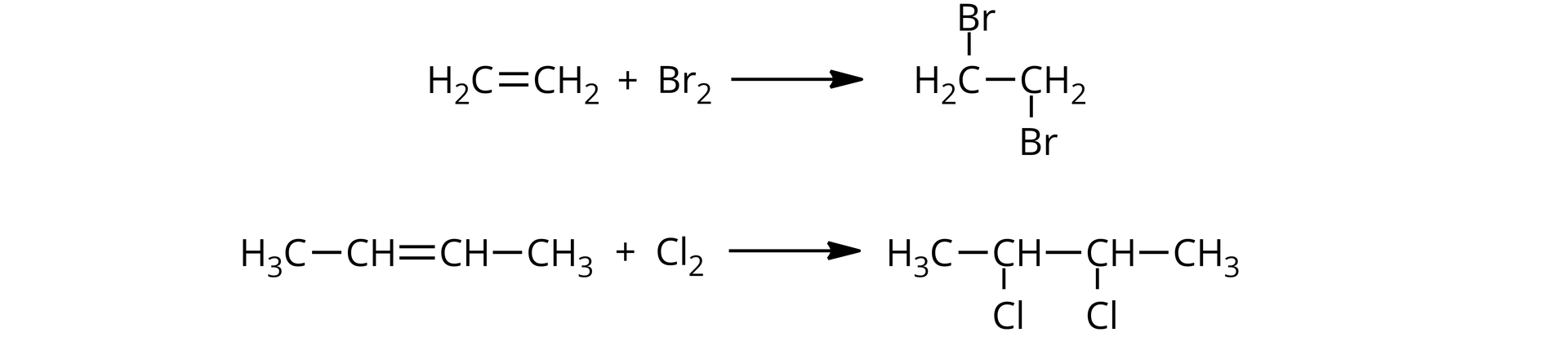
Reakcja ta umożliwia bezpośrednie otrzymywanie dihalogenopochodnych. Co więcej, może posłużyć do wykrycia obecności podwójnego wiązania węgiel‑węgiel w cząsteczce. Wymaga to zastosowania roztworu bromu (woda bromowa ma brunatną barwę), który w obecności związku nienasyconego ulega odbarwieniu.
z węglowodorów nienasyconych, poprzez addycję do wiązań wielokrotnych;
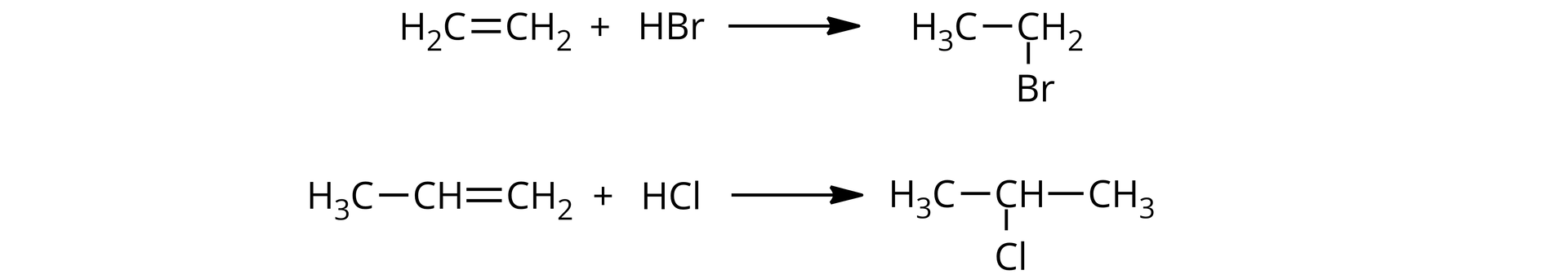
Reakcja ta przebiega zgodnie z regułą Markownikowa, określającą produkt główny reakcji – w trakcie addycji atom wodoru przyłącza się do tego atomu węgla, który jest związany z drugim wiązaniem podwójnym i gdzie jest więcej atomów wodoru, z kolei atom halogenu przyłącza się do drugiego atomu węgla przy tym wiązaniu o mniejszej ilości atomów wodoru.
z alkoholi, w reakcji substytucji nukleofilowej.
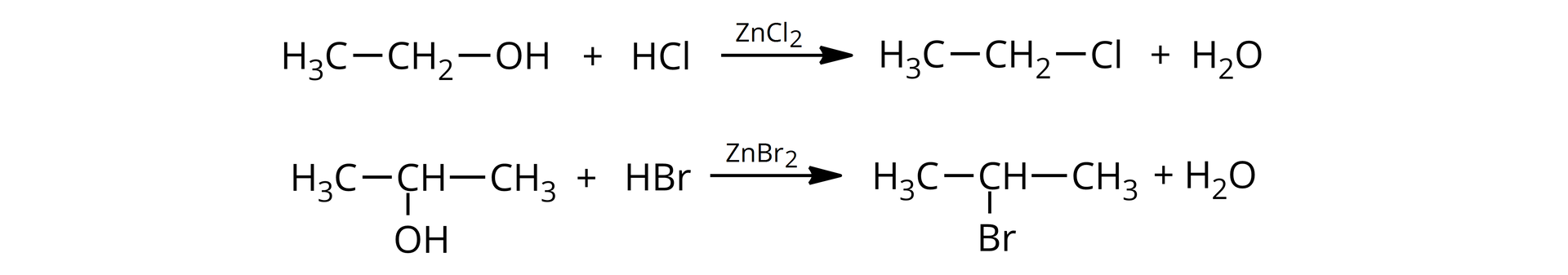
Zapoznaj się z poniższym filmem oraz wykonaj ćwiczenia pod nim zawarte, aby utrwalić metody otrzymywania fluorowcopochodnych.
Czy wiesz, w jaki sposób można otrzymać fluorowcopochodne węglowodorów? Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/RWmCascam1DcR
Film przedstawiający metody otrzymywania fluorowcopochodnych węglowodorów.
Zaprojektuj ciąg reakcji chemicznych, w wyniku których z but--ynu otrzymasz:
a) -bromobutan;
b) ,-dibromobutan;
c) ,-dibromobutan;
d) ,,-tribromobutan;
e) ,,,-tetrabromobutan;
f) ,-dibromobutan.
Zapisz odpowiednie równania reakcji, uwzględniając warunki prowadzenia poszczególnych reakcji.
C H indeks dolny trzy koniec indeksu dolnego, wiązanie pojedyncze C H indeks dolny dwa koniec indeksu dolnego, wiązanie pojedyncze C H wiązanie podwójne C H indeks dolny dwa koniec indeksu dolnego plus 1. C H indeks dolny trzy koniec indeksu dolnego, wiązanie pojedyncze C H indeks dolny dwa koniec indeksu dolnego, wiązanie pojedyncze C H B r, wiązanie pojedyncze C H indeks dolny trzy koniec indeksu dolnego, 2. H B r, 3. C H indeks dolny trzy koniec indeksu dolnego, wiązanie pojedyncze C H indeks dolny dwa koniec indeksu dolnego, wiązanie pojedyncze C H wiązanie podwójne C H indeks dolny dwa koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego strzałka w prawo 1. C H indeks dolny trzy koniec indeksu dolnego, wiązanie pojedyncze C H indeks dolny dwa koniec indeksu dolnego, wiązanie pojedyncze C H B r, wiązanie pojedyncze C H indeks dolny trzy koniec indeksu dolnego, 2. H B r, 3. C H indeks dolny trzy koniec indeksu dolnego, wiązanie pojedyncze C H indeks dolny dwa koniec indeksu dolnego, wiązanie pojedyncze C H wiązanie podwójne C H indeks dolny dwa koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego
Zapoznaj się z poniższym tekstem, a następnie rozwiąż zadanie.
Właściwości fizyczne halogenopochodnych węglowodorów
Pojawienie się jednej grupy funkcyjnej w związkach chemicznych w bardzo znaczącym stopniu wpływa na właściwości fizyczne, takie jak: temperatura topnienia i wrzenia, gęstość czy moment dipolowy. Przeanalizuj dane w poniższej tabeli oraz spróbuj wykonać polecenie pod nią.
Tabela 1. Właściwości fizyczne wybranych węglowodorów i halogenopochodnych
Nazwa związku | Wzór związku | Temperatura wrzenia, , | Gęstość cieczy , |
metan | gaz | ||
jodometan | |||
bromometan | gaz | ||
chlorometan | gaz | ||
dichlorometan | |||
trichlorometan | |||
tetrachlorometan | |||
etan | gaz | ||
chloroetan | gaz | ||
bromoetan | |||
jodoetan | |||
propan | gaz | ||
1‑chloropropan | |||
1‑bromopropan | |||
1‑jodopropan | |||
butan | gaz | ||
‑chlorobutan | |||
‑bromobutan | |||
‑jodobutan | |||
pentan | |||
‑chloropentan | |||
‑bromopentan | |||
‑jodopentan | |||
benzen | |||
chlorobenzen | |||
bromobenzen | |||
jodobenzen |
Indeks górny Źródło: Czerwińska A., Czerwiński A., i in., Chemia – podręczniki dla liceum ogólnokształcącego, profilowanego i technikum. Zakres rozszerzony, Warszawa 2019. Indeks górny koniecŹródło: Czerwińska A., Czerwiński A., i in., Chemia – podręczniki dla liceum ogólnokształcącego, profilowanego i technikum. Zakres rozszerzony, Warszawa 2019.
Porównaj temperatury wrzenia poszczególnych związków z ich masami molowymi. Czy widzisz jakąś korelację pomiędzy tymi wielkościami?