Alkohole monohydroksylowe - budowa nazewnictwo i otrzymywanie
Alkohole
Alkohole to związki, które zawierają grupę funkcyjną –OH, związaną z tetraedrycznym (w stanie hybrydyzacji ) atomem węgla.

Budowa i podział alkoholi
R‑OH to ogólny wzór alifatycznych alkoholi monohydroksylowych. Cząsteczka alkoholu zawiera hydrofilową grupę -OH i hydrofobową resztę węglowodorową -R (wyjątkiem jest metanol, który posiada grupę metylową ). Wśród alkoholi alifatycznych łańcuchowych możemy wyróżnić, np. alkohole monohydroksylowe, będące pochodnymi:
alkanów o wzorze ogólnym ;
alkenów o wzorze ogólnym ;
alkinów o wzorze ogólnym .
Alkohole można też traktować jako pochodne wody. W tym ujęciu zakładamy, że jeden z atomów wodoru w cząsteczce wody został zastąpiony grupą węglowodorową R.
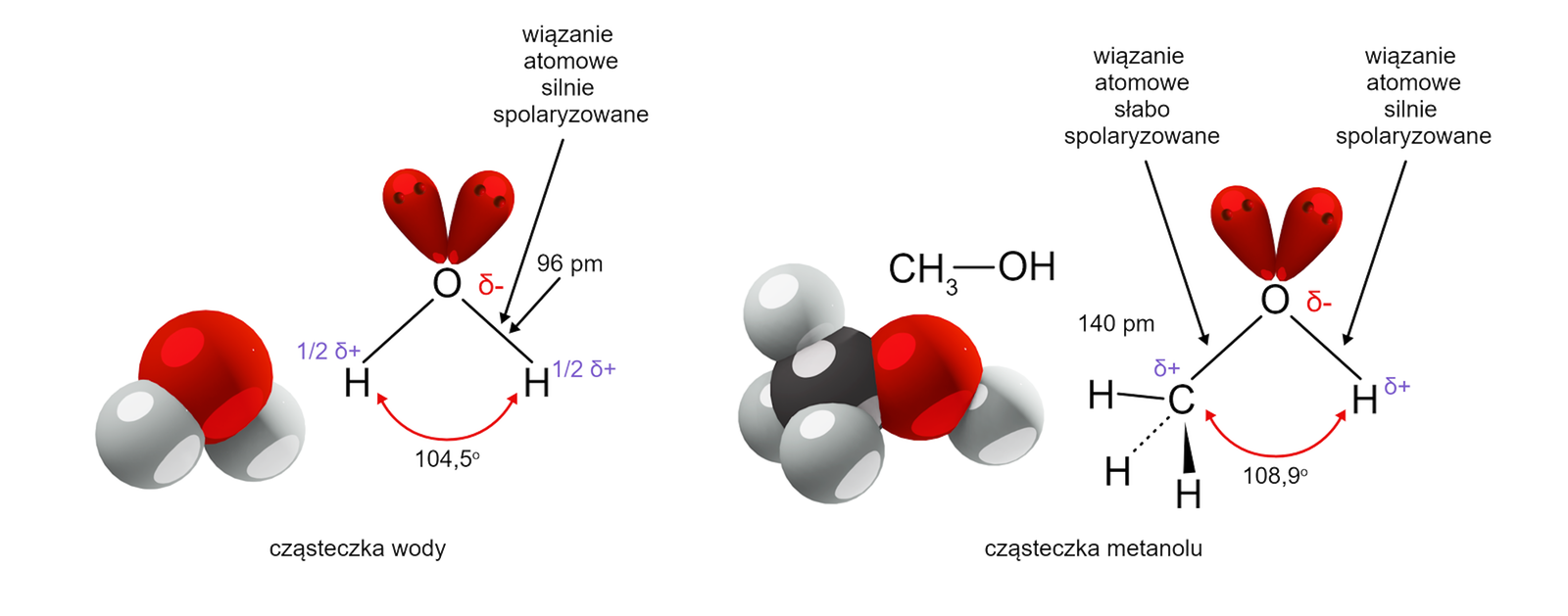
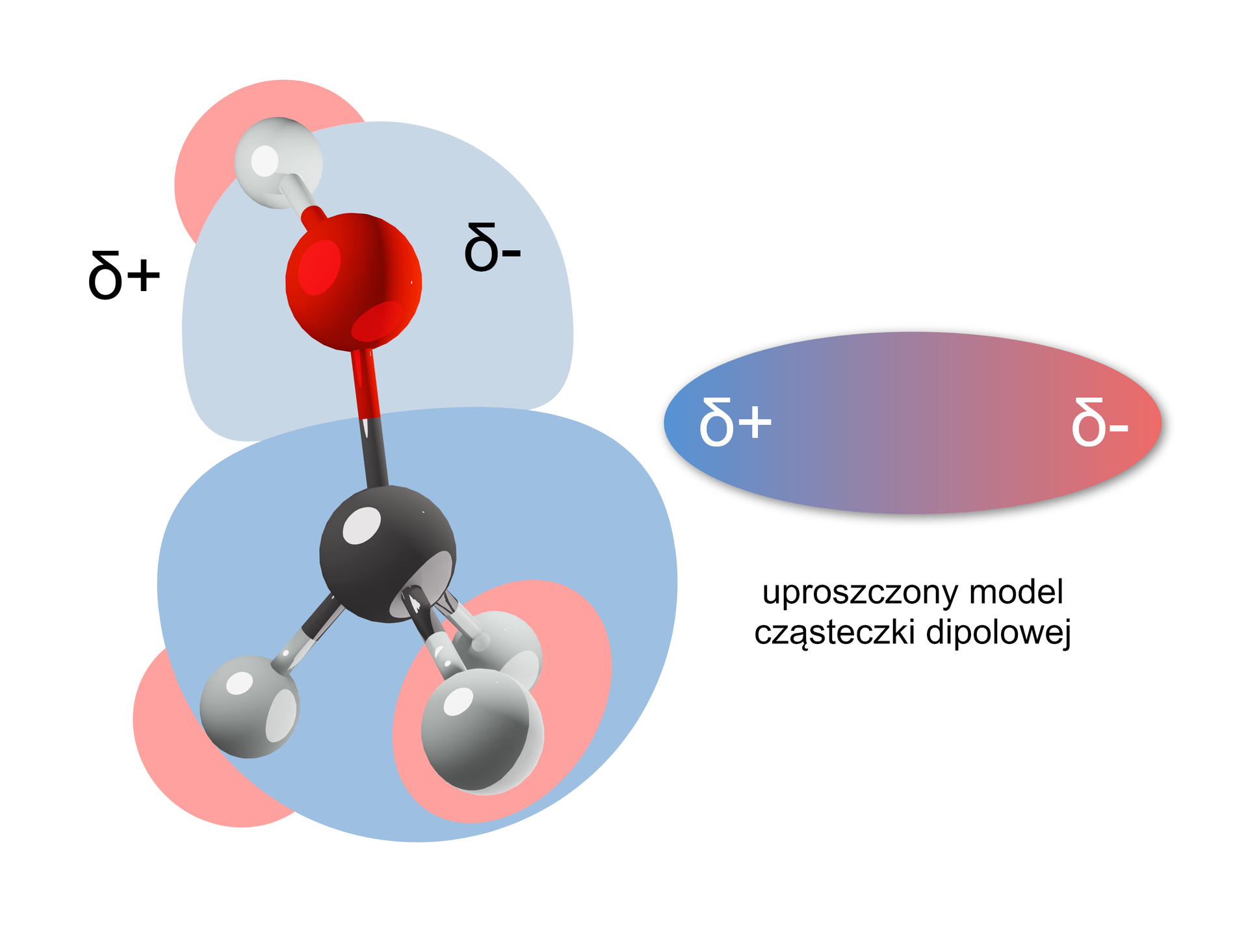
Obecność silnie spolaryzowanego wiązania determinuje właściwości fizyczne i chemiczne alkoholi. Silna polaryzacja wiązania sprawia, że cząsteczki alkoholi są dipolami.
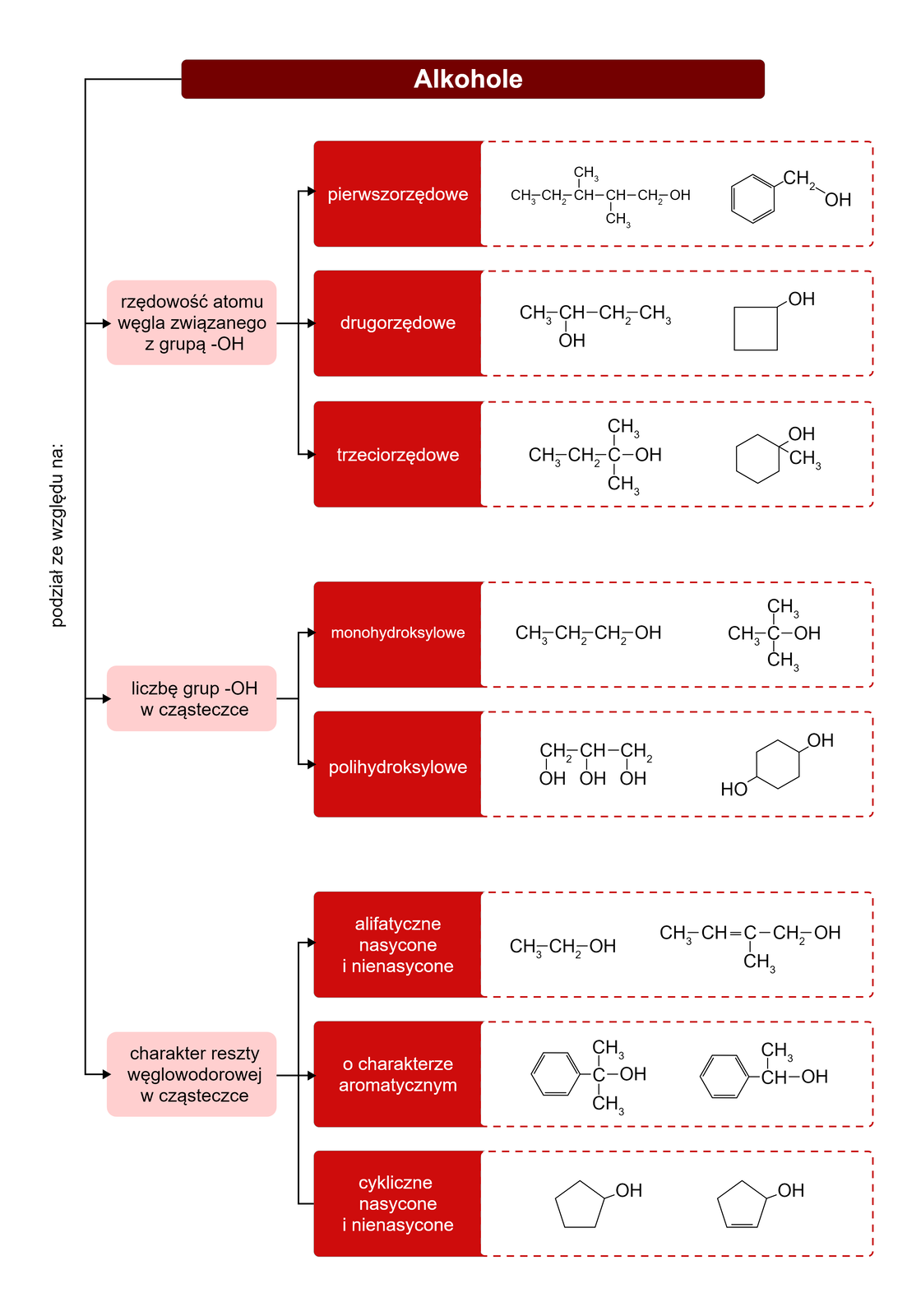
Alkohole są zróżnicowane pod względem budowy. Przykładowa klasyfikacja obejmuje te, które zawierają również reszty węglowodorowe o charakterze aromatycznym.
Czy wiesz, jak zbudowane są alkohole? Zapoznaj się z przedstawioną poniżej symulacją interaktywną dotyczącą budowy alkoholi, a następnie rozwiąż ćwiczenia.
Czy wiesz jak zbudowane są alkohole? Zapoznaj się z opisem symulacji interaktywnej dotyczącej budowy alkoholi a następnie rozwiąż ćwiczenia.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCZJTXPLJ
Nazewnictwo alkoholi
Budowa cząsteczek alkoholi decyduje o sposobie ich nazewnictwa, dlatego w tej części tematu omówione zostaną odpowiednie zasady. Zapoznaj się z poleceniem 1 i rozwiąż zawarte pod nim ćwiczenia.
Zapoznaj się z filmem samouczkiem. Czy wiesz, w jaki sposób tworzy się nazwy alkoholi w oparciu o ich wzór strukturalny?

Film dostępny pod adresem /preview/resource/REsecmmG6lrM0
Film nawiązujący do treści materiału dotyczącej tworzenia nazw i wzorów cząsteczek alkoholi.
Podaj nazwy związków, których wzory podano poniżej.

Otrzymywanie alkoholi monohydroksylowych
Poniżej przedstawiono mapę obrazującą metody otrzymywania alkoholi, które zostaną omówione w dalszej części tego materiału.
- Nazwa kategorii: metody otrzymywania alkoholi{value=26}
- Nazwa kategorii: metody naturalne{value=18}
- Nazwa kategorii: fermentacjaalkoholowacukrów{value=16}
- Nazwa kategorii: suchadestylacjawęgla(piroliza){value=16} Koniec elementów należących do kategorii metody naturalne{value=18}
- Nazwa kategorii: metody przemysłowe{value=18}
- Nazwa kategorii: addycjawody doalkenów{value=16}
- Nazwa kategorii: syntezaz użyciemgazusyntezowego{value=16} Koniec elementów należących do kategorii metody przemysłowe{value=18}
- Nazwa kategorii: metody laboratoryjne{value=18}
- Nazwa kategorii: reakcjeredukcji{value=16}
- Nazwa kategorii: aldehydów{value=12}
- Nazwa kategorii: ketonów{value=12}
- Nazwa kategorii: kwasówkarboksylowych{value=12}
- Nazwa kategorii: estrów{value=12} Koniec elementów należących do kategorii reakcje[br]redukcji{value=16}
- Elementy należące do kategorii metody otrzymywania alkoholi{value=26}
- Elementy należące do kategorii metody naturalne{value=18}
- Elementy należące do kategorii metody przemysłowe{value=18}
- Elementy należące do kategorii metody laboratoryjne{value=18}
- Elementy należące do kategorii reakcjeredukcji{value=16}
Fermentacja alkoholowa
Jednym z najprostszych alkoholi, dobrze nam znanym, jest etanol (). Można go otrzymać poprzez fermentację alkoholową skrobi, zawartą w ziemniakach lub innych bogatych w cukry (glukozę, sacharozę) surowców, np. owoców:
Sucha destylacja drewna
Metanol często otrzymuje się za pomocą pirolizy drewna (sucha destylacja). Polega to na rozkładzie drewna w warunkach beztlenowych poprzez ogrzewanie z zewnątrz do temperatury . Należy wyróżnić kilka etapów wykonywanej czynności. Niektóre z nich zostały przedstawione w tabeli poniżej.
Etap | Temperatura | Produkty |
|---|---|---|
głównie woda | ||
‑ | tlenek węgla() i tlenek węgla() | |
‑ | kwas octowy, metanol, smoła oraz węglowodory | |
‑ | węglowodory i wodór |
Metody przemysłowe
Metanol w przemyśle syntezuje się przy użyciu mieszaniny wodoru cząsteczkowego i tlenku węgla() , czyli tzw. gazu syntezowego. Reakcja zachodzi przy użyciu katalizatora i pod wpływem działania wysokiej temperatury oraz ciśnienia.
Gaz syntezowy powstaje podczas reakcji węgla, gazu ziemnego lub lekkich węglowodorów (głównie metanu) z parą wodną w obecności katalizatorów. Katalityczna konwersja metanu parą wodną zachodzi zgodnie z poniższym równaniem reakcji:
Addycja elektrofilowa alkenów
Poza tym w przemyśle na dużą skalę alkohole otrzymuje się w reakcji przyłączania wody do alkenów (addycja elektrofilowa do podwójnego wiązania). Dla przykładu, etanol otrzymuje się z etylenu (etenu) w bardzo kwaśnym środowisku:
Oprócz powyższych specyficznych metod w laboratorium, stosuje się poniżej wymienione metody otrzymywania alkoholi.
Substytucja nukleofilowa halogenków alkilowych z mocnymi zasadami w środowisku wodnym
Halogenki alkilowe są elektrofilami, zatem reagują z nukleofilami i zasadami. W powyższej reakcji substytucji nukleofilowej nukleofil () wypycha elektrony wiązania () w halogenku alkilowym w kierunku grupy opuszczającej (), co prowadzi do rozerwania wiązania i odejścia anionu chlorkowego. Reaktywność halogenków alkilowych zależy od właściwości grupy opuszczającej. Ogólnie najsłabsze zasady, czyli aniony najsilniejszych kwasów, są najlepszymi, najbardziej reaktywnymi grupami opuszczającymi. Szczególnie aktywne w tym procesie są bromo- i jodoalkany. Chloroalkany reagują stosunkowo trudno, natomiast fluoroalkany są bardzo mało reaktywne, ponieważ anion fluorkowy tworzy słabe kwasy.
Spróbuj przeprowadzić syntezę alkoholu w poniższym wirtualnym laboratorium, a następnie rozwiąż ćwiczenia.
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz również obserwacje, i wyniki, a następnie sformułuj wnioski. Określ typy zachodzących reakcji. Czy reakcja z azotanem() srebra() umożliwia potwierdzenie przebiegu reakcji chloroetanu oraz -chloropropanu z wodorotlenkiem sodu? Porównaj swoje obserwacje z zapisem równań reakcji dostępnych w e‑lekcji.
Zapoznaj się z opisem doświadczenia, a następnie rozwiąż zadania.
Analiza doświadczenia: Reakcje otrzymywania alkoholi.
Problem badawczy: Czy w reakcji halogenku alkilowego z wodorotlenkiem sodu można jako produkt otrzymać alkohol?
Hipoteza: W reakcji chlorku alkilowego z wodorotlenkiem sodu można otrzymać alkohol.
Sprzęt laboratoryjny:
probówki – podłużne naczynia szklane służące do przeprowadzania prostych reakcji chemicznych;
statyw – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
drewniana łapa – rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej;
łaźnia wodna – naczynie wypełnione wodą, służące do ogrzewania lub schładzania innych naczyń laboratoryjnych wraz z ich zawartością;
łaźnia lodowa – naczynie wypełnione lodem, służące do schładzania innych naczyń laboratoryjnych wraz z ich zawartością;
pipeta Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Potrzebne odczynniki:
chloroetan; chloropropan; wodorotlenek sodu; azotan() srebra().
Przebieg doświadczenia:
Wybrano jeden z chlorków, dodano do probówki około dwa centymetry sześcienne.
Następnie dodano taką samą ilość .
Probówkę z -chloropropanem ogrzano w łaźni wodnej, a probówkę z chloroetanem schłodzono w łaźni lodowej.
Do otrzymanego roztworu substancji dodano kilka kropli roztworu azotanu() srebra().
Obserwacje:
Po dodaniu roztworu wodorotlenku sodu do probówki zawierającej -chloropropan lub chloroetan zaobserwowano, że tworzą się dwie warstwy cieczy. W wyniku ogrzania probówki z -chloropropanem w łaźni wodnej oraz schłodzenia probówki zawierającej chloroetan w łaźni lodowej, z dwóch warstw cieczy tworzy się jedna. Dodanie wodnego roztworu azotanu() srebra() do obydwóch uzyskanych wcześniej roztworów prowadzi do wytrącenia się białego osadu.
Wyniki:
Reakcja -chloropropanu lub chloroetanu z wodorotlenkiem sodu to reakcja substytucji nukleofilowej, w wyniku której powstaje odpowiedni alkohol oraz chlorek sodu, , który posiada budowę jonową. W przypadku chloroetanu otrzymanym alkoholem jest etanol, a w przypadku -chloropropanu – propan--ol.
Dodanie azotanu() srebra() do produktów tych reakcji prowadzi wytrącenia się białego osadu nierozpuszczalnej soli . Jest to reakcja strącania.
Wnioski:
Alkohole można otrzymywać z fluorowcoalkanów w reakcji substytucji nukleofilowej. Hipoteza została potwierdzona.
Narysuj wzory półstrukturalne produktów poniższych reakcji.

Zapisz wzory produktów poniższych reakcji.
Zaproponuj wzory związków chemicznych, które można wykorzystać do syntezy poniższych alkoholi. Podaj nazwę zastosowanej metody oraz oceń, czy dany alkohol został otrzymany zgodnie z regułą Markownikowa – wyjaśnij dlaczego.



