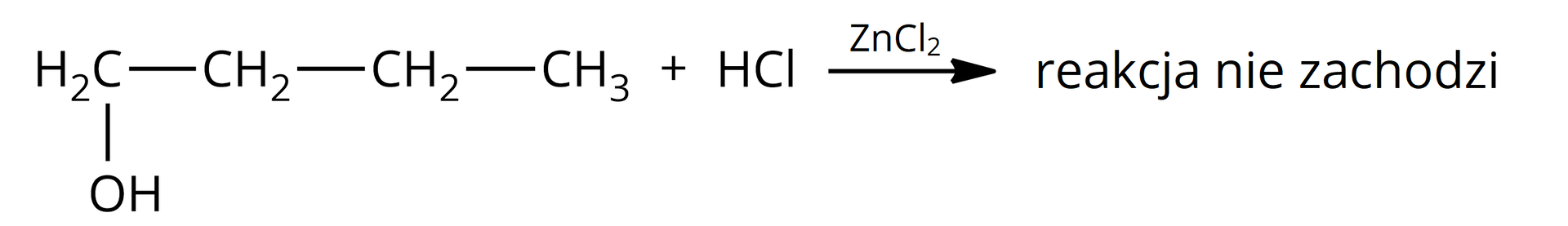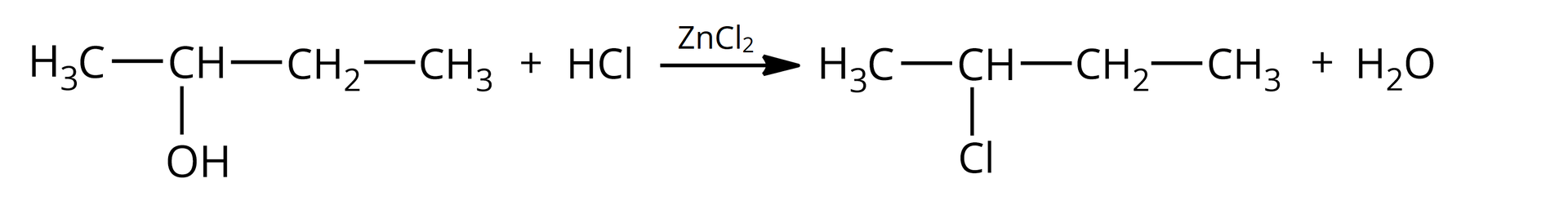Alkohole monohydroksylowe - właściwości
Właściwości chemiczne alkoholi monohydroksylowych
W tej części podręcznika zostaną omówione właściwości chemiczne alkoholi monohydroksylowych oraz reakcje, którym ulegają te związki organiczne.
Spalanie alkoholi monohydroksylowych
Wszystkie alkohole są substancjami łatwopalnymi i spalają się w zależności od dostępności tlenu do tlenku węgla, tlenku węgla lub sadzy oraz wody.
Spalanie całkowite to reakcja z tlenem, w wyniku której powstaje tlenek węgla i woda. Nasycone alkohole monohydroksylowe spalają się zgodnie ze schematycznym zapisem reakcji spalania całkowitego:
Półspalanie to reakcja z tlenem, w wyniku której powstaje tlenek węgla i woda. Półspalanie zachodzi w warunkach niedoboru tlenu. Nasycone alkohole monohydroksylowe spalają się zgodnie ze schematycznym zapisem reakcji półspalania:
Spalanie niecałkowite to reakcja z tlenem, w wyniku której powstaje sadza i woda. Spalanie niecałkowite zachodzi przy niedostatecznym dostępie tlenu do spalanej substancji. Nasycone alkohole monohydroksylowe spalają się zgodnie ze schematycznym zapisem reakcji spalania niecałkowitego:
Zapoznaj się z poleceniem 1, aby sprawdzić rozumienie i przećwiczyć reakcje spalania.
Jak dobrze znasz reakcje spalania alkoholi? Zdobądź skarb znajdujący się w sejfie. Aby to zrobić, trzeba uzyskać -cyfrowy kod, który umożliwi złamanie zabezpieczenia. Gra polega na uzupełnieniu współczynników stechiometrycznych w reakcjach spalania alkoholi.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBFBRO694
Reakcje spalania alkoholi
Test dotyczy reakcji spalania alkoholi. Sprawdź swoją dotychczasową wiedzę zdobytą po zapoznaniu się z materiałami zawartymi w lekcji. Masz minut na rozwiązanie testu składającego się z pytań jednokrotnego wyboru. Powodzenia!
Napisz reakcje spalania całkowitego i niecałkowitego oktan--olu.
Reakcja alkoholi z sodem
Alkohole () nie ulegają dysocjacji elektrolitycznej, a odczyn ich roztworów wodnych jest obojętny. Cząsteczka alkoholu zawiera atom wodoru połączony z silnie elektroujemnym atomem tlenu (grupa hydroksylowa, ). Różnica wartości elektroujemności pomiędzy atomem tlenu () a atomem wodoru () sprawia, że kowalencyjne wiązanie jest spolaryzowane w kierunku atomu tlenu, co umożliwia oderwanie się wodoru w postaci kationu (). W związku z tym alkohole, mimo obojętnego odczynu roztworu, posiadają bardzo słaby charakter kwasowy. Podczas reakcji z sodem (a także potasem oraz na gorąco z wapniem i magnezem) alkohole są zdolne do utracenia kationu wodoru () i przekształcenia się w anion alkoholanowy , który elektrostatycznie oddziałuje z kationem sodu. Skoro atom sodu utlenił się do kationu sodu, to kation wodoru redukuje się do wodoru cząsteczkowego. W ten sposób z alkoholu i sodu powstaje alkoholan sodu (związek chemiczny o charakterze soli) i wodór cząsteczkowy.
W poniższym wirtualnym laboratorium można przeprowadzić doświadczenie, które pokazuje, jak alkohole reagują z sodem. Zastanawiasz się, czy alkohole monohydroksylowe oraz polihydroksylowe reagują w ten sam sposób? W tym laboratorium pracujesz z sodem, który z uwagi na swoją reaktywność przechowywany jest pod warstwą nafty. Pamiętaj, aby po wyjęciu kawałka sodu osuszyć go bibułką. Po przeprowadzeniu doświadczenia, uzupełnij poniższy formularz oraz wykonaj ćwiczenia.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBFBRO694
Poniżej opisano doświadczenie, w którym zbadano reaktywność alkoholi z sodem. Zastanawiasz się, czy alkohole monohydroksylowe oraz polihydroksylowe reagują w ten sam sposób? W laboratorium wykorzystano sód, który z uwagi na swoją reaktywność przechowywany jest pod warstwą nafty. Po wyjęciu kawałka sodu zawsze należy osuszyć go bibułką.
Analiza doświadczenia:
Badanie reakcji alkoholi z sodem.
Problem badawczy:
Czy wszystkie badane alkohole w taki sam sposób reagują z sodem?
Hipoteza:
Alkohole polihydroksylowe i monohydroksylowe reagują reagują z sodem z różną intensywnością.
Szkło i sprzęt laboratoryjny:
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości służące do odmierzania cieczy;
krystalizator – szkło laboratoryjne o walcowatym kształcie, przy czym w odróżnieniu od zlewki, podstawa krystalizatora ma dużą średnicę, zaś jego wysokość jest mała; zazwyczaj wykorzystywany jest do krystalizacji;
pęseta (szczypce) – z reguły metalowe narzędzie o sprężystych ramionach umożliwiające chwytanie niewielkich przedmiotów;
pipeta – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki:
sód, etanol, metanol, gliceryna, roztwór fenoloftaleiny.
Przebieg doświadczenia:
1. Umieszczenie w dwóch krystalizatora po centymetrów sześciennych wybranego alkoholu.
2. Dodanie do pierwszego krystalizatora kilku kropli roztworu fenoloftaleiny.
3. Wyjęcie spod warstwy nafty kawałka sodu za pomocą szczypiec oraz osuszenie go za pomocą bibuły.
4. Dodanie sodu do obu krystalizatorów.
5. Zaobserwowanie zmian oraz sprawdzenie koloru uniwersalnego papierka wskaźnikowego dla roztworu nie zawierającego fenoloftaleiny.
Obserwacje:
Dla metanolu oraz etanolu: w obu krystalizatorach: sód pływa w postaci kulki, która zmniejsza swoją wielkość – sód rozpuszcza się; wydziela się bezbarwny, bezwonny gaz. W pierwszym: roztwór z dodatkiem alkoholowego roztworu fenoloftaleiny barwi się na malinowo. W drugim: uniwersalny papierek wskaźnikowy przyjmuje niebieskie zabarwienie.
Dla gliceryny: w obu krystalizatorach sód reaguje gwałtownie i zapala się; wydziela się bezwonny oraz bezbarwny gaz. W pierwszym: roztwór z dodatkiem alkoholowego roztworu fenoloftaleiny barwi się na malinowo. W drugim: uniwersalny papierek wskaźnikowy przyjmuje niebieskie zabarwienie.
Wyniki:
Wszystkie badane alkohole reagują z sodem, w wyniku czego dochodzi do powstania związku o charakterze zasadowym i wydzielenia gazu. W przypadku gliceryny reakcja z sodem zachodzi gwałtownie – dochodzi do samozapłonu reagentów.
Wnioski:
Badane alkohole reagują z sodem, ponieważ obserwowane jest rozpuszczanie metalu. W wyniku reakcji chemicznej powstają produkty, których roztwór posiada odczyn zasadowy, ponieważ roztwór z dodatkiem alkoholowego roztworu fenoloftaleiny barwi się na malinowo, a uniwersalny papierek wskaźnikowy przyjmuje niebieskie zabarwienie. Powstającym bezbarwnym i bezwonnym gazem jest wodór. W przypadku glicerolu (alkoholu polihydroksylowego) reakcja zachodzi gwałtowniej niż w przypadku alkoholi monohydroksylowych. Hipoteza została potwierdzona.
Przeprowadzono powyższe doświadczenie chemiczne, wybierając jako badany alkohol metanol.
A. Zaznacz prawidłowe obserwacje dla reakcji zachodzącej dla tego alkoholu.
B. Zaznacz prawidłowe wnioski dla reakcji zachodzącej z udziałem metanolu.
C. Zaznacz prawidłowy zapis równania reakcji chemicznej, w której bierze udział metanol.
C. Uzupełnij poniższe równania, wstawiając wzór odpowiedniego reagenta wybranego z poniższych.
dwa C H indeks dolny, trzy, koniec indeksu dolnego, O H + dwa N a strzałka dwa 1. C H indeks dolny, trzy, koniec indeksu dolnego, O H, 2. C H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, minus, koniec indeksu górnego, 3. C H indeks dolny, trzy, koniec indeksu dolnego, O N a + H indeks dolny, dwa, koniec indeksu dolnego
Zapis jonowy skrócony reakcji hydrolizy:
1. C H indeks dolny, trzy, koniec indeksu dolnego, O H, 2. C H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, minus, koniec indeksu górnego, 3. C H indeks dolny, trzy, koniec indeksu dolnego, O N a + H indeks dolny, dwa, koniec indeksu dolnego, O strzałka 1. C H indeks dolny, trzy, koniec indeksu dolnego, O H, 2. C H indeks dolny, trzy, koniec indeksu dolnego, O indeks górny, minus, koniec indeksu górnego, 3. C H indeks dolny, trzy, koniec indeksu dolnego, O N a + O H indeks górny, minus, koniec indeksu górnego
Reakcja z HCl i HBr
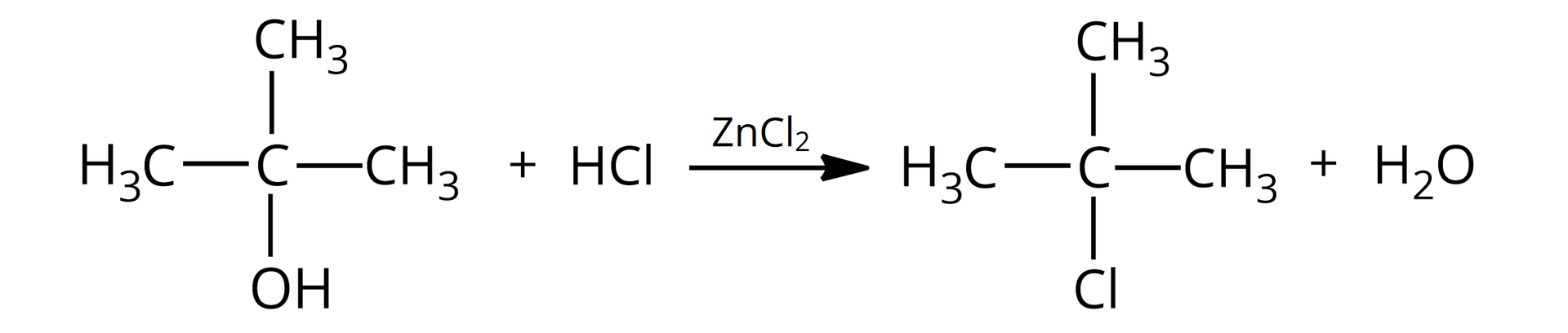
Alkohole to związki, które w swoich cząsteczkach zawierają grupę (bądź grupy) związaną z atomem węgla o hybrydyzacji . Wiązanie to jest spolaryzowane z uwagi na różnice w elektroujemności pomiędzy atomem węgla i atomem tlenu. Grupa jest grupą elektronoakceptorową, a to powoduje, że alkohole mogą ulegać reakcji substytucji nukleofilowej, np. z wodorkami fluorowców. W reakcji alkoholi z fluorowcowodorami (, ) udział bierze cała grupa hydroksylowa, która zastąpiona zostaje atomem fluorowca.
Zarówno alkohole pierwszorzędowe, jak i drugorzędowe i trzeciorzędowe, reagują z i . Alkohole wyższego rzędu łatwiej ulegają tym reakcjom z uwagi na ich większą reaktywność. W przypadku alkoholi pierwszo– i drugorzędowych konieczne bywa użycie katalizatora – i podwyższonej temperatury.
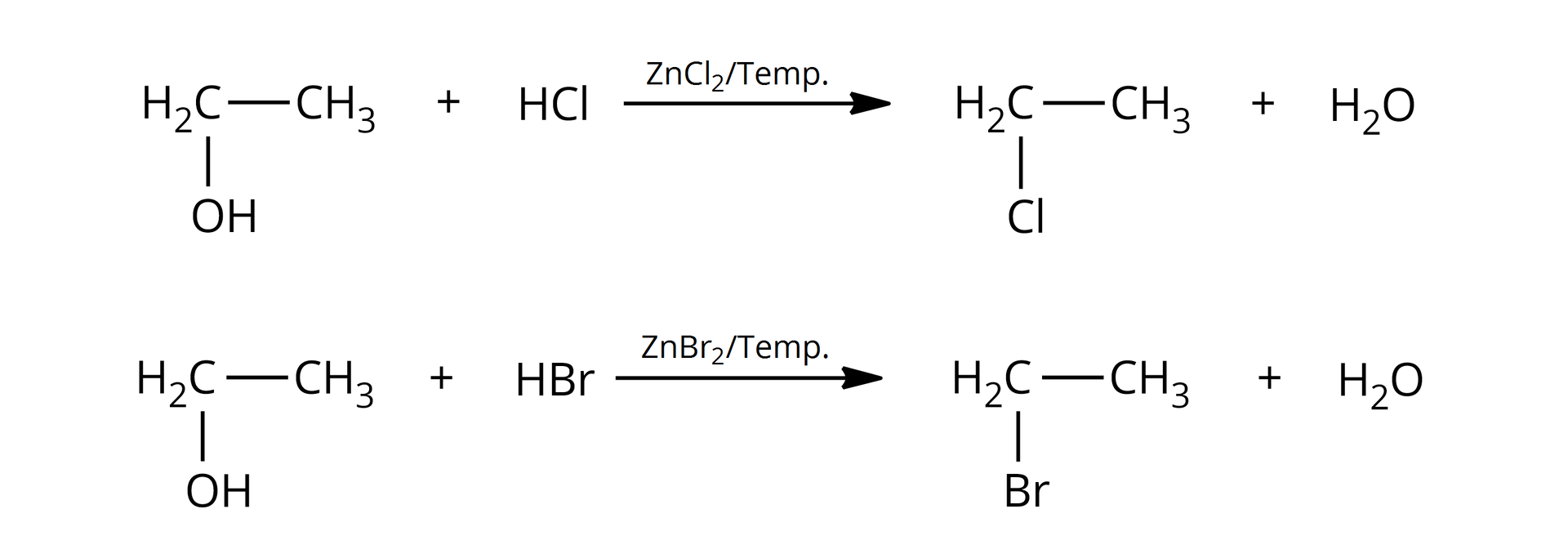
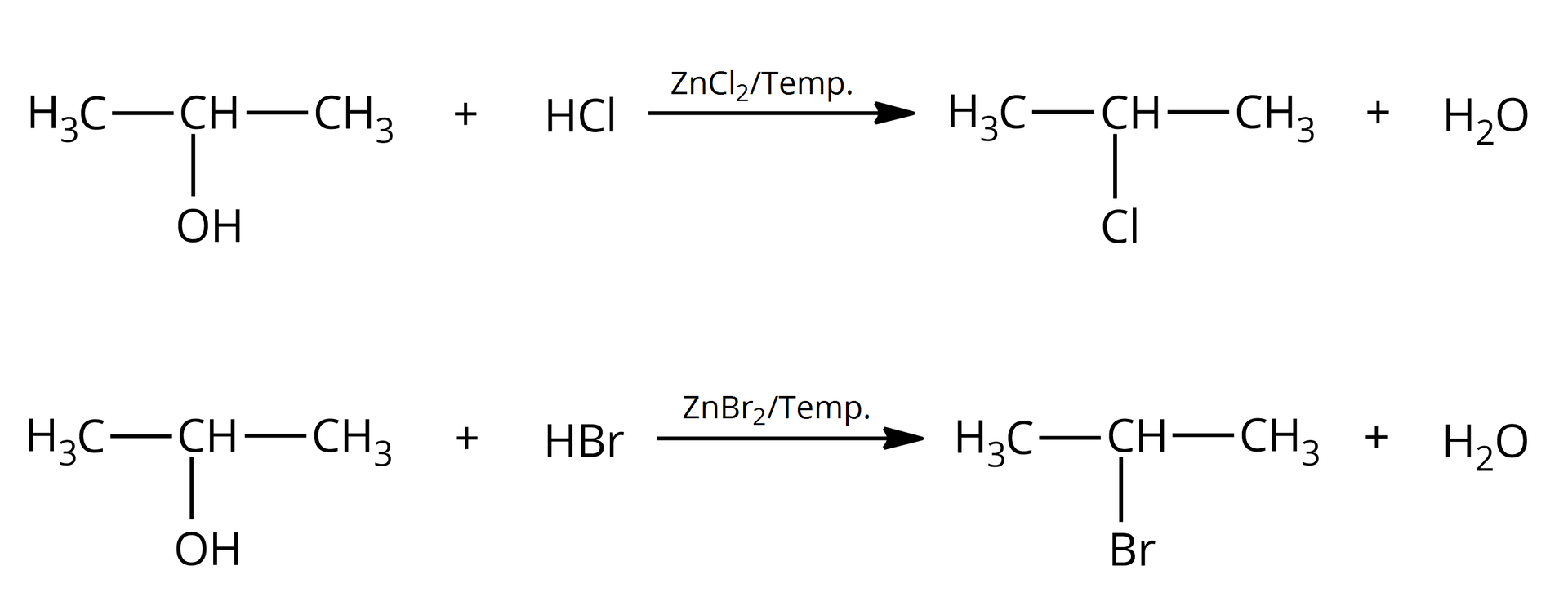
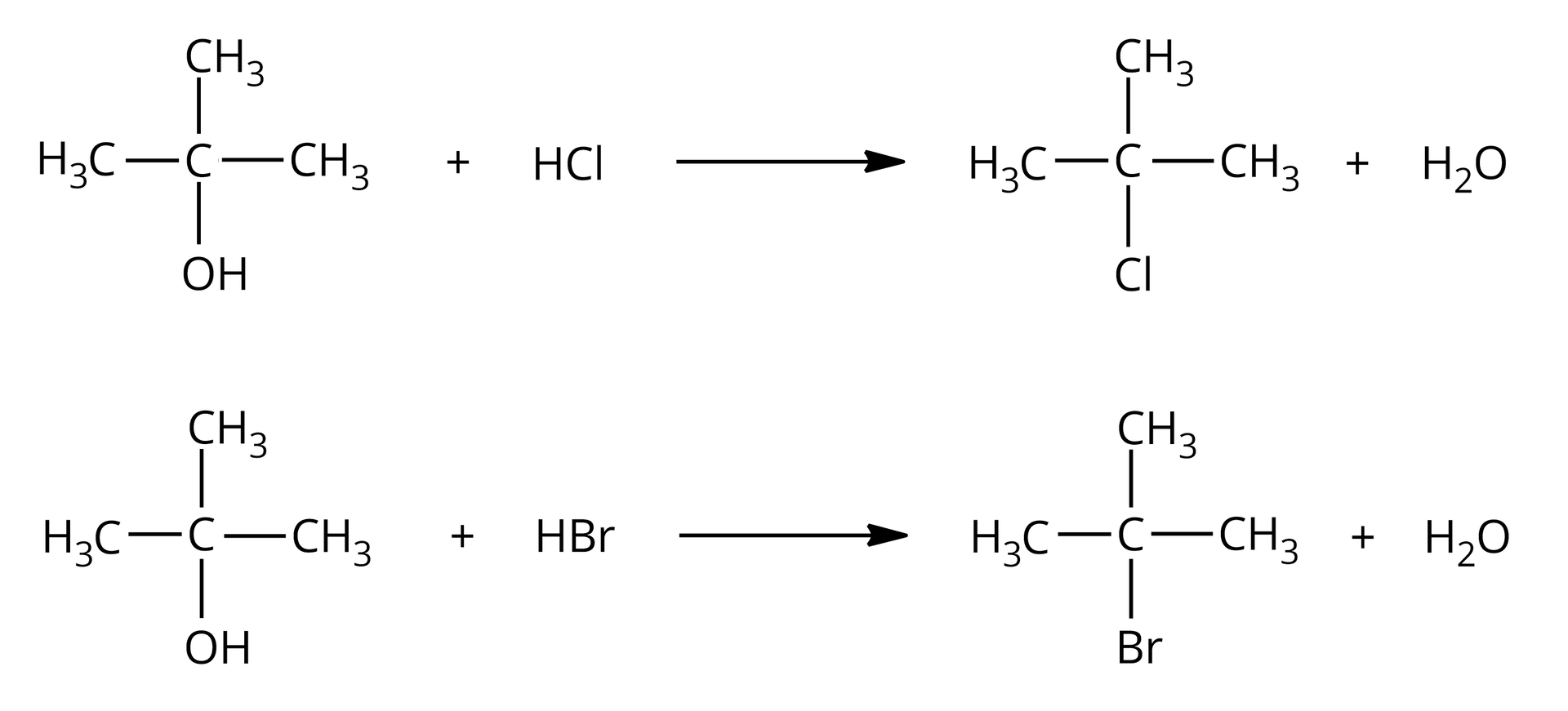
Podstawienie grupy hydroksylowej atomem fluorowca to przykład reakcji substytucji nukleofilowej, ponieważ zarówno grupa opuszczająca cząsteczkę (anion hydroksylowy, ), jak i grupa, która ją podstawia (anion chlorkowy, lub anion bromkowy, ), to nukleofile. Substytucja nukleofilowa może zachodzić zgodnie z mechanizmem jednocząsteczkowym lub dwucząsteczkowym, w zależności od rzędowości alkoholu.
Przeprowadź opisane reakcje chemiczne w poniższym laboratorum oraz rozwiąż zawaete pod nim ćwiczenie.
Korzystając z wiedzy na temat reakcji alkoholi z kwasem chlorowodorowym, zaplanuj i przeprowadź eksperyment, który pozwoli Ci rozwiązać poniższy problem badawczy. Hipotezę, obserwacje, wyniki i wnioski zanotuj w dzienniku.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBFBRO694
Przeprowadzono eksperyment, które pozwolił zbadać reakcję alkoholi z kwasem chlorowodorowym w środowisku chlorku cynku. Zapoznaj się z opisem doświadczenia i wykonaj polecenia.
Analiza eksperymentu: Badanie reakcji alkoholi z kwasem chlorowodorowym w środowisku chlorku cynku.
Problem badawczy: Jak odróżnić od siebie trzy alkohole: butan––ol, butan––ol i –metylopropan––ol.
Hipoteza: Butan––ol, butan––ol i –metylopropan––ol to alkohole o różnych rzędowościach, w związku z czym będą z różną szybkością reagowały z pod wpływem .
Sprzęt laboratoryjny:
probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
waga laboratoryjna – urządzenie elektryczne służące do wyznaczania mas substancji. Daną substancję umieszcza się na srebrnej tacy umieszczonej na urządzeniu. Masa ważonej substancji wyświetlana jest na wyświetlaczu;
naczynko wagowe – sprzęt laboratoryjny służący do dokładnego odważania substancji stałych;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
pręcik szklany, służący do mieszania cieczy;
pipeta automatyczna – jest to specjalny rodzaj pipety miarowej; posiada ona mechanizm składający się z tłoczka ze sprężynką, rączki, regulatora oraz wymiennej końcówki.
Odczynniki chemiczne:
butan––ol;
butan––ol;
–metylopropan––ol;
bezwodny chlorek cynku;
stężony roztwór kwasu chlorowodorowego.
Przebieg eksperymentu:
Przygotowany odczynnik Lucasa: a) za pomocą łyżeczki pobrano bezwodny chlorek cynku do naczynka wagowego i odważono gramów; b) odmierzono centymetrów sześciennych w cylindrze miarowym stężonego roztworu ; c) odważony bezwodny chlorek cynku przeniesiono do stężonego roztworu kwasu chlorowodorowego i zamieszano szklanym pręcikiem.
Odmierzono za pomocą pipety automatycznej po centymetra sześciennego badanych alkoholi i przeniesiono je do probówek , i .
Za pomocą pipety automatycznej do każdej z probówek dodano po centymetry sześcienne odczynnika Lucasa.
Probówki lekko wstrząśnięto.
Obserwacje:
W probówce brak objawów reakcji, w probówce zaobserwowano zmętnienie po około minutach, natomiast w probówce zmętnienie pojawiło się natychmiast.
Wyniki:
W probówce pierwszej znajduje się butan––ol, ponieważ reakcja chemiczna zaszła z tak niewielką szybkością, że nie zaobserwowano powstającego chlorku – jest to charakterystyczne dla alkoholi pierwszorzędowych.
W drugiej probówce obecny jest butan––ol, ponieważ reakcja chemiczna zaszła po pewnym czasie (zmętnienie pojawiło się po około minutach) – jest to charakterystyczne dla alkoholi drugorzędowych, które są aktywniejsze od alkoholi pierwszorzędowych.
W trzeciej probówce znajduje się –metylopropan––ol, ponieważ reakcja chemiczna zaszła natychmiast (od razu pojawiło się zmętnienie) – jest to charakterystyczne dla alkoholi trzeciorzędowych, które są najbardziej aktywne.
Wnioski:
Alkohole trzeciorzędowe są aktywniejsze w reakcji substytucji nukleofilowej od alkoholi drugorzędowych, które są aktywniejsze od alkoholi pierwszorzędowych. Butan––ol, butan––ol i –metylopropan––ol to alkohole o różnych rzędowościach, w związku z czym reagują z różną szybkością z kwasem chlorowodorowym – butan––ol najwolniej, butan––ol szybciej, natomiast –metylopropan––ol najszybciej.
Przyporządkuj nazwy alkoholi do obserwacji, których można dokonać po przeprowadzeniu próby Lucasa z ich udziałem.
Zjawisko kontrakcji
Czy wiesz, dlaczego po zmieszaniu wody i czystego alkoholu etylowego nie otrzymasz roztworu o objętości ? Odpowiedź na to pytanie znajdziesz w poniższym filmie. Zapoznaj się z filmem samouczkiem i wykonaj poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/RjF6bnQL3t0M7
Film nawiązujący do treści materiału dotyczącej kontrakcji objętości.
Oceń prawdziwość poniższych zdań, które próbują opisać oddziaływania występujące między cząsteczkami wody i alkoholu. Oznacz podane stwierdzenia odpowiednio jako „Prawda” lub „Fałsz”.
Przeprowadzono doświadczenie, zilustrowane poniższym schematem.
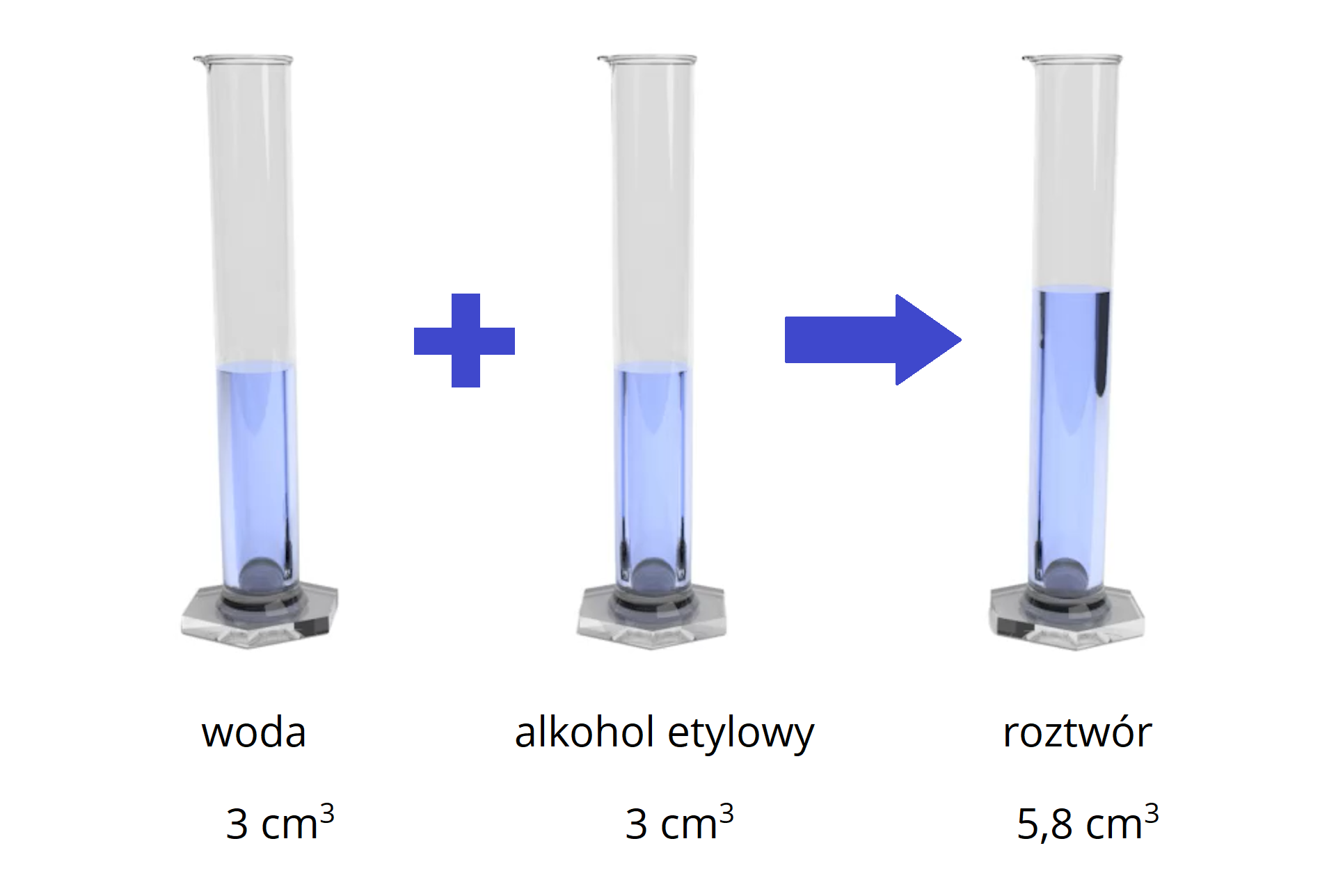
Oblicz, ile procent (w procentach objętościowych) objętości teoretycznej zajmuje objętość rzeczywista uzyskanego roztworu. Wynik zaokrąglij do drugiego miejsca po przecinku.