Aminy
Aminy
Aminy są związkami organicznymi, pochodnymi amoniaku. Mają swoją charakterystyczną grupę aminową (w przypadku amin pierwszorzędowych).
Aminy można uważać za pochodne amoniaku, w którego cząsteczce jeden, dwa lub trzy atomy wodoru zostały zastąpione resztami węglowodorowymi (alkilowymi lub/i arylowymi).

Rzędowość amin określona jest liczbą grup węglowodorowych, związanych z atomem azotu.

Właściwości fizyczne amin
Niższe alifatyczne aminy w temperaturze pokojowej są gazami dobrze rozpuszczalnymi w wodzie.

Wyższe aminy alifatyczne są cieczami lub ciałami stałymi. Cząsteczki amin pierwszo- i drugorzędowych ulegają asocjacji (pomiędzy cząsteczkami tworzą się wiązania wodorowe) i stąd aminy te mają wyższe temperatury wrzenia niż węglowodory nasycone o identycznej liczbie atomów węgla w cząsteczce.
Właściwości chemiczne amin

O zasadowym charakterze amin, podobnie jak w przypadku amoniaku, decyduje atom azotu, który, mając wolną parę elektronową, jest zdolny do przyłączenia jonów . Wniosek więc jest taki, że aminy mogą reagować z kwasami i wodą.
Aminy mają charakterystyczny rybi zapach, a niektóre, np. N‑metylometanoamina (dimetyloamina) i N,N‑dimetylometanoamina (trimetyloamina) można znaleźć w zalewie śledziowej. Wodne roztwory amin mają odczyn zasadowy.
Rzędowość amin | Przykład reakcji |
|---|---|
aminy pierwszorzędowe | |
aminy drugorzędowe | |
aminy trzeciorzędowe |
Wniosek: w czasie rozpuszczania aminy w wodzie następuje wzrost stężenia jonów , powstaje zasada amoniowa.
Aminy mają charakter zasadowy, więc reagują z kwasami, np.:
Rzędowość amin | Przykład reakcji |
|---|---|
aminy pierwszorzędowe | |
aminy drugorzędowe | |
aminy trzeciorzędowe |
Wniosek: w reakcji amin z powstają odpowiednie chlorowodorki, np. chlorowodorek metyloaminy – . Jest to związek o budowie jonowej (typu soli): .
Aminy alifatyczne są silniejszymi zasadami od amoniaku. Ich zasadowość rośnie wraz ze wzrostem rzędowości.

Zwiększona w porównaniu z amoniakiem zasadowość jest skutkiem efektu indukcyjnego grup alkilowych, które odpychają elektrony w kierunku atomu azotu. Należy pamiętać, że każdy czynnik (podstawniki, elektroujemne atomy itp.) „angażujący” wolną parę elektronową atomu azotu, osłabia zasadowość związku, a każdy czynnik „dopychający” elektrony w kierunku atomu azotu – zwiększa zasadowość.
Czy wiesz, jak zbudowane są aminy? Dowiesz się tego w poniższej symulacji. Następnie sprawdź, czy wszystko zostało zapamiętane i rozwiąż zadania.

Film dostępny pod adresem /preview/resource/R14eoUzh4UFBF
Film nawiązujący do treści materiału dotyczącej budowy amin.
Otrzymywanie amin
Zapoznaj się z animacją dotyczącą amin alifatycznych, z zawartymi informacjami, a następnie rozwiąż ćwiczenia.
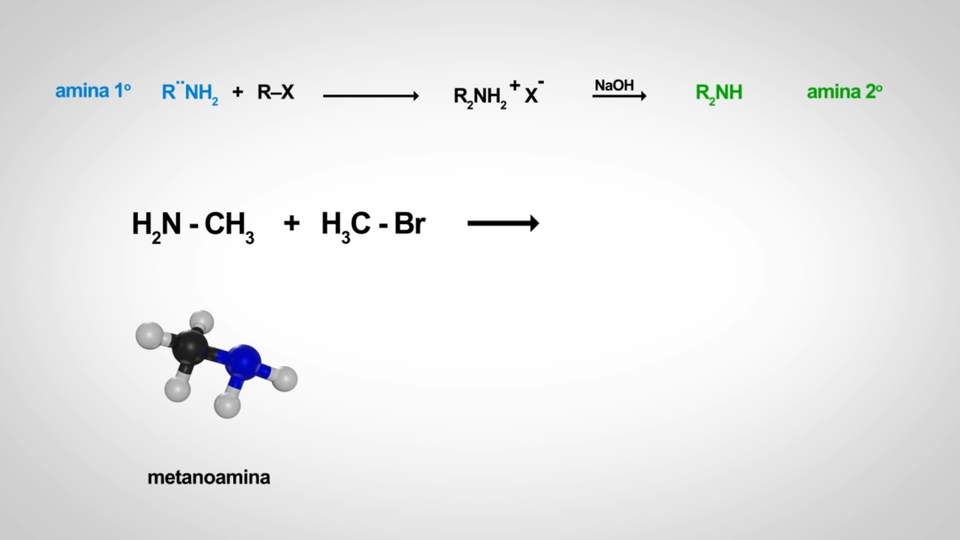
Film dostępny pod adresem /preview/resource/R6lhPfvNnD6eW
Animacja stanowi przegląd metod otrzymywania amin alifatycznych.
Wyjaśnij, dlaczego stosowany jest nadmiar amoniaku w reakcji z halogenkiem alkilu?
Zastanawiałeś się kiedyś, w jaki sposób otrzymuje się aminy aromatyczne i dlaczego stosuje się inne metody niż w przypadku amin alifatycznych?

Film dostępny pod adresem /preview/resource/Rq9uQoQmJabZp
Animacja dotyczy metod otrzymywania amin alifatycznych.