Kwasy karboksylowe - budowa i otrzymywanie
Budowa kwasów karboksylowych
Kwasy karboksylowe to związki organiczne, w których atom wodoru związku został zastąpiony grupą karboksylową , na którą składa się grupa karbonylowa oraz hydroksylowa .

R – atom wodoru, grupa alkilowa bądź arylowa
Ze względu na swoją budowę, możemy podzielić kwasy karboksylowe na kilka grup.
Alifatyczne kwasy karboksylowe
Alifatyczne kwasy karboksylowe, inaczej nazwane są kwasami łańcuchowymi bądź acyklicznymi. W cząsteczkach tego kwasu grupa karbonylowa jest połączona z łańcuchem węglowodorowym.
Aromatyczne kwasy karboksylowe
Aromatyczne kwasy karboksylowe to kwasy, w których grupa karboksylowa jest bezpośrednio połączona z pierścieniem aromatycznym grupą arylową.
Polikarbonylowe i polihydroksylowe kwasy karboksylowe
Wielokarboksylowe (polikarboksylowe) kwasy karboksylowe to związki, w których występują co najmniej dwie grupy karboksylowe. W kwasach polihydroksylowych występuje więcej niż jedna grupa hydroksylowa.
Nomenklatura kwasów karboksylowych
Wspomniany we wstępie kwas etanowy (kwas octowy) zawiera w swojej strukturze dwa atomy węgla. Poniżej przedstawiony jest jego wzór półstrukturalny.
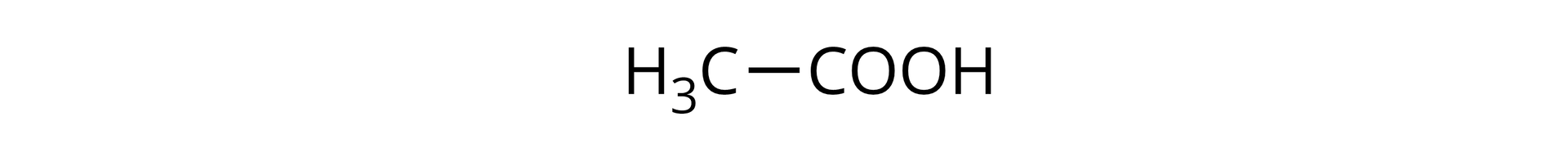
IUPAC wskazuje cztery nazwy zachowane, zalecane do stosowania przy nazewnictwie czterech kwasów i ich pochodnych.

Nazwy kwasów karboksylowych tworzymy w następujący sposób:
podajemy wyraz „kwas”;
podajemy nazwę (w mianowniku) węglowodoru, który zawiera w cząsteczce tyle samo atomów węgla, co kwas (wg zasad obowiązujących dla węglowodorów);
jeśli w cząsteczce znajdują się podstawniki, to wymieniamy je na początku nazwy wraz z lokantamilokantami w kolejności alfabetycznej;
numerację łańcucha węglowego rozpoczynamy od atomu węgla grupy karboksylowej;
podajemy końcówkę „owy”, którą poprzedzamy przedrostkiem „di-”, jeżeli w cząsteczce występują dwie grupy karboksylowe (wtedy do nazwy węglowodoru dodajemy końcówkę „o”).
Nazwy kwasów karboksylowych o budowie cyklicznej tworzymy w następujący sposób:
podajemy wyraz „kwas”;
podajemy nazwę węglowodoru, poprzedzoną nazwą podstawników wraz z ich lokantami (przy czym atomu węgla grupy nie uwzględnia się w numeracji, dlatego jest traktowany jako podstawnik, a atom węgla, do którego jest przyłączona grupa , ma nr );
dodajemy łącznik „o”;
podajemy wyraz „karboksylowy” (w przypadku dwóch, trzech grup podajemy przed końcówką „karboksylowy” lokant każdej grupy i przedrostek „di-”, „tri-”, …).
W przypadku pojawienia się większej liczby grup karboksylowych w kwasach łańcuchowych, stosujemy podobną zasadę nazewnictwa, jak w przypadku kwasów o budowie cyklicznej. Zatem grupy karboksylowe niejako „wypadają” z łańcucha głównego, a ich obecność wskazuje się przyrostkiem „karboksylowy”, jak na poniższym przykładzie.

Znając nazwę kwasu karboksylowego, z łatwością możemy podać jego wzór półstrukturalny i strukturalny. Zaczynamy zawsze od narysowania łańcucha węglowego.
Narysuj wzór szkieletowy kwasu cykloheks--eno--karboksylowego.
Po nazwie możemy wywnioskować, że szkielet węglowy tego kwasu składa się z cykloheksanu.

Następnym krokiem jest dodanie grupy do pierścienia.

Licząc kolejno od atomu węgla, do którego przyłączona została grupa , wiązanie podwójne dodajemy do trzeciego atomu węgla.

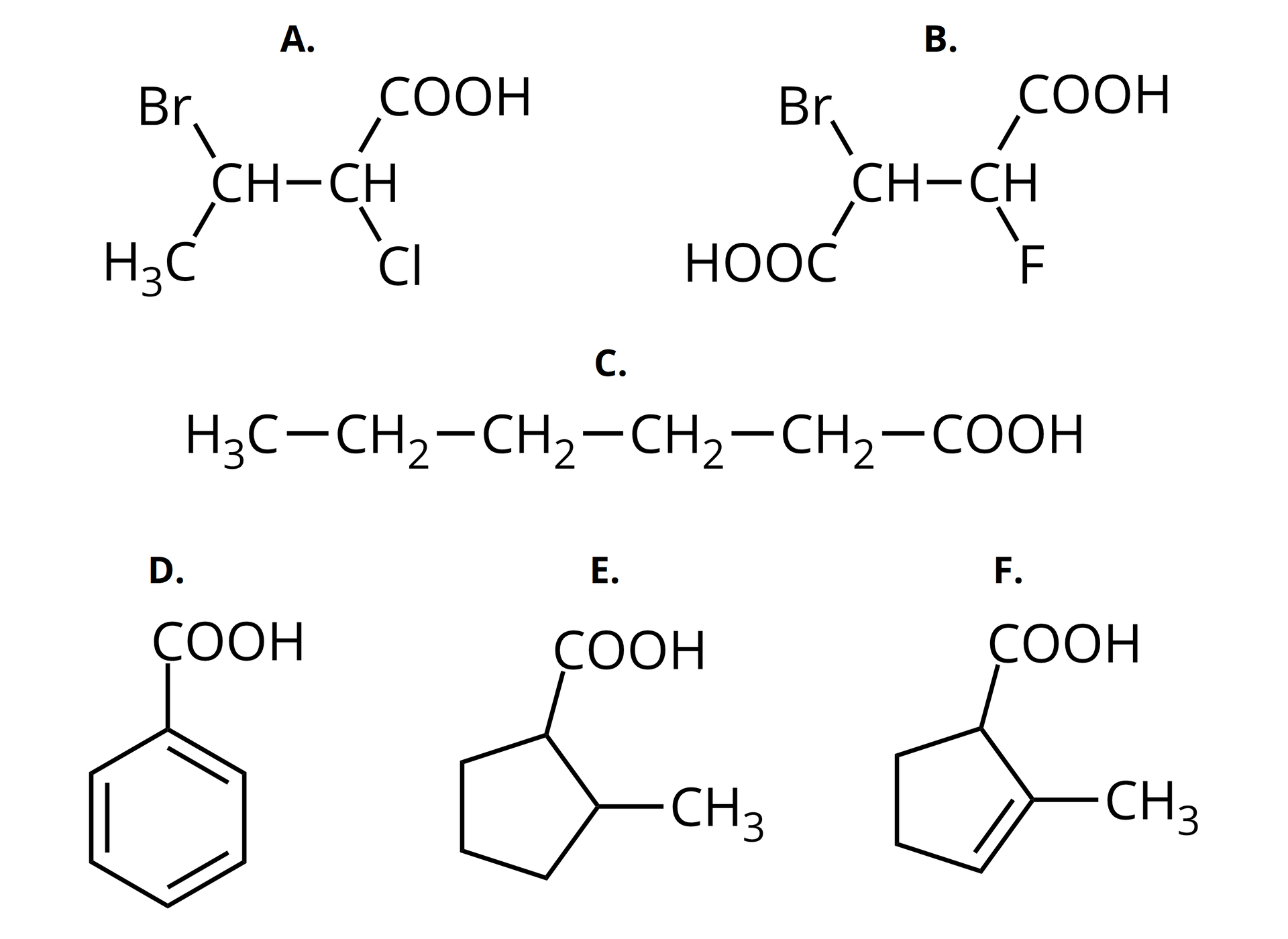
Na podstawie poniższych wzorów półstrukturalnych, podaj nazwy systematyczne bądź zalecane przedstawionych poniżej kwasów karboksylowych.
Przykład
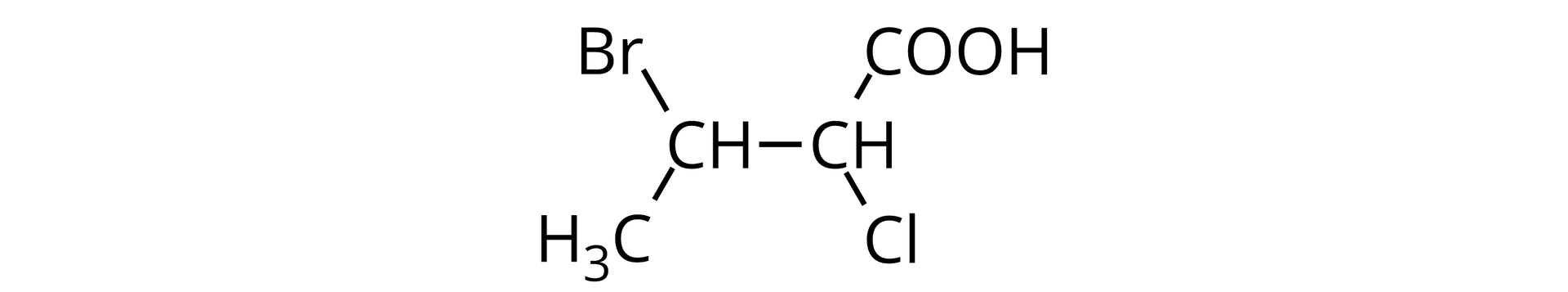
Wybieramy najdłuższy łańcuch węglowy i numerujemy atomy węgla, zaczynając od grupy .

W cząsteczce tego kwasu znajdują się cztery atomy węgla, połączone wiązaniami pojedynczymi, więc podstawą nazwy będzie nazwa węglowodoru nazywanego butanem (węglowodór nasycony).
Zauważ, że przy trzecim atomie węgla znajduje się atom bromu, a przy drugim jest atom chloru. Kolejny krok to „poskładanie” nazwy poprzez podawanie nazw podstawników w kolejności alfabetycznej.
Nazwa kwasu: kwas -bromo--chlorobutanowy.
Zapisz poniżej nazwy pozostałych kwasów.
Zapoznaj się z filmem, a dowiesz się, jak nazywać kwasy karboksylowe oraz jak – na podstawie nazwy – narysować ich wzór półstrukturalny.

Film dostępny pod adresem /preview/resource/R1MME3NOMKK44
Film nawiązujący do treści materiału dotyczącej tworzenia i interpretacji nazw i wzorów kwasów karboksylowych.
Otrzymywanie kwasów karboksylowych
Otrzymywanie alifatycznych kwasów karboksylowych
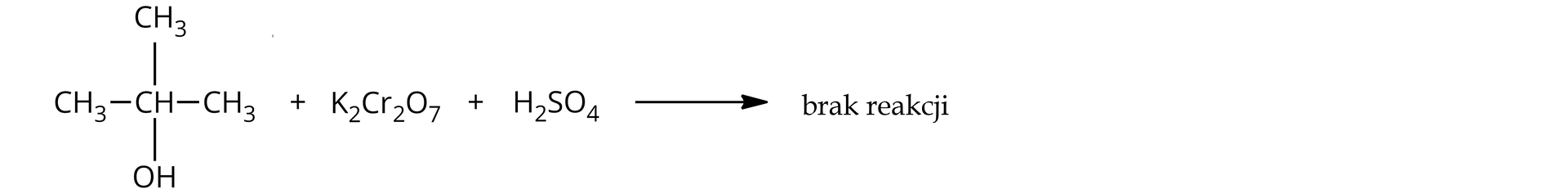
Część metod otrzymywania kwasów karboksylowych została już poznana we wcześniejszych tematach. Do takich metod można zaliczyć utlenianie aldehydów, które zachodzi m.in. w próbie Tollensa oraz próbie Trommera – w ich wyniku aldehydy ulegają przemianie do odpowiednich kwasów karboksylowych. Innym sposobem otrzymywania kwasów karboksylowych jest utlenianie alkoholi, jednak reakcja ta wymaga zastosowania mocnych środków utleniających, takich jak dichromiany czy nadmanganiany, i prowadzi do powstania kwasów z alkoholi pierwszorzędowych.
Sprawdź w poniższym laboratorium jak ważna jest rzędowość alkoholu użytego do reakcji utleniania.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zachowanie alkoholi pierwszo-, drugo- i trzeciorzędowych wobec takich utleniaczy jak dichromian(VI) potasu w środowisku kwasowym
Szafa laboratoryjna
Przeprowadzono doświadczenie w laboratorium chemicznym. Zapoznaj się z opisem doświadczenia, a następnie wykonaj polecenia. Analiza doświadczenia: Zachowanie alkoholi pierwszo-, drugo- i trzeciorzędowych wobec takich utleniaczy, jak dichromian() potasu w środowisku kwasowym.
Problem badawczy: Czy produkt powstały w wyniku reakcji alkoholi z utleniaczem, takim jak w środowisku kwasu siarkowego(), zależy od rzędowości alkoholi?
Hipoteza: W wyniku reakcji alkoholi pierwszo-, drugo- i trzeciorzędowych z utleniaczami w środowisku powstają różne produkty.
Odczynniki: etanol, propan--ol, -metylopropan--ol, roztwór dichromianu() potasu roztwór kwasu siarkowego().
Szkło laboratoryjne
probówka – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
kolba kulista płaskodenna – szklane naczynie laboratoryjne o kształcie ściętej kuli od dołu; długa szyjka z nacięciem określa dokładnie określoną objętość kolby; pomimo kulistego kształtu można je stawiać na stole lub szafce;
kolba stożkowa – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką;
szalki Petriego – szklane spodki do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
lejek szklany – podstawowy sprzęt laboratoryjny, zazwyczaj w kształcie stożka zakończonego rurką lub szlifem, który służy do przelewania płynów, przesypywania proszków oraz do sączenia;
bagietka szklana – pręcik szklany, służący do mieszania cieczy
łyżka metalowa – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
łyżka do spalań – sprzęt laboratoryjny stosowany głównie w analizie jakościowej, ściślej płomieniowej wykonywany ze spieków ceramicznych lub wysokoodpornych termicznie stopów metali;
szczypce laboratoryjne – sprzęt przeznaczony do podtrzymywania drobnego sprzętu laboratoryjnego;
pipety Pasteura – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łapa drewniana – rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej;
trójnóg z siatką – urządzenie w kształcie pierścienia, zaopatrzone w trzy wkręcane nogi, mocowane prostopadle do jego powierzchni, służące do ustawiania nad palnikiem naczyń laboratoryjnych, przeznaczonych do podgrzania;
palnik laboratoryjny – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych.
Przebieg doświadczenia:
Przygotowano trzy probówki i do każdej z nich wlano po dwa centymetry sześcienne roztworu dichromianu() potasu oraz dwa centymetry sześcienne roztworu kwasu siarkowego().
Następnie do każdej probówki dodano po dwa centymetry sześcienne innego alkoholu: etanolu, propan--olu, -metylopropan--olu.
Wstrząśnięto probówkami w celu wymieszania reagentów, a następnie ogrzano je w łaźni wodnej.
Obserwacje:
W probówce z etanolem i propan--olem po ogrzaniu zmienia się zabarwienie roztworu z pomarańczowego na zielony. W probówce z -metylopropan--olem roztwór nie zmienia koloru.
Wyniki:
Alkohole pierwszo- i drugorzędowe ulegają przeprowadzonej reakcji.
Wnioski:
Alkohole -rzędowe utleniają się do kwasów karboksylowych.
Alkohole -rzędowe utleniają się do ketonów.
Alkohole -rzędowe nie ulegają reakcji utlenienia.