Kwasy karboksylowe - właściwości i zastosowanie
Właściwości fizyczne kwasów karboksylowych
Rozpuszczalność
W cząsteczkach kwasów karboksylowych występuje polarna grupa karboksylowa, w której skład wchodzi grupa karbonylowa () oraz hydroksylowa (). Obecność tych grup sprawia, że możliwe jest wytworzenie wiązania wodorowego pomiędzy cząsteczkami kwasu. Obecność grupy hydroksylowej i karbonylowej wpływa na właściwości fizyczne kwasów karboksylowych. Grupa karbonylowa charakteryzuje się wysoką polarnością, dzięki czemu kwasy karboksylowe są silnie polarne. Dodatkowo atom wodoru, pochodzący z grupy karbonylowej, z łatwością tworzy wiązania wodorowe. Przypomnij sobie, że pierwszy z węglowodorów – metan () – w warunkach pokojowych jest gazem. Natomiast najprostszy kwas karboksylowy – kwas mrówkowy () – w warunkach pokojowych jest cieczą. Swój stan skupienia zawdzięcza właśnie występowaniu wiązania wodorowego, wytworzonego między cząsteczkami kwasu.
Kwasy karboksylowe wykazują lepszą rozpuszczalność w etanolu (lub innych rozpuszczalnikach organicznych) ze względu na możliwość wytworzenia wiązań wodorowych między grupą karbonylową cząsteczki kwasu a grupą hydroksylową cząsteczki alkoholu. Rozpuszczalność kwasów karboksylowych w wodzie jest spowodowana tworzeniem się wiązań wodorowych oraz oddziaływań dipol‑dipol pomiędzy polarnym fragmentem organicznej cząsteczki (kwasu) a wodą. Podobna sytuacja występuje w przypadku rozpuszczania alkoholi w wodzie. Rozpuszczalność kwasów karboksylowych zmniejsza się wraz ze wzrostem liczby atomów węgla w budowie kwasu.
Czy wiesz, co jest przyczyną dobrej rozpuszczalności kwasów w wodzie? Zapoznaj się z animacją i rozwiąż poniższe zadania.
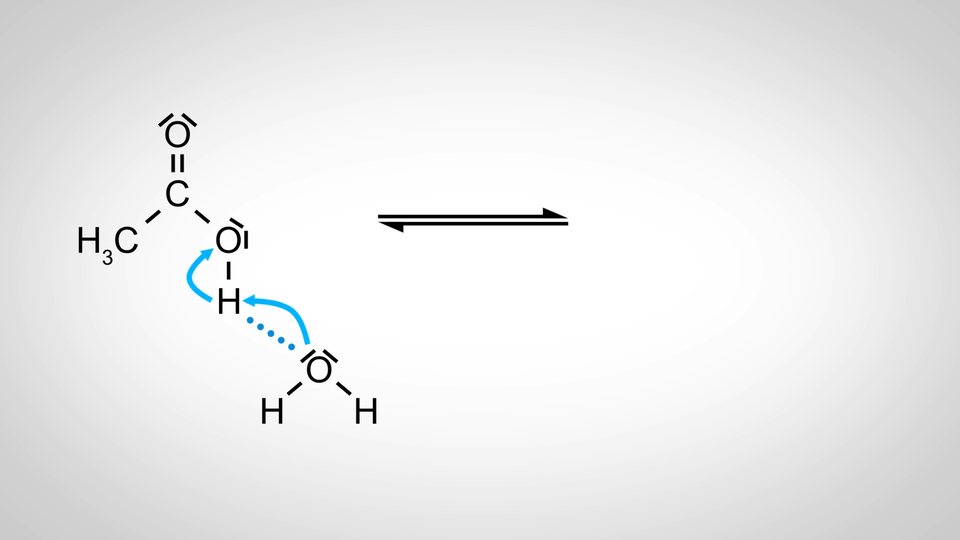
Film dostępny pod adresem /preview/resource/R1BdNx0KuGwIt
Film nawiązujący do treści materiału - wyjaśnia, jak w wodzie zachowują się kwasy karboksylowe.
Właściwości chemiczne kwasów karboksylowych
Dysocjacja kwasów karboksylowych
Kwasy organiczne są słabymi elektrolitami, co oznacza, że w roztworze wodnym nie wszystkie cząsteczki kwasu dysocjują na kationy hydroniowe () i aniony reszty kwasowej ().
W celu określenia mocy kwasu organicznego używa się stałej dysocjacji elektrolitycznej kwasowej .
Wyrażenie na stałą dysocjacji kwasu:
- równowagowe stężenie molowe jonów hydroniowych ;
- równowagowe stężenie molowe jonów karboksylanowych ;
- równowagowe stężenie molowe kwasu karboksylowego .
Im wartość stałej dysocjacji kwasu większa, tym więcej cząsteczek kwasu ulega dysocjacji, w rezultacie pH roztworu maleje.
Spróbuj samodzielnie zbadać właściwości fizykochemiczne kwasów karboksylowych w poniższym wirtualnym laboratorium i rozwiąż ćwiczenia.
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod ikoną notatnika w prawym górnym rogu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DFJ4L5AR5
Analiza eksperymentu: Badanie właściwości fizycznych i chemicznych kwasów karboksylowych.
Problem badawczy: Czy właściwości kwasów karboksylowych zależą od rodzaju kwasu karboksylowego?
Hipoteza: Właściwości kwasów karboksylowych są zależne od rodzaju kwasu karboksylowego.
Odczynniki chemiczne: kwas etanowy, kwas pentanowy, kwas benzoesowy, fenoloftaleina, magnez, wodorotlenek sodu, tlenek miedzi(II).
Sprzęt laboratoryjny: probówki - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych; pipety Pasteura, - wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; łyżki laboratoryjne - długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych; statyw na probówki - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; tryskawka - plastikowe naczynie zamknięte nakrętką z długą końcówką. Tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę; palnik - rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych; łuczywo - długi patyczek z drewna, służący do przenoszenia płomienia, na przykład nad probówkę.
Instrukcja wykonania doświadczenia.
Badanie właściwości fizycznych. 1. wybrano badany kwas karboksylowy. 2. dodano małą ilość kwasu do próbówki oraz zaobserwowano barwę, stan skupienia kwasu. 3. używając truskawki, dodano małą ilość wody do próbówki oraz wstrząśnięto probówką.
Badanie właściwości chemicznych. 1. Reakcja kwasu etanowego z metalami. Wlano do próbówki około trzech centymetrów sześciennych wodnego roztworu kwasu etanowego. Dodano do próbówki niewielką ilość zbiórek magnezowych. Zbliżono płonące łuczywo do wylotu próbówki. Zwrócono uwagę na efekty dźwiękowe reakcji. 2. Reakcja kwasu etanowego z wodorotlenkiem sodu. Wlano do próbówki około trzech centymetrów sześciennych roztworu wodorotlenku sodu. Dodano dwie‑trzy krople fenoloftaleiny. Dodano kroplami wodny roztwór kwasu etanowego. Zaobserwowano zmiany barwy zawartość próbówki. 3. Reakcja z tlenkami metali. Wlano do próbówki około trzech centymetrów sześciennych wodnego roztworu kwasu etanowego. Dodano do próbówki trochę tlenku miedzi(II). Lekko ogrzano probówkę. Zwrócono uwagę na zmianę barwy reagentów.
Obserwacje:
Badanie właściwości fizycznych:
mieszalność z wodą: wszystkie kwasy mieszają się z wodą, tworząc bezbarwne roztwory; kwas benzoesowy rozpuszcza się;
stan skupienia i barwa: kwas etanowy, kwas pentanowy to bezbarwne ciecze; kwas benzoesowy to białe ciało stałe.
Badanie właściwości chemicznych:
reakcja kwasu etanowego z metalami: wydzielają się pęcherzyki gazu;
reakcja kwasu etanowego z NaOH: po dodaniu fenoloftaleina zmienia kolor na malinowy; po dodaniu kwasu etanowego (octowego) roztwór odbarwia się; w reakcji z tlenkiem miedzi(II) roztwór przyjmuje barwę niebieską.
Wyniki: w reakcji z NaOH kwas octowy zobojętnił wodorotlenek sodu. Produktami reakcji były: octan sodu (etanian sodu) i woda. W reakcji z tlenkiem miedzi(II) powstaje sól – octan miedzi(II) i woda.Wydzielającym się gazem w reakcji kwasu etanowego z magnezem jest wodór.
Wnioski: Hipoteza została potwierdzona – właściwości fizyczne i chemiczne są zależne od rodzaju kwasu karboksylowego.
Czy wiesz, jakie czynniki wpływają na reaktywność kwasów karboksylowych? Zapoznaj się z poniższym filmem. W oparciu o zdobytą wiedzę postaraj się samodzielnie wykonać przedstawione w filmie zadanie, a następnie rozwiąż poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/R1SWYfINJsAZf
Film nawiązujący do treści materiału - odpowiada na pytanie, jakie czynniki wpływają na moc i reaktywność kwasów karboksylowych.
Czy wiesz, jakie czynniki wpływają na reaktywność kwasów karboksylowych? Zapoznaj się z poniższym filmem. W oparciu o zdobytą wiedzę postaraj się samodzielnie wykonać przedstawione w filmie zadanie, a następnie rozwiąż poniższe ćwiczenia.
Reakcje spalania
W zależności od dostępności tlenu, wyróżniamy kilka sposobów spalania, m.in. całkowite i niecałkowite.
Równania reakcji spalania całkowitego wybranych kwasów karboksylowych:
Równanie reakcji spalania niecałkowitego kwasu oktadekanowego (stearynowego):
Reakcja z metalami
Doświadczenie I
Reakcja z tlenkami metali
Doświadczenie II

Reakcja z wodorotlenkami metali
Doświadczenie III

W wyniku reakcji kwasu octowego (etanowego) z sodem lub tlenkiem sodu oraz wodorotlenkiem sodu otrzymujemy octan (etanian) sodu. Ta sól dobrze rozpuszcza się w wodzie. Wraz ze wzrostem temperatury wzrasta jej rozpuszczalność. Przygotowanie nasyconego roztworu tej soli, a następnie jego oziębienie, spowoduje powstanie roztworu przesyconego. Wprowadzając bagietkę lub szczyptę octanu sodu do takiego roztworu, wywołamy natychmiastową krystalizację. Powstaje ciało stałe – hydrathydrat octanu (etanianu) sodu . Procesowi towarzyszy wydzielanie ciepła, dlatego omawiana sól jest wykorzystywana w produkcji kieszonkowych ogrzewaczy termicznych.


