Masa cząsteczkowa i molowa związku chemicznego
Cząsteczki mają niezmiernie małe masy, dlatego – podobnie jak masy atomów – wyraża się je w atomowych jednostkach masy. Masa cząsteczek zależy od masy atomów, które wchodzą w ich skład. Do określania masy cząsteczkowej niezbędna jest znajomość wzoru związku chemicznego. Na jego podstawie można także ustalić udział każdego pierwiastka w całej masie związku chemicznego.
Co to jest masa atomowa pierwiastka?
Masa atomu jest bardzo mała, stanowi tylko niewielką część grama (około ). Wyraża się ją w atomowych jednostkach masy, zwanych unitami. Wartość jednego unitu wynosi .
Masa atomowa jest niepowtarzalną cechą pierwiastka i nie ma dwóch pierwiastków, które miałyby jednakową jej wartość. Dlatego też znając tylko masę atomową, można zidentyfikować pierwiastek.
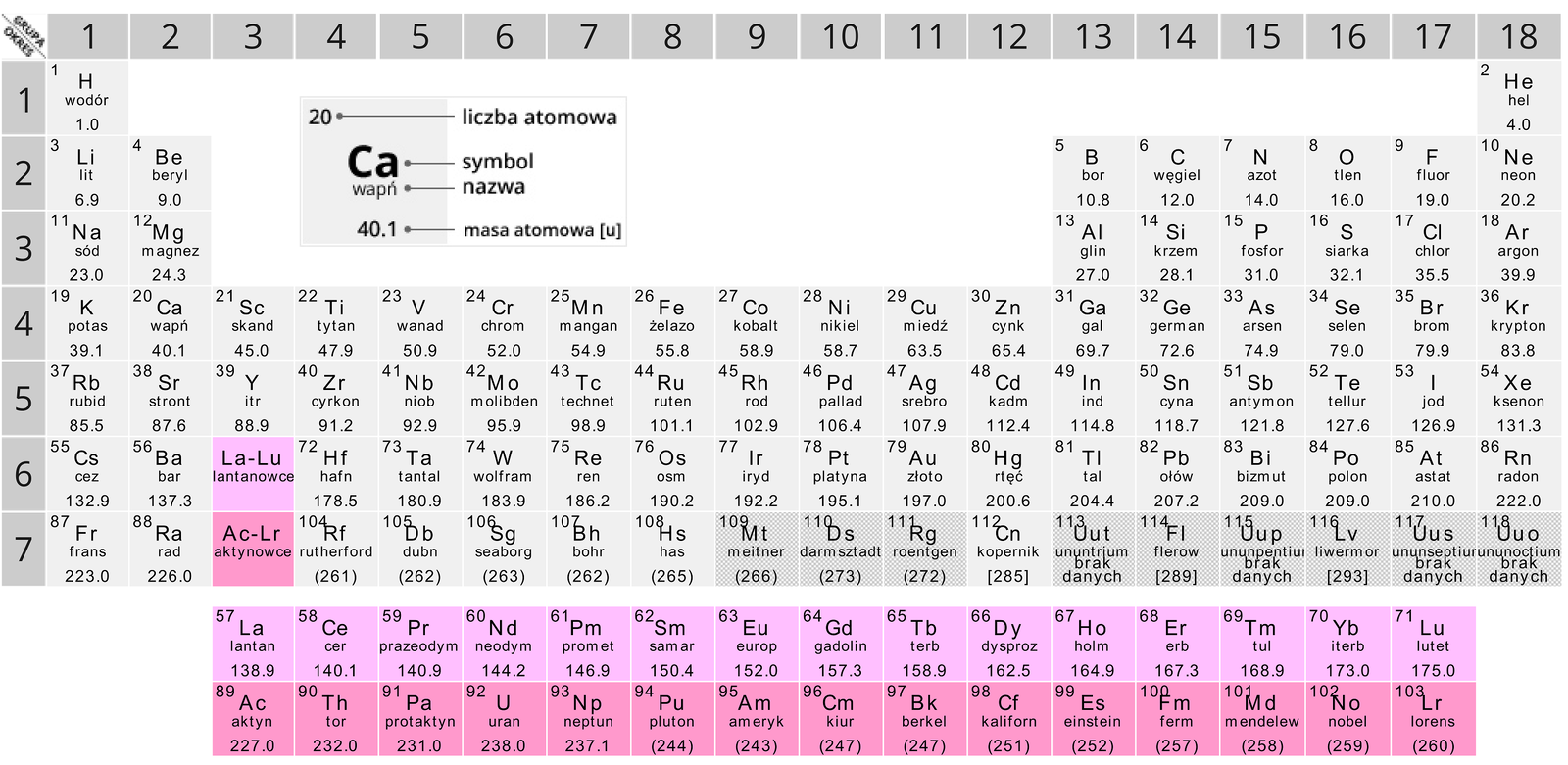
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D7OD1ETGD
Korzystając z układu okresowego, odszukaj pierwiastki o masach atomowych: 32 u, 23 u, 4 u i 40 u, a następnie podaj ich nazwy oraz symbole chemiczne.
Jak obliczamy masę cząsteczkową związku chemicznego?
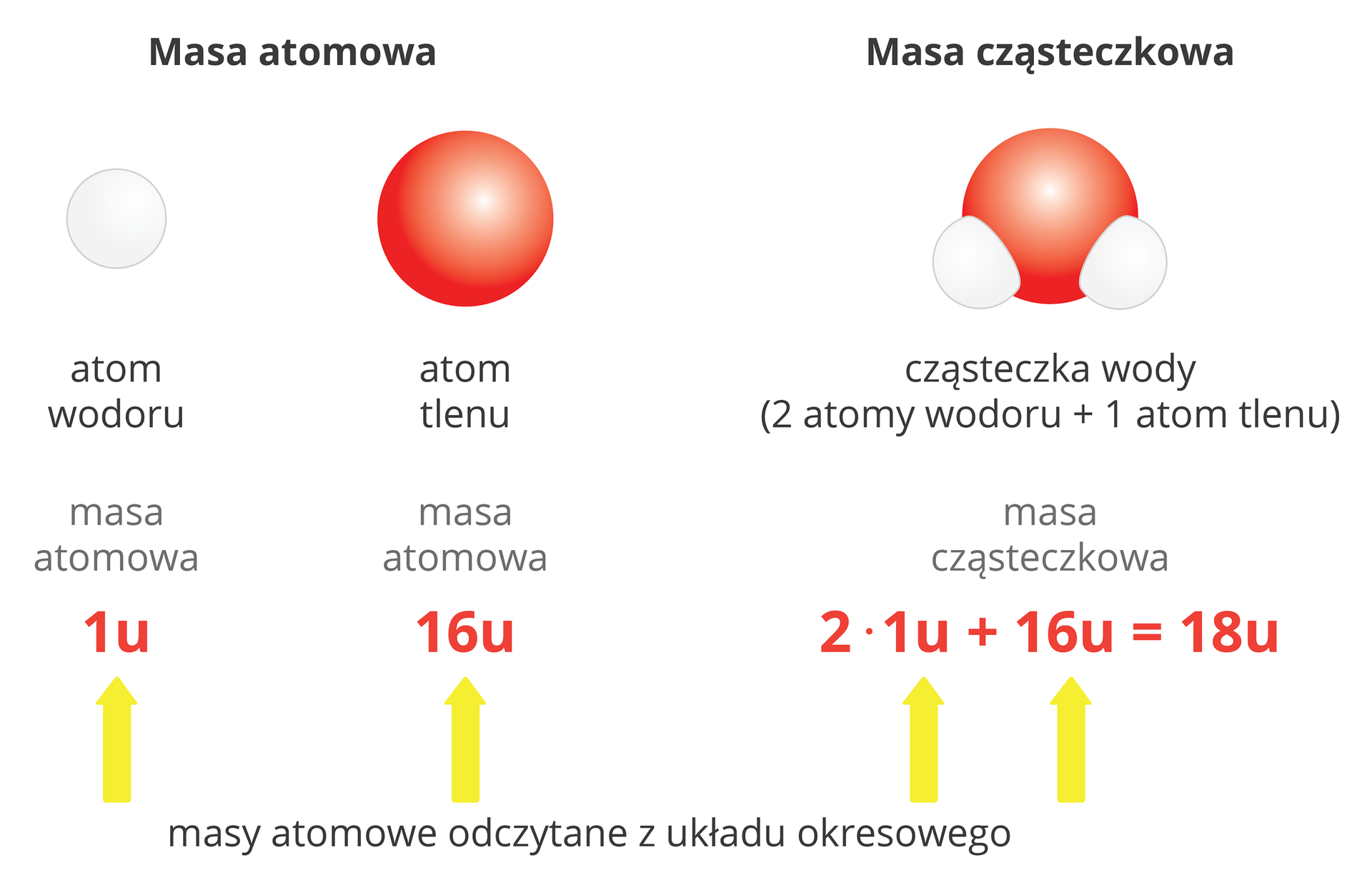
Związki chemiczne są zbudowane z cząsteczek lub tworzą sieci krystaliczne, w których jony występują w określonym stosunku ilościowym. Wzór sumaryczny zwykle odpowiada najprostszemu stosunkowi stechiometrycznemu atomów lub jonów tworzących związek chemiczny. Masa tych najmniejszych struktur związków chemicznych, wyrażona w atomowych jednostkach masy, jest nazywana masą cząsteczkową. Mimo tego, że w nazwie tej występuje wyraz „cząsteczkowa”, to jednak jej zakres nie ogranicza się tylko do związków cząsteczkowych, ale obejmuje także substancje zbudowane z jonów. Masa cząsteczkowa jest sumą iloczynów masy atomowej danego pierwiastka i liczby atomów tego pierwiastka w związku chemicznym.
Masę atomową poszczególnych pierwiastków można odczytać z układu okresowego. Jest ona zazwyczaj wyrażona liczbą niecałkowitą, z kilkoma cyframi po przecinku. W obliczeniach chemicznych masy atomowe zaokrągla się zazwyczaj do liczb całkowitych.
Dokonując przybliżeń, trzeba kierować się pewnymi zasadami:
1. Jeśli pierwsza cyfra po przecinku jest mniejsza od 5, to odrzucamy wszystkie cyfry znajdujące się za przecinkiem, na przykład:
2. Jeśli cyfra znajdująca się jako pierwsza po przecinku jest większa od 5, to zwiększamy cyfrę odpowiadającą jedności o 1, na przykład:
3. Dla np. chloru pierwsza cyfra po przecinku wynosi 5 (ich mas atomowych nie zaokrągla się do liczb całkowitych).

Film dostępny pod adresem /preview/resource/RGTxzIE8m46sj
W filmie ukazano, w jaki sposób obliczyć masę cząsteczkową chlorowodoru, wykorzystując układ okresowy pierwiastków.
Film dostępny pod adresem /preview/resource/RNQXFuYzXsD2I
W filmie ukazano, w jaki sposób obliczyć masę cząsteczkową kwasu fosforowego(V), wykorzystując układ okresowy pierwiastków.
Wzór sumaryczny | Nazwa związku | Wyrażenie na masę cząsteczkową związku | Wartość |
chlorek sodu | 58,5 | ||
chlorek glinu | 133,5 | ||
metan | 16 | ||
kwas siarkowy(VI) | 98 | ||
sacharoza | 342 | ||
wodorotlenek magnezu | 58 |
Masa molowa
Masa jednego mola pierwiastków lub związku chemicznego jest nazywana masą molową. Jej jednostką w układzie SI jest , choć najczęściej jest wyrażana w i oznaczona symbolem . W dolnym indeksie należy dodać informację o rodzaju substancji (np. , ).
Średnia masa atomowa żelaza wynosi . W związku z tym jeden mol atomów żelaza ma masę . Do określania masy jednego mola pierwiastka można wykorzystać dane zawarte w układzie okresowym pierwiastków.
W poniższej tabeli przedstawione zostały masy atomowe, masy molowe oraz masy mola wybranych pierwiastków.
Symbol | Pierwiastek | Średnia | Masa mola | Masa molowa |
|---|---|---|---|---|
sód | ||||
magnez | ||||
węgiel |
Na poniższym rysunku porównano ilości, jakie stanowi jeden mol pierwiastka.
Czy wiesz, jak obliczyć masy molowe związków chemicznych? Ile moli stanowią konkretne masy związków? Zapoznaj się z filmem samouczkiem, a następnie sprawdź swoją wiedzę, rozwiązując poniższe zadania.

Film dostępny pod adresem /preview/resource/RueUIN26b3pNT
Film nawiązujący do treści materiału - dotyczy obliczania mas molowych związków chemicznych.
A. M g S O indeks dolny, cztery, koniec indeksu dolnego
B. N a indeks dolny, trzy, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego
C. C indeks dolny, pięć, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, B r
D. C a nawias, O H, zamknięcie nawiasu, indeks dolny, dwa, koniec indeksu dolnego
Wybierz poprawny zestaw odpowiedzi: Możliwe odpowiedzi: 1. A. sto dwadzieścia początek ułamka, g, mianownik, mol, koniec ułamka
B. sto sześćdziesiąt cztery początek ułamka, g, mianownik, mol, koniec ułamka
C. sto pięćdziesiąt jeden początek ułamka, g, mianownik, mol, koniec ułamka
D. siedemdziesiąt cztery początek ułamka, g, mianownik, mol, koniec ułamka, 2. A. pięćdziesiąt trzy początek ułamka, g, mianownik, mol, koniec ułamka
B. sto dziewięćdziesiąt początek ułamka, g, mianownik, mol, koniec ułamka
C. dziewięćdziesiąt pięć początek ułamka, g, mianownik, mol, koniec ułamka
D. czterdzieści pięć początek ułamka, g, mianownik, mol, koniec ułamka, 3. A. dziewięćdziesiąt sześć początek ułamka, g, mianownik, mol, koniec ułamka
B. sto osiemdziesiąt początek ułamka, g, mianownik, mol, koniec ułamka
C. sto dwadzieścia początek ułamka, g, mianownik, mol, koniec ułamka
D. siedemdziesiąt początek ułamka, g, mianownik, mol, koniec ułamka
Oblicz masy molowe podanych związków:
A.
B. .
Jak obliczyć liczbę moli związku chemicznego w próbce o podanej masie i odwrotnie?
Aby obliczyć liczbę moli indywiduów chemicznych, znając masę próbki, należy podzielić masę w gramach przez masę molową:
Oblicz masę węgla. Masa molowa węgla wynosi .
Oblicz liczbę moli zawartą w tej substancji.
Sprawdź masę molową wybranego pierwiastka lub związku chemicznego.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D7OD1ETGD