Równanie Clapeyrona
Dotarcie do idealnego prawa gazowego
Ponad trzy stulecia temu naukowcy przeprowadzali eksperymenty, aby sprawdzić, jak zachowują się gazy, jeśli ich ciśnienie lub temperatura ulegną zmianie. Na podstawie badań sformułowano prawa dla hipotetycznego gazu, zwanego „gazem doskonałym”.
Równanie Clapeyrona (często nazywane też równaniem gazu doskonałego) opisuje zależność między ciśnieniem, objętością, temperaturą oraz ilością gazu. Jest ono jednym z podstawowych równań wykorzystywanych w chemii i fizyce do opisu zachowania gazów.
Równanie to ma postać:
Gdzie:
– ciśnienie gazu;
– objętość;
– liczba moli gazu;
– temperatura bezwzględna (w Kelwinach);
– stała gazowa; .
W obliczeniach należy zwrócić uwagę na warunki, w jakich znajduje się gaz (warunki standardowewarunki standardowe albo warunki normalnewarunki normalne).
Do przeliczenia temperatury () wyrażonej w stopniach Celsjusza () na Kelwiny (), należy posługiwać się zależnością:
Przeliczanie temperatury wyrażonej w stopniach Celsjusza na skalę Kelwina.
np. w skali Kelwina wynosi:
w skali Kelwina ma wartość .
Jak wyprowadzić prawa gazowe z równania stanu gazu doskonałego?
Mamy początkowe wartości dla stanu gazu:
W innych warunkach, kiedy zmieniamy stan gazu, liczba cząsteczek/atomów nie zmienia się w trakcie przemiany ().
Gdy ciśnienie gazu jest stałe (), otrzymujemy:
Dzielimy dwie strony równania przez i dotarliśmy do prawa Gay‑Lussaca:
Zastosowanie równania gazu doskonałego (równanie Clapeyrona)
Równanie Clapeyrona stosuje się w zadaniach praktycznych, gdy gaz zmienia swoją objętość, ciśnienie lub temperaturę. Pozwala ono obliczać te wielkości fizyczne w różnych przemianach gazowych. Przekształcając równanie Clapeyrona, możemy również wyznaczyć wielkości w stałych warunkach:
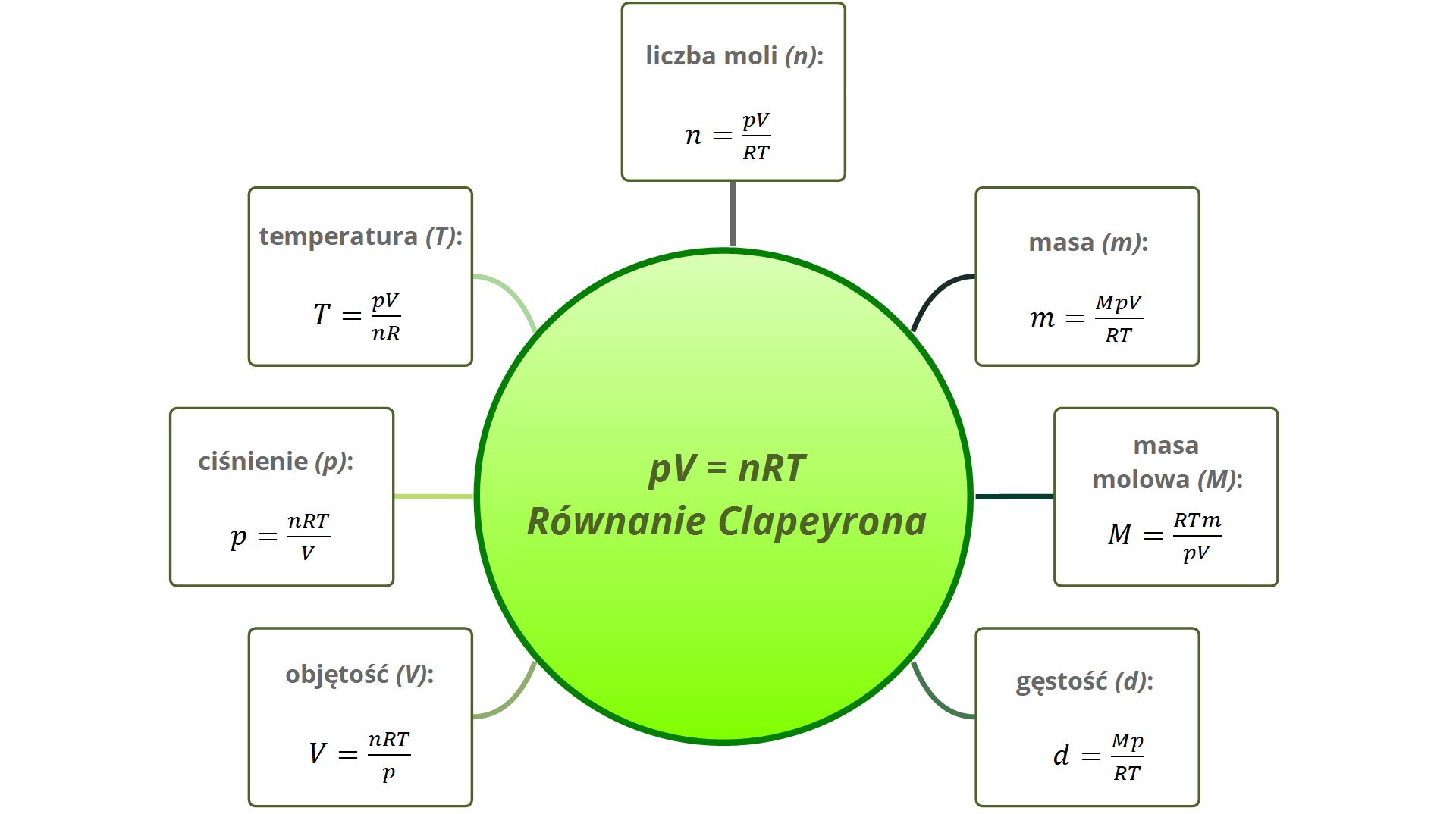
Spójrz na poniższe problemy, aby zapoznać się z różnymi przykładami zastosowań równania Clapeyrona. Najpierw spróbuj rozwiązać je samodzielnie, a jeśli potrzebujesz pomocy – rozwiązania są ukryte tuż pod nimi.
Oblicz ciśnienie, jakie jest wywierane na mole gazu znajdującego się w pojemniku o objętości , jeśli temperatura wewnątrz układu wynosi .
Oblicz masę chloru w temperaturze i pod ciśnieniem . Przyjmij, że stała gazowa wynosi .
Zapoznaj się z symulacją, która ilustruje równanie Clapeyrona oraz zmiany parametrów układu. Zwróć uwagę, że poruszające się w zamkniętych pojemnikach kulki prezentują model cząsteczek gazu doskonałego, natomiast kształt cząsteczek gazów rzeczywistych może różnić się od zaprezentowanego poniżej.
Za pomocą suwaków dołączonych do wykresów zmieniaj parametry układu, a następnie odpowiedz na pytania zamieszczone pod symulacją.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBHKQXHMS
Równanie Clapeyrona (równanie stanu gazu doskonałego)
jest kombinacją wszystkich omówionych praw gazowych:
Gdzie:
– ciśnienie gazu;
– objętość;
– liczba moli gazu;
– temperatura bezwzględna (w Kelwinach);
– stała gazowa; .
Załóżmy, że gaz zajmuje pewną stałą objętość. Odpowiedz, jak zmienia się ciśnienie gazu, gdy temperatura pojemnika, w którym znajduje się gaz, rośnie.
Wyprowadź zależność między parametrami równania Clapeyrona w momencie, gdy temperatura układu, w którym znajduje się gaz, przyjmuje stałą wartość.
Objętość gazu w warunkach normalnych
Warunki normalne zdefiniowane są następująco:
Ciśnienie normalne: 101 325 Pa = 1013,25 hPa (średnie ciśnienie atmosferyczne na poziomie morza).
Temperatura normalna: 273,15 K, czyli (temperatura krzepnięcia wody przy ciśnieniu normalnym).
Rozważ następujący problem: jaką objętość ma 1 mol gazu w warunkach normalnych?
Korzystamy z równania Clapeyrona: , gdzie to ciśnienie normalne, – temperatura normalna, – liczba moli (), – stała gazowa, a to szukana objętość 1 mola gazu. Mamy stąd:
Zauważ, że powyższy wynik nie zależy od rodzaju gazu pod warunkiem, że gaz można traktować jak gaz doskonały. Otrzymaliśmy więc ważny rezultat:
1 mol każdego gazu ma w warunkach normalnych objętość (22,4 litra).
Wybierz właściwą odpowiedź:
1. Pojemnik A. T=273,15 K, p=1000 hPa
2. Pojemnik B. t=0 stopni Celsjusza, p=101325 Pa
3. Pojemnik C. T=273,15 K, p=1013,25 hPa
4. Pojemnik D. t=20 stopni Celsjusza, p=101325 Pa
Oblicz, ile moli powietrza znajduje się w pokoju.
n, równa się
Wybierz odpowiedź:
A. 2322
B. 3232
C. 2232