Chromatografia
Zapewne zdarzyło Ci się kiedyś zamoczyć kawałek papieru, na którym coś napisano kolorowym pisakiem lub atramentem. Co się stało? Prawdopodobnie tusz „rozlał się”, ale nie jako jednolita plama. Zamiast tego, wędrująca po kartce woda rozdzieliła go na różne barwy – na przykład czarny pisak mógł okazać się mieszaniną niebieskiego, żółtego i czerwonego barwnika. Powyższy przykład to jeden z najprostszych eksperymentów chromatograficznych.
Chromatografia to jedna z najważniejszych i najczęściej stosowanych technik rozdzielania mieszanin, jaką dysponuje współczesna nauka. Bez niej niemożliwa byłaby analiza składu leków, badania antydopingowe, kontrola czystości żywności czy wiele badań kryminalistycznych.
Nazwa tej metody pochodzi od greckich słów chrōma (kolor) i graphein (pisać). Dosłownie oznacza „pisanie kolorem”, ponieważ jej historyczne początki wiążą się z rozdzielaniem barwników roślinnych (np. chlorofilu) na wyraźne, kolorowe pasma.
Czy wiesz, kto odkrył chromatografię i w jakich okolicznościach?
Wprowadzenie do metod chromatograficznych
Chromatografia jest zaliczana do jednej z metod analitycznych i preparatywnych. Technika ta pozwala na rozkładanie mieszaniny na oddzielne składniki lub ich grupy (frakcjefrakcje), a także ich identyfikację. Procedura ta korzysta z różnic w zachowaniu poszczególnych związków chemicznych w układzie dwufazowym – czyli działa na zasadzie oddziaływań międzycząsteczkowych, powstających pomiędzy związkami chemicznymi, z których składa się mieszanina, a złożem. Wówczas pewne związki chemiczne przechodzą przez złoże szybciej, a inne wolniej.
Jedna z faz pozostaje w tym samym miejscu, nie ulega zmianie jej położenie (faza stacjonarna, faza nieruchomafaza nieruchoma, złoże, adsorbent). Druga natomiast przemieszcza się w stosunku do pierwszej w określonym kierunku (roztwór rozwijający, eluent, faza ruchomafaza ruchoma, faza nośna).
Chromatografię można podzielić, w zależności od stanu skupienia fazy ruchomej, na:
gazową – fazę ruchomą stanowi gaz (zazwyczaj hel, argon, wodór);
cieczową – fazę ruchomą stanowi ciecz;
nadkrytyczną – fazą ruchomą jest substancja (najczęściej tlenek węgla()) w stanie nadkrytycznym.
Możliwe zależności pomiędzy fazą ruchomą i fazą stacjonarną:
Faza ruchoma | Faza nieruchoma |
|---|---|
gaz | ciecz |
gaz | ciało stałe |
ciecz | ciecz |
ciecz | ciało stałe |
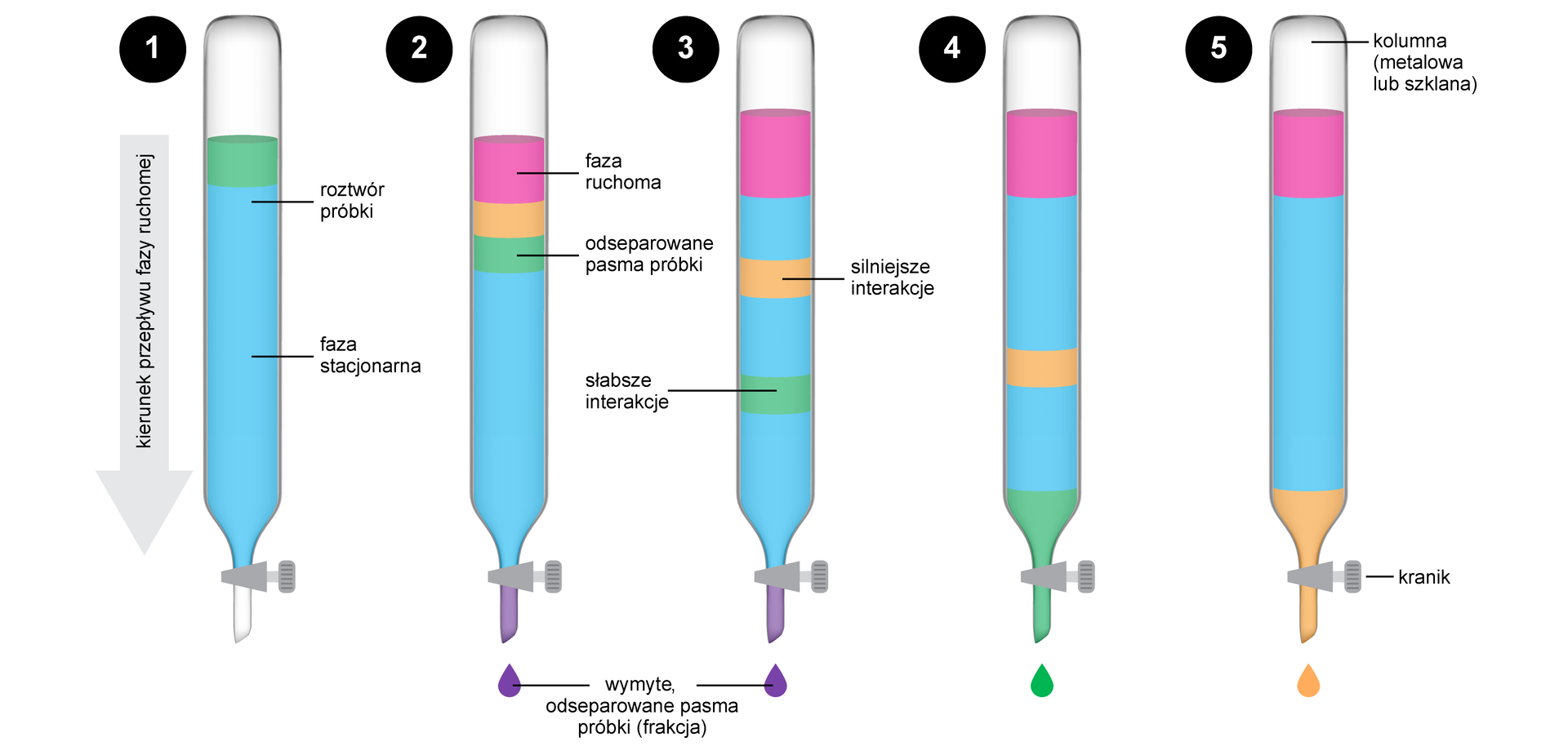
Chromatografia kolumnowa
Chromatografia kolumnowa jest reprezentantem chromatografii cieczowej. Jest dobrą i wydajną techniką, służącą do rozdzielania mieszanin i oczyszczania produktów naturalnych i syntetycznych.
W mechanizmie rozdzielania wykorzystuje się istnienie różnic w sile oddziaływań międzycząsteczkowych dla różnych związków, pomiędzy składnikami mieszaniny a fazą ruchomą oraz składnikami mieszaniny a fazą stacjonarną. W roli fazy stacjonarnej można używać rozmaitych adsorbentów, którymi są ciała stałe, porowate, o silnie rozwiniętej powierzchni, nierozpuszczalne w wodzie i rozpuszczalnikach organicznych.
Najczęściej stosowanymi adsorbentami (faza stacjonarna) są:
żel krzemionkowy – (silnie polarny);
tlenek glinu() – ;
węgiel aktywny;
poliamid;
glinokrzemiany.
Z kolei fazę ruchomą stanowią woda lub organiczne rozpuszczalniki, takie jak: metanol, acetonitryl, propanol lub heksan.
Związki polarne adsorbują się silniej na polarnych cząsteczkach silikażelu, dlatego są wymywane z kolumny później niż składniki mniej polarne, które poruszają się szybciej przy zastosowaniu rozpuszczalnika mniej polarnego.
Przeprowadź doświadczenie w laboratorium chemicznym. Metodą chromatografii kolumnowej rozdziel mieszaninę -nitrofenol i -nitrofenolu. Jako eluent zastosuj dichlorometan. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBZS7XUC6
Zapoznaj się z opisem doświadczenia, w którym metodą chromatografii kolumnowej rozdzielono mieszaninę -nitrofenol i -nitrofenolu. Jako eluent zastosowano dichlorometan. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje wyniki, a następnie sformułuj wnioski.
Analiza doświadczenia:
Chromatografia kolumnowa.
Problem badawczy:
Czy za pomocą chromatografii kolumnowej można rozdzielić -nitrofenol oraz -nitrofenol?
Hipoteza:
Za pomocą chromatografii kolumnowej można rozdzielić -nitrofenol oraz -nitrofenol.
Sprzęt laboratoryjny:
statyw – pionowy pręt ze stabilną podstawą, umożliwiający mocowanie na wybranej wysokości, na przykład szkła laboratoryjnego umieszczonego w łapie;
łapa – rodzaj narzędzia, wykorzystywanego w laboratorium do trzymania, na przykład kolb;
szklana kolumna chromatograficzna – szklana rurka zakończona u dołu kranikiem;
kolby stożkowe – szklane naczynia laboratoryjne o kształcie stożka z płaskim dnem i wąską szyjką;
lejek – szkło w kształcie odwróconego stożka, ze zwężającą się rurką, służący do przelewania cieczy lub sączenia;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca, z umieszczoną na ściance podziałką objętości, służące do odmierzania cieczy;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu, zakończony z jednej strony łyżeczką;
bagietka szklana – szklany pręt laboratoryjny służący do mieszania;
pipeta – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
mieszanina -nitrofenolu i -nitrofenolu, dichlorometan, silikażel
Przebieg doświadczenia:
Do zlewki dodano pięć łyżek silikażelu, a następnie około mililitrów dichlorometanu. Zawartość dokładnie wymieszano przy pomocy szklanej bagietki.
Przygotowany silikażel wraz z dichlorometanem przeniesiono do kolumny z wykorzystaniem lejka.
Łyżeczkę mieszaniny nitrofenoli rozpuszczono w jak najmniejszej ilości dichlorometanu i naniesiono na kolumnę przy pomocy pipety, lejąc bardzo powoli po ściankach kolumny.
Kolejno dokonano rozdziału mieszaniny, używając jako eluentu dichlorometanu, który w miarę przepływu fazy ruchomej uzupełniano tak, by jego poziom zawsze znajdował się ponad fazą stacjonarną.
Z zebranych frakcji odparowano rozpuszczalnik przy pomocy wyparki laboratoryjnej.
Obserwacje:
Po wprowadzeniu mieszaniny dwóch związków na kolumnę chromatograficzną, barwna smuga przesuwa się po silikażelu, a następnie rozdziela się w miarę postępującej elucji.
Wyniki: W wyniku przeprowadzenia chromatografii kolumnowej, mieszaniny -nitrofenolu oraz -nitrofenolu, otrzymano dwa czyste związki: -nitrofenol oraz -nitrofenol.
Wnioski: Chromatografia kolumnowa pozwala na rozdział badanej mieszaniny dwóch związków.
Hipoteza została potwierdzona.
Chromatografia cienkowarstwowa (TLC)
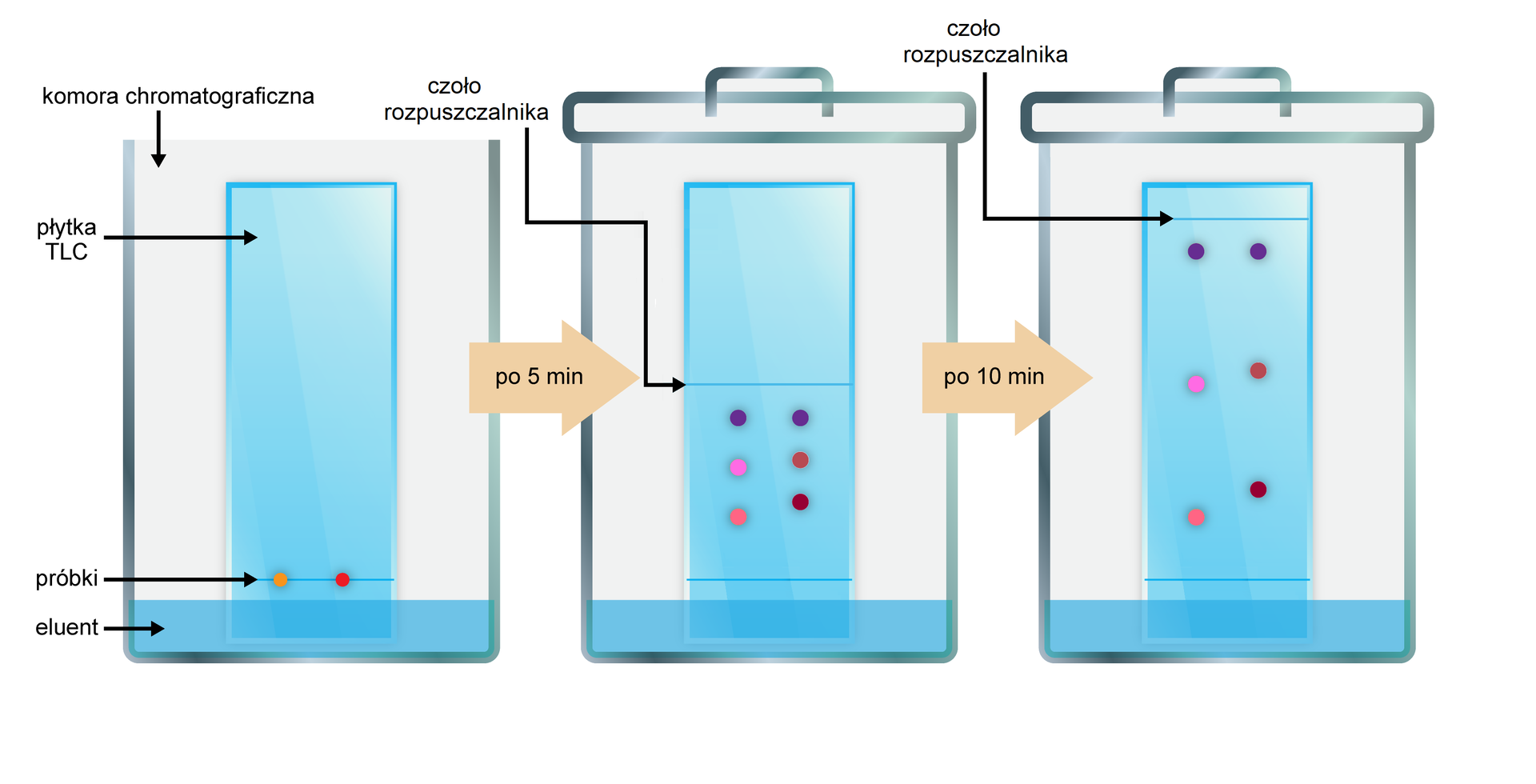
Chromatografia cienkowarstwowa (TLC, ang. Thin Layer Chromatography) stanowi powszechną technikę sprawnego kontrolowania postępu reakcji chemicznych i czystości produktów. Za pomocą tej metody można zidentyfikować związki zarówno organiczne, jak i nieorganiczne.
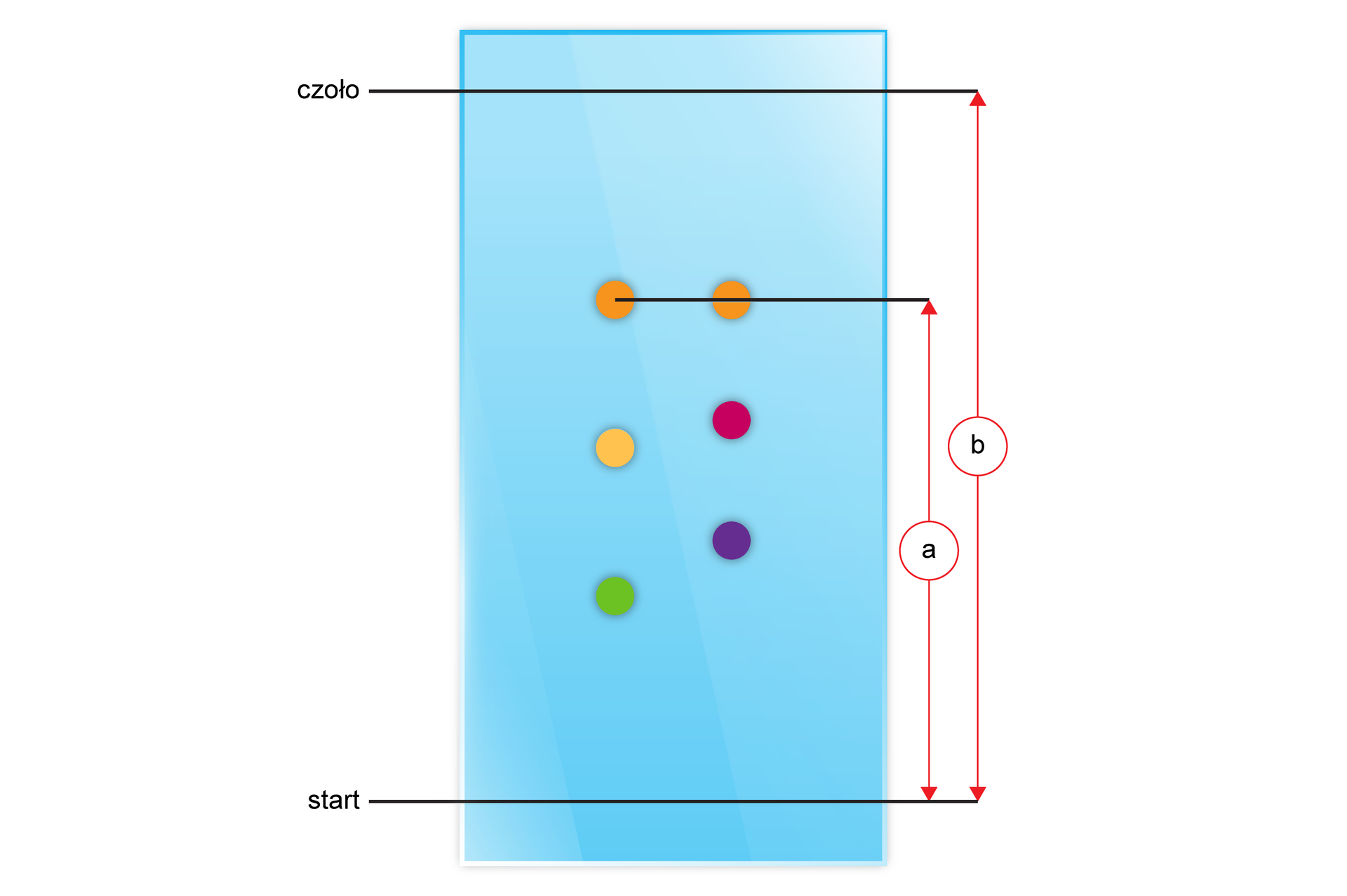
W technice TLC, fazę stacjonarną nakłada się w formie cienkiej, równomiernej warstewki na płytkę szklaną, arkusz folii aluminiowej lub na tworzywo sztuczne. Mieszaninę substancji do rozdzielenia lub po rozdziale nanosi się punktowo przy dolnej krawędzi płytki. Następnie płytkę chromatograficzną umieszcza się w komorze chromatograficznej. Jeden koniec płytki zanurzony jest w zlewce z fazą ruchomą, która – dzięki siłom kapilarnym – porusza się przez złoże prostopadle do powierzchni fazy ruchomej. Taki ruch kapilarny jest porównywany do dyfuzji substancji rozpuszczonej w fazie ruchomej pod kątem prostym w stosunku do drogi migracji, więc substancja rozpuszczona ograniczona jest do wąskiej dróżki.
Składniki rozdzielanej mieszaniny chemicznej wiążą się z różną siłą z polarnym adsorbentem. Następnie są wymywane za pomocą rozpuszczalnika, który pełni funkcje fazy ruchomej.
Wraz z polarnością badanej substancji, wzrasta wiązanie się ich z fazą stałą, czego efektem jest trudniejsze wymywanie substancji chemicznych przez eluent. Natomiast wraz ze wzrostem polarności fazy ruchomej następuje wzrost blokowania przez niego polarnych centrów aktywnych fazy stałej, co zmniejsza „opory” przesuwania się wymywanych substancji.
Zalety TLC
Stosowana jest do wstępnego doboru faz dla układów kolumnowych, ponieważ zużycie rozpuszczalników, w porównaniu z chromatografią kolumnową, jest znacznie mniejsze.
Możliwość przechowywania płytek z rozdzielonymi substancjami.
Na jednej warstwie chromatograficznej można równocześnie rozdzielać kilka różnych próbek.
Pozwala określić stopień rozdzielenia substancji na każdym etapie rozwijania chromatogramu i przerwać ten proces w dowolnym momencie.
W przypadku kolumny chromatograficznej, zarówno detekcja składników, jak i ocena stopnia ich rozdzielenia możliwe są dopiero, gdy związki te opuszczą kolumnę.
Chromatografia bibułowa
Wyżej została omówiona chromatografia cienkowarstwowa (TLC), gdzie fazą stacjonarną jest żel krzemionkowy lub tlenek glinu naniesiony na płytkę. Chromatografia bibułowa jest historycznie starszą i technicznie prostszą wersją chromatografii odbywającej się na płaszczyźnie.
Główna i w zasadzie jedyna fundamentalna różnica polega na fazie stacjonarnej. W TLC była to cienka warstwa adsorbentu umieszczonego na płytce, a w chromatografii bibułowej fazą stacjonarną jest po prostu pasek specjalnej, wysokiej jakości bibuły filtracyjnej, która zbudowana jest głównie z celulozy.
Przebieg procesu jest analogiczny do TLC:
Mieszaninę nanosi się w postaci kropki na linię startową paska bibuły.
Pasek umieszcza się pionowo w zamkniętej komorze chromatograficznej, tak aby jego dolny brzeg był zanurzony w eluencie (fazie ruchomej), ale plamka startowa znajdowała się nad powierzchnią cieczy.
Eluent, dzięki siłom kapilarnym, wspina się po bibule, porywając składniki mieszaniny.
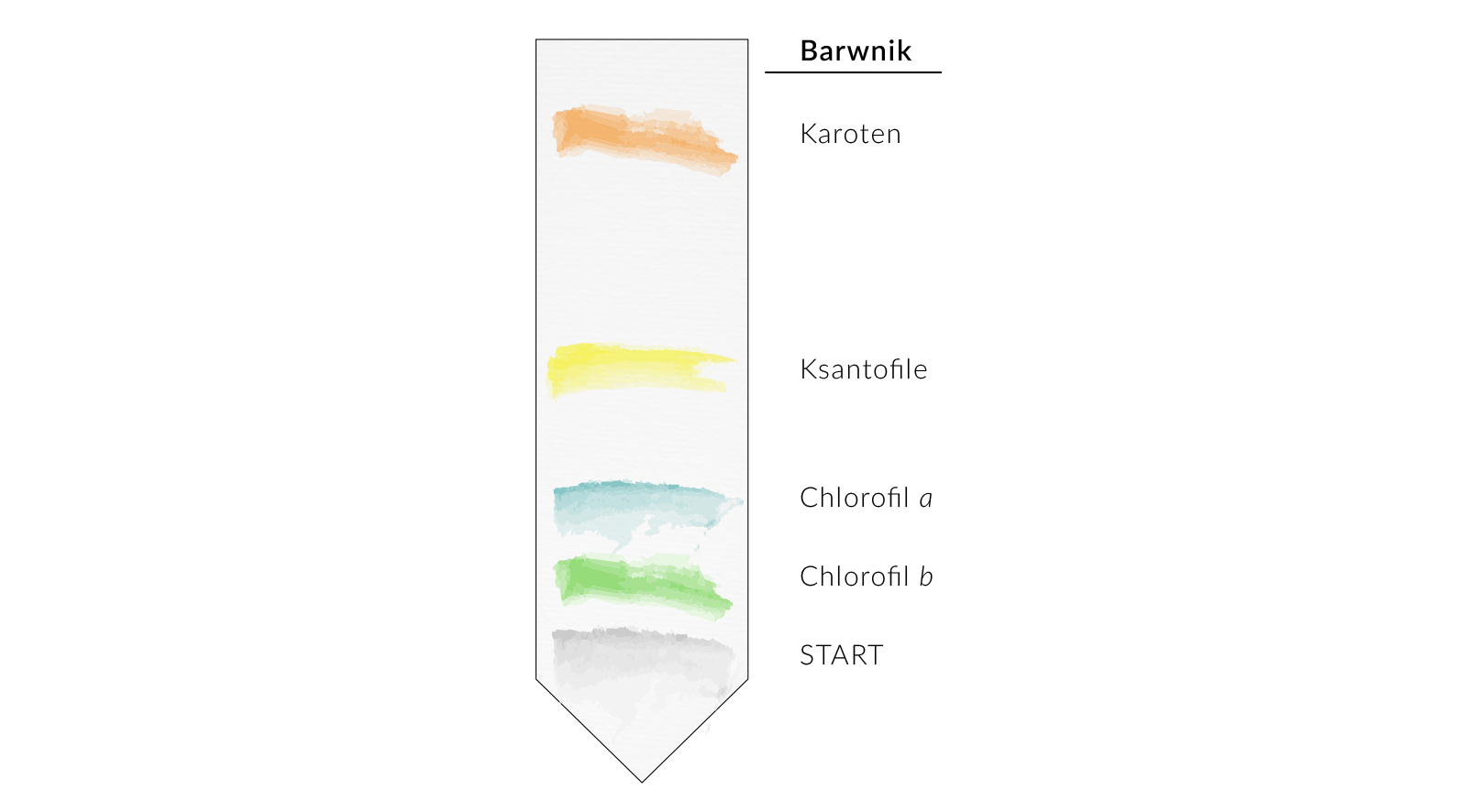
Rozdział następuje identycznie jak w TLC – składniki, które silniej oddziałują z polarną celulozą (fazą stacjonarną), „przylepiają się” do niej mocniej i wędrują wolniej. Składniki, które lepiej rozpuszczają się w fazie ruchomej (eluencie), są przez nią transportowane szybciej i wędrują dalej od linii startu.
Chromatografia bibułowa jest tańsza i łatwiejsza w przygotowaniu niż TLC, ale zazwyczaj rozdział trwa dłużej, a uzyskane plamy są bardziej rozmyte (co oznacza mniejszą precyzję i rozdzielczość).
Przeprowadź doświadczenie w laboratorium biologicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje wyniki, a następnie sformułuj wnioski.
Temat:
Rozdział barwników fotosyntetycznych metodą chromatografii cieczowej z użyciem bibuły filtracyjnej (chromatografii bibułowej)
Problem badawczy:
Jakie barwniki fotosyntetyczne występują w liściach szpinaku?
Hipoteza:
W liściach szpinaku występują: chlorofil oraz dodatkowe barwniki fotosyntetyczne z grupy karotenoidów.
Materiał biologiczny:
liście szpinaku
Odczynniki:
5 ml 96% etanolu
10 ml benzyny ekstrakcyjnej
2,5 ml eteru
2 ml acetonu
Sprzęt laboratoryjny:

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBZS7XUC6
Co kryje się pod skrótowcami HPLC oraz GC?
Co kryje się pod skrótowcami HPLC oraz GC? Czym jest chromatografia?

Film dostępny pod adresem /preview/resource/RzNbZhY6v1dB7
Film nawiązujący do treści materiału - wyjaśnia znaczenie skrótowców HPLC i GC.
Uzupełnij podsumowanie dotyczące chromatografii gazowej i wysokosprawnej chromatografii cieczowej.
HPLC (z ang. 1. high performance, 2. liquid, 3. cieczowa, 4. wysokosprawna, 5. high pressure, 6. gazowa, 7. wysokociśnieniowa, 8. gas 1. high performance, 2. liquid, 3. cieczowa, 4. wysokosprawna, 5. high pressure, 6. gazowa, 7. wysokociśnieniowa, 8. gas chromatography) czyli 1. high performance, 2. liquid, 3. cieczowa, 4. wysokosprawna, 5. high pressure, 6. gazowa, 7. wysokociśnieniowa, 8. gas chromatografia 1. high performance, 2. liquid, 3. cieczowa, 4. wysokosprawna, 5. high pressure, 6. gazowa, 7. wysokociśnieniowa, 8. gas
Podział pomiędzy fazę stacjonarną i ruchomą polega na różnicach w temperaturach 1. topnienia, 2. stacjonarnej, 3. gorzej, 4. lepiej, 5. wrzenia, 6. bardziej, 7. mniej, 8. ruchomej badanych substancji.
Bardziej lotne składniki mieszaniny 1. topnienia, 2. stacjonarnej, 3. gorzej, 4. lepiej, 5. wrzenia, 6. bardziej, 7. mniej, 8. ruchomej rozpuszczają się w fazie 1. topnienia, 2. stacjonarnej, 3. gorzej, 4. lepiej, 5. wrzenia, 6. bardziej, 7. mniej, 8. ruchomej (gazowej) i wcześniej pojawiają się na wyjściu z kolumny. 1. topnienia, 2. stacjonarnej, 3. gorzej, 4. lepiej, 5. wrzenia, 6. bardziej, 7. mniej, 8. ruchomej lotne składniki mieszaniny będą wykazywać lepszą rozpuszczalność w fazie 1. topnienia, 2. stacjonarnej, 3. gorzej, 4. lepiej, 5. wrzenia, 6. bardziej, 7. mniej, 8. ruchomej.
Fazą 1. stacjonarną, 2. ruchomą, 3. wzrasta, 4. większy, 5. mniejszy, 6. maleje jest ciecz podawana pod wysokim ciśnieniem, natomiast fazą 1. stacjonarną, 2. ruchomą, 3. wzrasta, 4. większy, 5. mniejszy, 6. maleje jest substancja stała bazująca na krzemionce. Im 1. stacjonarną, 2. ruchomą, 3. wzrasta, 4. większy, 5. mniejszy, 6. maleje rozmiar ziaren fazy stacjonarnej, tym większa jest jej powierzchnia, co sprawia, że skuteczność tej metody 1. stacjonarną, 2. ruchomą, 3. wzrasta, 4. większy, 5. mniejszy, 6. maleje.