Czy odczyn wszystkich soli jest obojętny?
Wodne roztwory kwasów mają odczyn kwasowy, a wodne roztwory zasad – zasadowy. A jaki odczyn mają wodne roztwory soli?
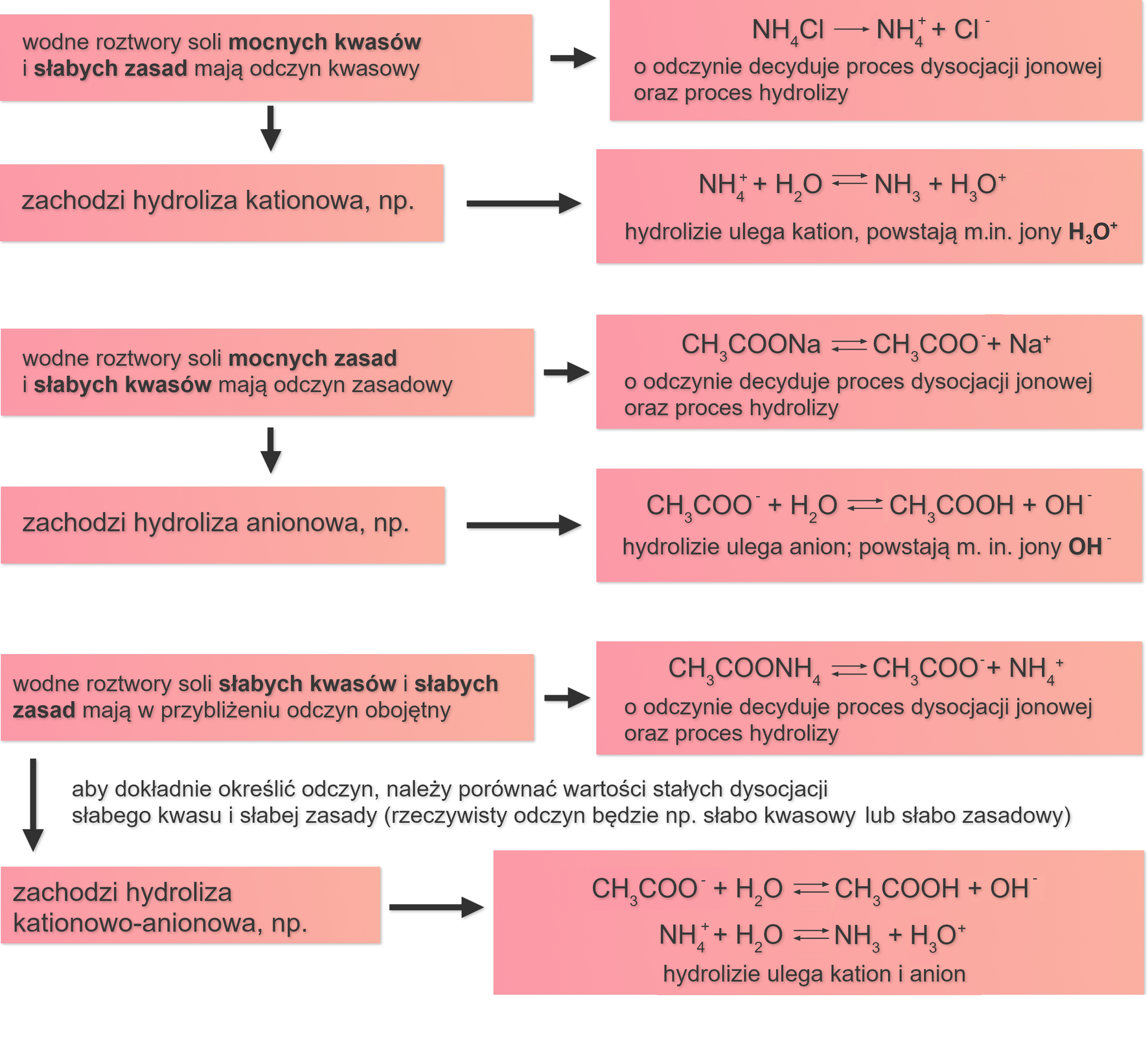
Przeanalizuj poniższy schemat hydrolizy wodnych roztworów różnych soli i odpowiedz na powyższe pytanie.
Przeanalizuj opis schematu hydrolizy wodnych roztworów różnych soli i odpowiedz na powyższe pytanie.
Hydroliza | ||
|---|---|---|
hydroliza kationowa – hydrolizie ulega kation | hydroliza anionowa – hydrolizie ulega anion | hydroliza kationowo‑anionowa – hydrolizie ulega kation i anion |
kwasowy odczyn roztworu | zasadowy odczyn roztworu | odczyn zbliżony do obojętnego |
sole pochodzące od mocnych kwasów i słabych zasad | sole pochodzące od mocnych zasad i słabych kwasów | sole pochodzące od słabych zasad i słabych kwasów |
Tabela 1. Hydroliza – podsumowanie
Indeks górny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Warszawa 2010. Indeks górny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Warszawa 2010.
Aby dokładnie określić odczyn, należy porównać wartości stałych dysocjacjistałych dysocjacji słabego kwasu i słabej zasady, np. w przypadku metanianu (mrówczanu) amonu odczyn jego roztworu wodnego jest bardzo słabo kwasowy (pH < 7), ponieważ:
Przeprowadź eksperyment w laboratorium chemicznym. Zapisz problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie sformułuj wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2T9ONL73
Zadanie: Sprawdzenie, czy odczyn wszystkich soli jest obojętny.
Hipoteza: Odczyn soli nie zawsze jest obojętny.
Sprzęt laboratoryjny: zlewka (150 centymetrów sześciennych) - naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych; pH‑metr - urządzenie służące do pomiaru pH analizowanych substancji chemicznych; tryskawka - plastikowe naczynie zamknięte nakrętką z długą końcówką. Tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę; cylinder miarowy - podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy.
Badane substancje to roztwory wodne o stężeniach 1 mol na decymetr sześciennyIndeks górny 33, 0,5 mola na decymetr sześciennyIndeks górny 33 i 0,1 mola na decymetr sześciennyIndeks górny 33, następujących substancji: chlorek sodu, cyjanek sodu, fluorek sodu, wodorosiarczan(VI) sodu, chlorek amonu, fluorek amonu, azotan(III) potasu, siarczan(VI) potasu, węglan potasu, octan amonu, siarczan(IV) sodu.
Instrukcja: Wybrano roztwór do badania i przeniesiono go na blat stołu laboratoryjnego. Wybrano stężenie roztworu. Odmierzono cylindrem miarowym 50 centymetrów sześciennych wybranego roztworu i przenieś go do zlewki. Następnie przy użyciu pH‑metru sprawdzono pH roztworu. Przed i po dokonaniu pomiaru przemyto elektrodę wodą.
Wnioski: Odczyn soli zależy od jej rodzaju. Jeśli sól pochodzi od mocnego kwasu oraz mocnej zasady odczyn będzie obojętny (lub bliski obojętnego). Jeśli sól pochodzi od słabego kwasu i mocnej zasady odczyn będzie zasadowy, jeśli sól pochodzi od mocnego kwasu i słabej zasady to odczyn jest kwasowy. Ostatni przypadek to jeśli sól pochodzi od słabego kwasu i słabej soli to odczyn jest obojętny (lub bliski obojętnego).
Jak na wartość pH wpływa zmiana objętości i zmiana stężenia wodnych roztworów soli?
Czy wiesz, jakie związki ulegają procesowi hydrolizy? Czy wiesz, jak za pomocą równań reakcji zapisać ten proces? Aby poznać odpowiedzi na te pytania, zapoznaj się z poniższym filmem, a następnie rozwiąż ćwiczenia.

Film dostępny pod adresem /preview/resource/RMLAHRXXznLTc
Film nawiązujący do zagadnienia procesu hydrolizy oraz opisania tego procesu równaniami reakcji
Odczyn kwasowy wykazuje wodny roztwór: Możliwe odpowiedzi: 1. chlorku amonu., 2. węglanu sodu., 3. octanu amonu., 4. siarczku potasu.
Wodny roztwór siarczanusześć amonu wykazuje odczyn: Możliwe odpowiedzi: 1. zasadowy., 2. obojętny., 3. kwasowy., 4. słabo kwasowy.
Alkoholowy roztwór fenoloftaleiny przyjmuje malinowe zabarwienie w wodnym roztworze: Możliwe odpowiedzi: 1. chlorku sodu., 2. siarczanusześć potasu., 3. siarczanucztery sodu., 4. chlorku potasu.
Wodny roztwór octanu amonu wykazuje odczyn obojętny, ponieważ: Możliwe odpowiedzi: 1. wartość stałej dysocjacji kwasu octowego jest w przybliżeniu równa wartości stałej dysocjacji amoniaku., 2. sól ta pochodzi od mocnego kwasu i mocnej zasady., 3. wartość stałej dysocjacji kwasu octowego jest mniejsza od wartości stałej dysocjacji amoniaku., 4. wartość stałej dysocjacji kwasu octowego jest większa od wartości stałej dysocjacji amoniaku.
Wodny roztwór węglanu sodu wykazuje odczyn zasadowy, ponieważ: Możliwe odpowiedzi: 1. jest to sól pochodząca od słabego kwasu i mocnej zasady., 2. jest to sól pochodząca od mocnego kwasu i słabej zasady., 3. jest to sól pochodząca od słabego kwasu i słabej zasady., 4. jest to sól pochodząca od mocnego kwasu i mocnej zasady.
Papierek uniwersalny przyjmuje czerwone zabarwienie w wodnym roztworze: Możliwe odpowiedzi: 1. chlorku amonu., 2. chlorku sodu., 3. chlorku potasu., 4. chlorku baru.