Czy stała równowagi jest zależna od temperatury?
Stała równowagi reakcji
Wraz ze zmianą temperatury obserwuje się zmianę stałej równowagi . W zależności od tego, jakiego typu jest reakcja, endotermicznaendotermiczna czy egzotermicznaegzotermiczna, obserwuje się odpowiednie zmiany wartości .
Należy pamiętać, że stała równowagi jest wartością bezwymiarową.
Zależność stałej równowagi od temperatury określa równanie:
gdzie:
– stała równowagi;
– stała charakterystyczna dla danej reakcji;
– ciepło reakcji ;
- stała gazowastała gazowa odpowiadająca wartości 8,314510 ;
- temperatura [K].
Reakcje egzotermiczne
W reakcjach egzotermicznych obserwujemy wydzielenie ciepła w trakcie reakcji. Schematycznie możemy to zapisać jako:
gdzie jako oznaczamy ciepło.
Wydzielanie ciepła z układu oznacza jego utratę. W tym wypadku wartość przyjmuje wartości ujemne. Po podstawieniu ujemnej wartości do równania:
zaobserwujemy wzrost wartości lnK wraz ze spadkiem temperatury.
W reakcjach egzotermicznych podwyższenie temperatury doprowadza do obniżenia wartości stałej . W przypadku obniżenia temperatury – wartość stałej rośnie. Taką zależność prezentuje poniższy wykres.
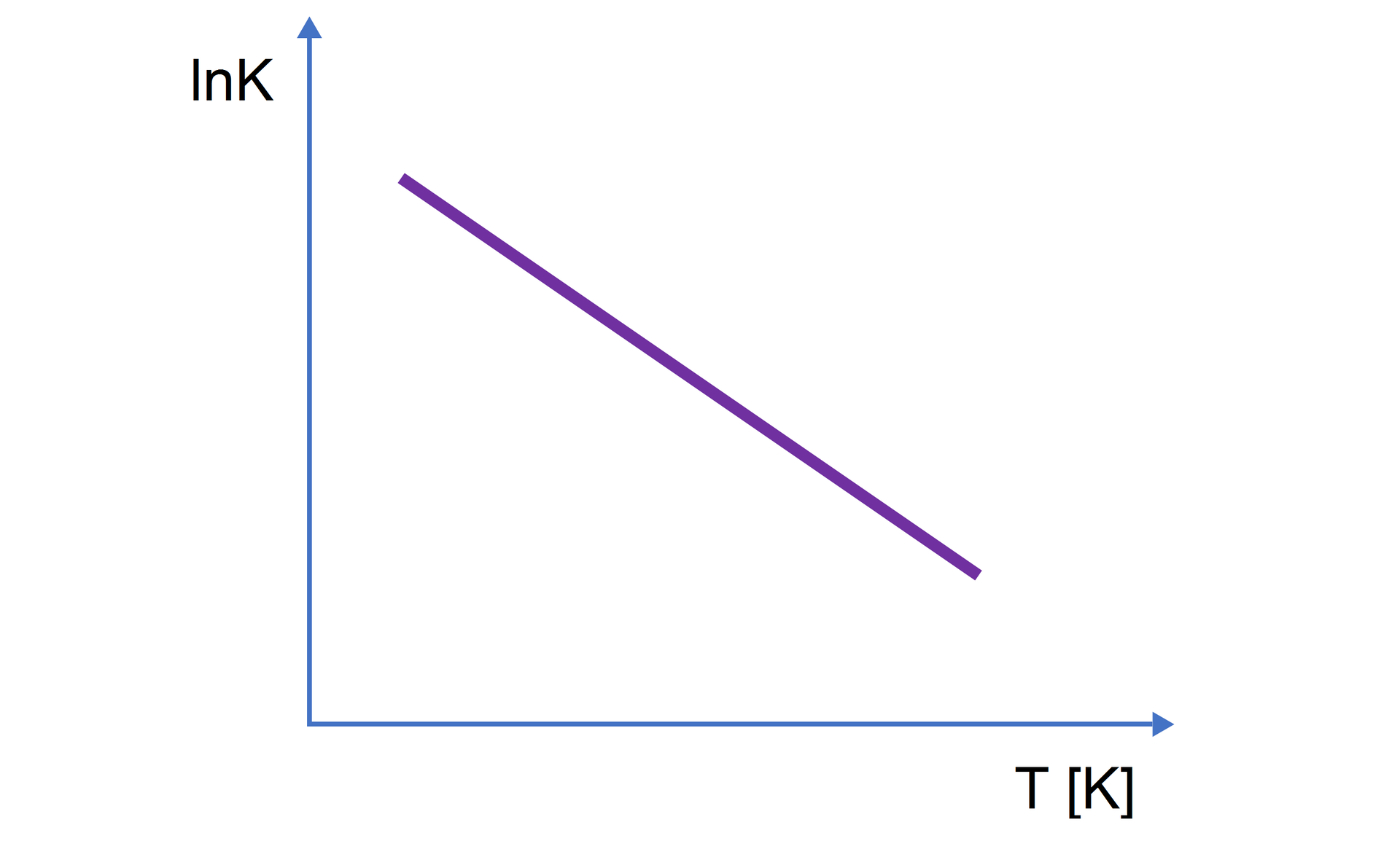
Wraz ze wzrostem temperatury obserwujemy obniżenie wartości logarytmu ze stałej równowagi .
Reakcje endotermiczne
W reakcjach endotermicznych, aby zaszła reakcja, należy dostarczyć ciepła. Schematycznie możemy to zapisać jako:
gdzie jako oznaczamy ciepło.
Pobieranie ciepła do układu oznacza jego przyrost. W tym wypadku wartość przyjmuje wartości dodatnie. Po podstawieniu dodatniej wartości do równania:
zaobserwujemy wzrost wartości lnK wraz ze wzrostem temperatury.
W reakcjach endotermicznych podwyższenie temperatury doprowadza do podwyższenia wartości stałej . W przypadku obniżenia temperatury wartość stałej maleje. Zależność taką prezentuje poniższy wykres.
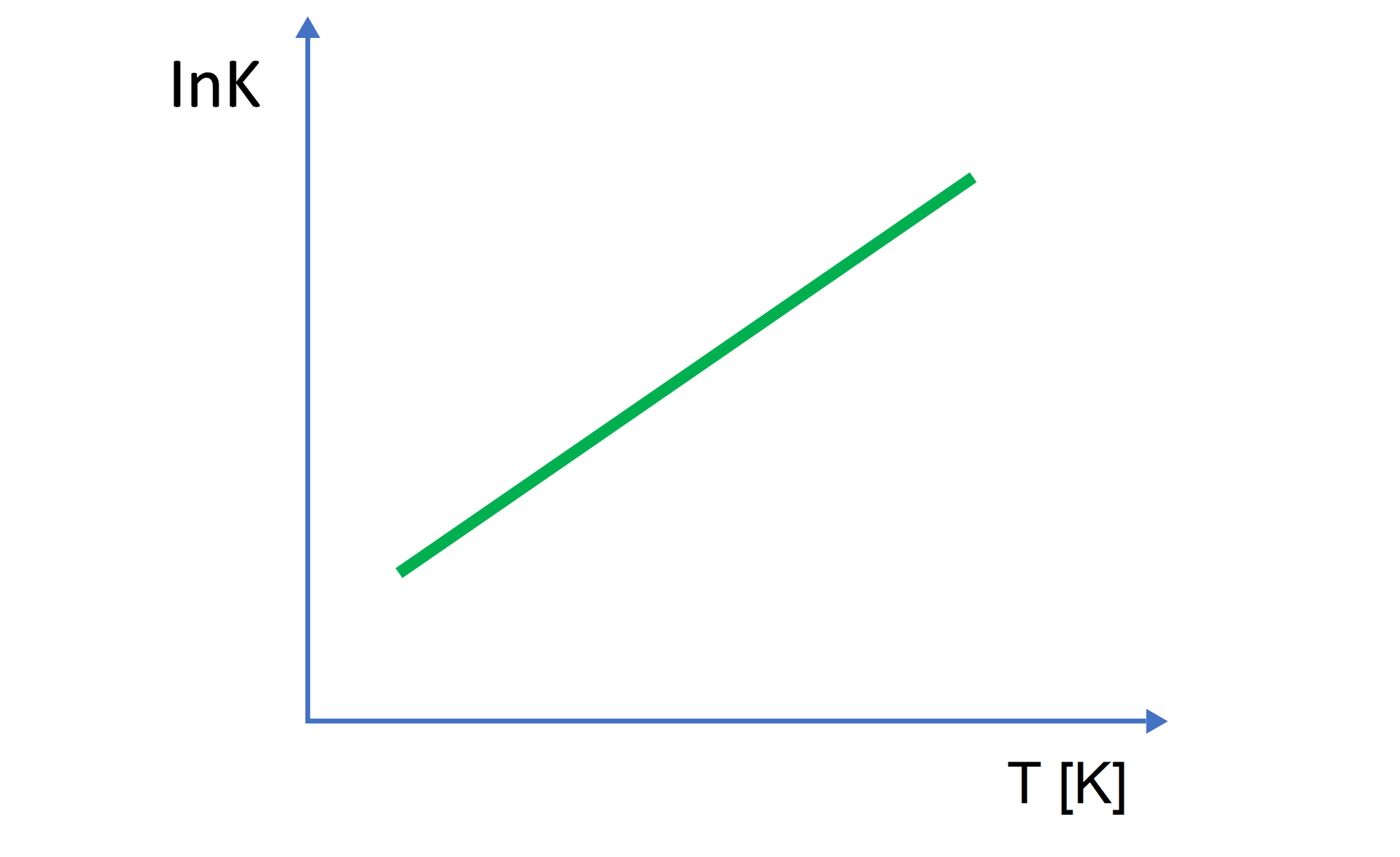
Wraz ze wzrostem temperatury obserwujemy podwyższenie wartości logarytmu ze stałej równowagi .
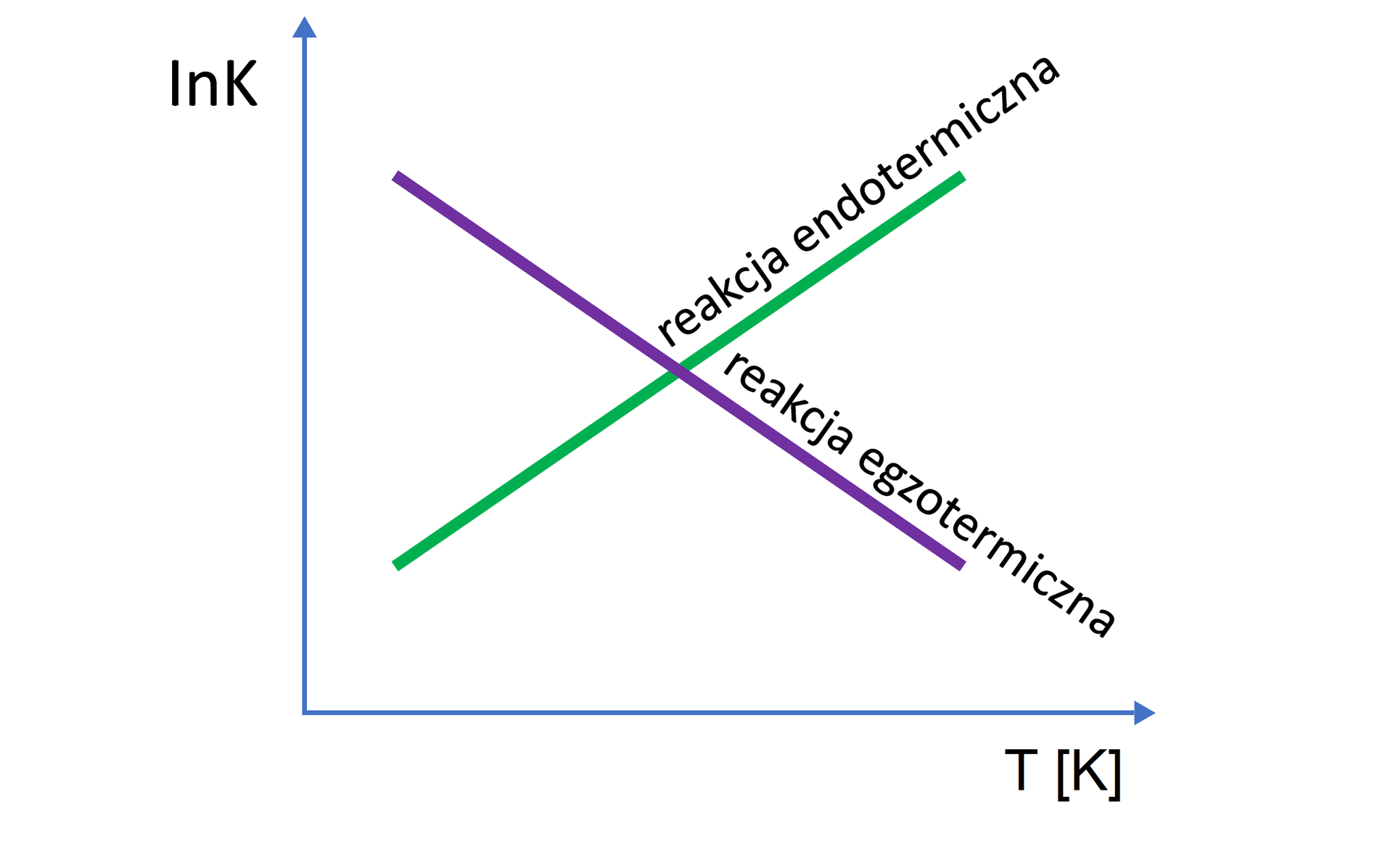
Zapoznaj się z filmem samouczkiem, w którym dowiesz się, czy stała równowagi jest zależna od temperatury. Zwróć uwagę na wykresy zależności stałej równowagi od temperatury w reakcjach endo- i egzotermicznych. Na podstawie informacji zawartych w filmie rozwiąż ćwiczenia, które znajdują się poniżej. W razie problemów z rozwiązaniem – zapoznaj się z filmem ponownie.

Film dostępny pod adresem /preview/resource/R8lscT753uuT1
Film nawiązujący do treści materiału - dotyczy stałej równowagi chemicznej i jej zależności od temperatury. Film wyjaśnia, jak zmienia się wartość stałej równowagi w reakcji endo- i egzoenergetycznej.
dwa N O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
Jeśli obniżymy temperaturę układu wartość stałej dysocjacji : Możliwe odpowiedzi: 1. wzrośnie, 2. zmaleje, 3. nie zmieni się, 4. nie można określić wpływu temperatury na wartość stałej równowagi tej reakcji
trzy H indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, N indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N H indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
jeśli zwiększymy temperaturę panującą w układzie: Możliwe odpowiedzi: 1. wzrośnie, 2. zmaleje, 3. nie zmieni się, 4. nie można określić wpływu temperatury na wartość stałej równowagi tej reakcji