Jak na stan równowagi wpływa temperatura?
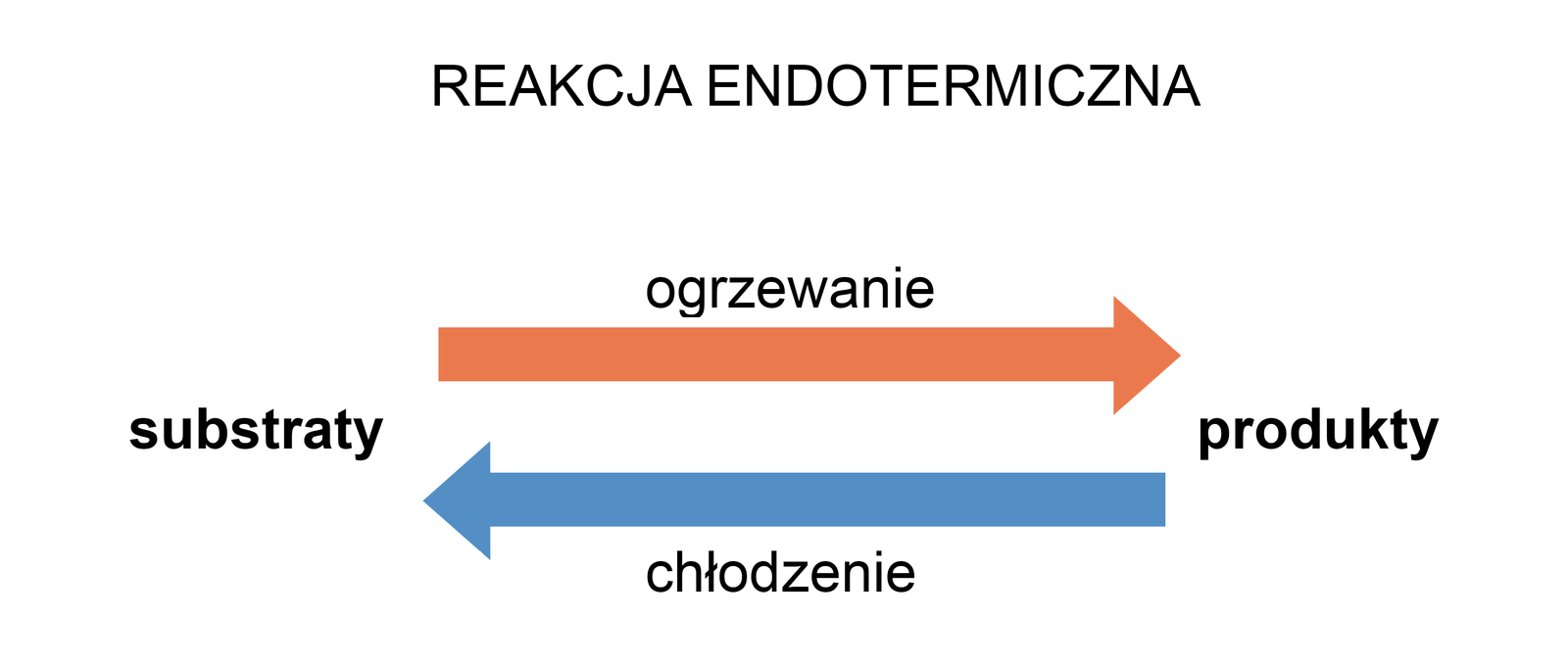
Reakcja endotermiczna
Reakcje chemiczne możemy podzielić na reakcje endotermicznereakcje endotermiczne, które potrzebują ciepła oraz egzotermiczneegzotermiczne, które to ciepło oddają. Schematycznie traktując ciepło „Q”, jako jeden z reagentów, omówimy wpływ temperatury na stan równowagi.
Przeanalizujmy hipotetyczną reakcję przebiegającą zgodnie z poniższym równaniem:
Oznaczając ciepło „Q”, zapisujemy je po stronie substratów jako jeden z elementów reakcji. W ten sposób uzyskamy zapis:
Przyjmijmy, że w układzie ustalił się już stan równowagi. W takiej sytuacji, podnosząc temperaturę, dostarczamy do układu ciepło (Q), które pełni rolę substratu. Układ zostaje zatem wytrącony ze stanu równowagi. Aby przywrócić ów stan, rozpoczyna się proces, w czasie którego układ działa „na przekór” i zużywa dostarczone ciepło. W takiej sytuacji stan równowagi przesunie się w stronę syntezy związku C.
Gdy z kolei zaczniemy ochładzać układ znajdujący się w stanie równowagi, to odbieranie ciepła będzie równoznaczne z odbieraniem jednego z substratów. Wytrącony w ten sposób ze stanu równowagi układ zaczyna odbierane przez nas ciepło odtwarzać. W ten sposób stan równowagi przesuwa się w stronę syntezy związków A i B.
Reakcja rozkładu pary wodnej na pierwiastki jest reakcją endotermiczną. Zakładając, że reakcja biegnie w układzie zamkniętym przy p, V=const, zapisz odpowiednie równanie reakcji, uwzględniając w nich ciepło (oznacz je literą Q). Napisz, jak na położenie stanu równowagi wpłynie ogrzewanie i ochładzanie układu.
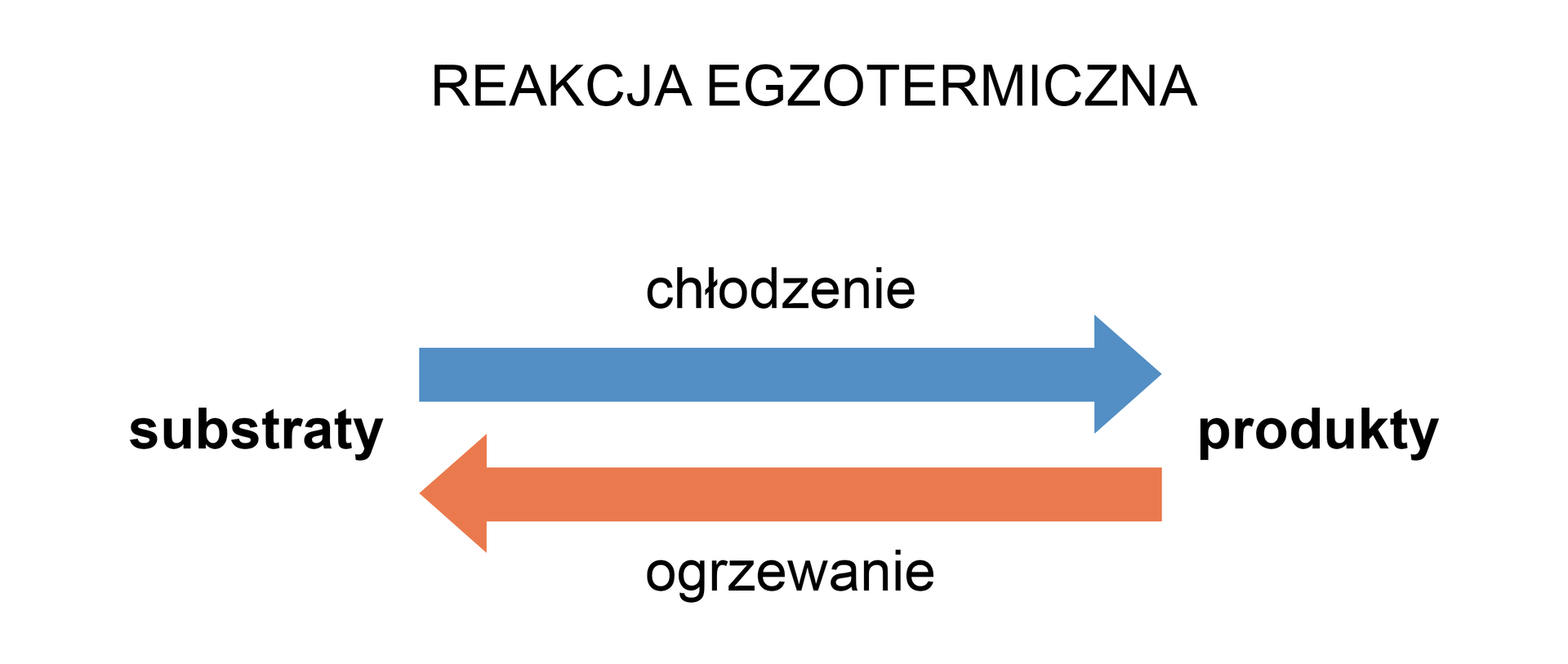
Reakcja egzotermiczna
Przeanalizujmy hipotetyczną reakcję:
Oznaczając ciepło „Q”, zapisujemy je po stronie produktów jako jeden z elementów reakcji. W ten sposób uzyskamy zapis:
Przeanalizujmy, co się stanie, jeśli układ, w którym ustalił się już stan równowagi, zaczniemy ogrzewać. Układ zaczyna powracać do stanu równowagi, czyli obniżenia temperatury. Zgodnie z regułą przekory, stan równowagi przesunie się w stronę rozkładu związku C – rozkład C to proces zużywający dostarczane przez nas ciepło.
Gdy zaś zaczniemy ochładzać układ znajdujący się w stanie równowagi, odbierzemy z układu ciepło (Q). Układ znów zacznie dążyć do stanu równowagi i zacznie się proces wytwarzający ciepło. Zgodnie z regułą przekory, stan równowagi przesunie się w kierunku produktów.
Reakcja spalania metanu w tlenie do tlenku węgla(IV) i wody jest reakcją egzotermiczną. Zakładając, że reakcja biegnie w układzie zamkniętym przy p, V=const, zapisz odpowiednie równanie reakcji, uwzględniając w nich ciepło (oznacz je literą Q). Napisz, jak na położenie stanu równowagi wpłynie ogrzewanie i ochładzanie układu.
Podsumowując, trzeba zaznaczyć, że każda zmiana temperatury w reakcjach egzotermicznych i endotermicznych powoduje przesunięcie położenia równowagi. W przypadku reakcji endotermicznych, dostarczenie ciepła przesuwa stan równowagi w kierunku syntezy produktów. Ochłodzenie układu wywołuje skutek odwrotny, czyli przesunięcie stanu równowagi w kierunku substratów. W przypadku reakcji egzotermicznych, dostarczenie ciepła przesuwa stan równowagi w kierunku substratów, a ochłodzenie układu w kierunku produktów.
Zapoznaj się z filmem samouczkiem, w którym dowiesz się, jak na zmianę położenia stanu równowagi odwracalnej reakcji chemicznej wpływa temperatura. Zwróć uwagę, jak wówczas zmienia się kierunek zmiany stanu równowagi w reakcjach endotermicznych i egzotermicznych. Na podstawie informacji zamieszczonych w filmie, rozwiąż ćwiczenia zamieszczone poniżej.

Film dostępny pod adresem /preview/resource/RfSPuUisFwxGI
Film nawiązujący do treści materiału - wyjaśnia, jak temperatura wpływa na stan równowagi reakcji endotermicznej i egzotermicznej.
N indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, trzy H indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N H indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
Wzrost wydajności reakcji spowoduje : Możliwe odpowiedzi: 1. wzrost temperatury, 2. spadek temperatury, 3. użycie katalizatora, 4. użycie inhibitora
dwa H indeks dolny, dwa, koniec indeksu dolnego, S indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, trzy O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa S O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, dwa H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
Możliwe odpowiedzi: 1. spowodujemy przesunięcie położenia stanu równowagi w kierunku substratów, 2. spowodujemy przesunięcie położenia stanu równowagi w kierunku produktów, 3. wzrost wydajności tej reakcji, 4. nie dojdzie do żadnej zmiany położenia stanu równowagi