Jak na stan równowagi wpływa ciśnienie?
Czym jest stała równowagi?
W każdej odwracalnej reakcji chemicznejodwracalnej reakcji chemicznej może ustalić się stan równowagi.
Jest on opisywany przez wartość stałej równowagi Kstałej równowagi K, która to z kolei jest równa ilorazowi reakcji w stanie doskonałej równowagi, tj. w sytuacji, gdy szybkość reakcji, w stronę od substratów do produktów i od produktów do substratów, jest dokładnie taka sama. Stała K jest przypisana dla konkretnych wartości temperatury oraz ciśnienia. Czynniki zewnętrzne mogą przesuwać stan równowagi w stronę produktów lub substratów.
Jak ciśnienie wpływa na położenie stanu równowagi?
W tej części rozważymy wpływ ciśnienia na położenie stanu równowagi.
Reakcja syntezy – kiedy z kilku substratów powstaje jeden produkt
Rozważmy hipotetyczną reakcję:
Wszystkie reagenty są w stanie gazowym, przy stałym ciśnieniu i temperaturze. Bilansując (uzgadniając) równanie reakcji zauważymy, że liczba moli substratów (4 mole) jest różna od ilości moli produktów (dwa mole). Synteza związku powoduje zmniejszenie się ilości reagentów. Zakłócenie stanu równowagi, poprzez zwiększenie ciśnienia, przesunie równowagę w stronę syntezy produktu, ponieważ układ dąży do powrotu do stanu równowagi. Zmniejszenie ciśnienia natomiast będzie miało skutek odwrotny – przesunięcie równowagi w stronę substratów.
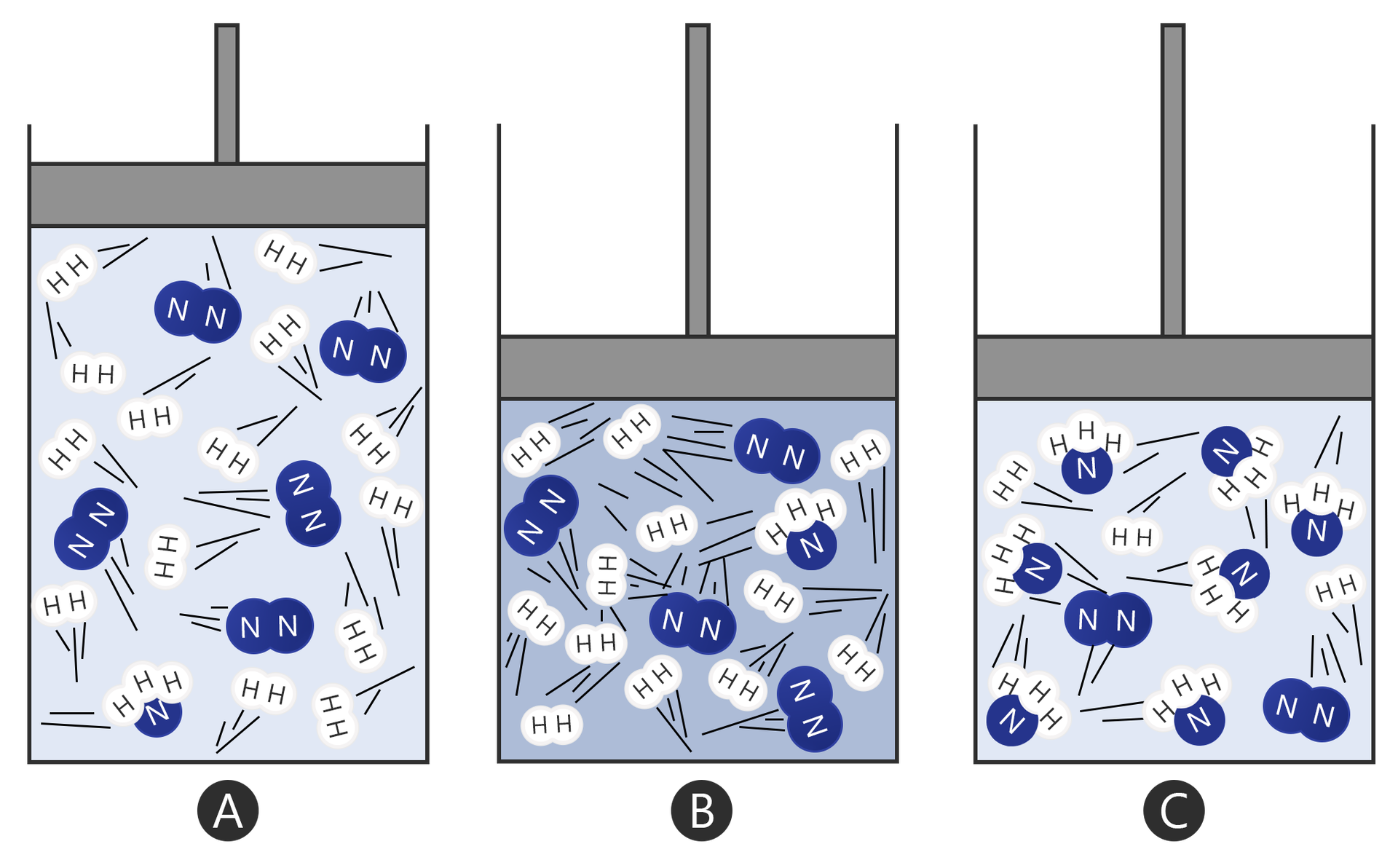
B) Poprzez opuszczenie tłoka zwiększa się ciśnienie w układzie. Cząsteczki zaczynają poruszać się szybciej, przez co prawdopodobieństwo ich zderzenia jest większe, a tym samym także zajścia reakcji.
C) Ustala się stan równowagi. Przeważają głównie cząsteczki produktu.

Podwyższenie ciśnienia wodoru oraz azotu w reaktorach powoduje zwiększenie wydajności procesu syntezy amoniaku do około 30%. MetodęMetodę syntezy amoniaku opracował niemiecki fizykochemik, Fritz Haber, za co w 1918 r. otrzymał nagrodę Nobla. Współcześnie ocenia się, że nawozy azotowe, produkowane przy użyciu tej metody, są odpowiedzialne za produkcję żywności, która utrzymuje przy życiu ok. jedną trzecią ludzkości. Wytwarzanie amoniaku jest procesem bardzo energochłonnym – produkcja 1 t bezwodnego amoniaku pochłania 1000–1250 gazu ziemnego. Na wytwarzanie amoniaku zużywa się ok. 5% światowej produkcji gazu ziemnego i ok. 2% energii.
Reakcja analizy – kiedy z jednego substratu powstaje kilka produktów
Rozważmy hipotetyczną reakcję:
Wszystkie reagenty są w stanie gazowym przy stałym ciśnieniu i temperaturze. Bilansując (uzgadniając) równanie reakcji zauważymy, że liczba moli substratów jest różna od ilości moli produktów. Poprzez rozkład związku A otrzymuje się dwa mole produktów, co powoduje zwiększenie ilości reagentów. Zakłócenie stanu równowagi reakcji przez zmniejszenie ciśnienia powoduje przesunięcie równowagi w kierunku produktów. Zmiana ciśnienia w drugą stronę powoduje skutek odwrotny – przesunięcie równowagi w kierunku substratów.
Reakcja bez zmiany objętości
Rozważmy hipotetyczną reakcję:
Wszystkie reagenty są w stanie gazowym, przy stałym ciśnieniu i temperaturze. Bilansując równanie reakcji zauważymy, że liczba moli substratów jest równa liczbie moli produktów. W wyniku reakcji z dwóch moli substratów powstają dwa mole produktów. W związku z czym nie zmienia się objętość reagentów, a co za tym idzie – zmiana ciśnienia nie powoduje przesunięcia stanu równowagi.
Reakcje dwufazowe
Rozważmy hipotetyczną reakcję:
Reagenty są w stanie stałym oraz gazowym. Po stronie produktów są trzy mole gazu (dwa mole C i jeden mol D). Zakłócenie stanu równowagi przez zwiększenie ciśnienia przesunie równowagę w stronę syntezy produktu. Z kolei zmniejszenie ciśnienia będzie miało skutek odwrotny – przesunięcie równowagi w stronę substratów.
Reakcje z inertnym indywiduum w formie gazowej
Wprowadzenie do układu reakcyjnego gazu inertnegogazu inertnego powoduje zmniejszenie stężenia reagentów w układzie. Z tego względu maleją również ciśnienia cząstkoweciśnienia cząstkowe, a co za tym idzie – zmniejsza się ciśnienie ogólne w układzie. Dlatego dodanie gazu inertnego powoduje przesunięcie stanu równowagi tak samo, jak obniżenie ciśnienia ogólnego. Jest on zatem korzystny dla reakcji analizy, natomiast niekorzystny dla reakcji syntezy.
Zapoznaj się z filmem samouczkiem, w którym dowiesz się, jak na stan równowagi wpływa ciśnienie. Zwróć uwagę na kierunek zmiany stanu równowagi na skutek zmiany ciśnienia, gdy reakcja przebiega ze wzrostem lub spadkiem objętości. Na podstawie informacji zawartych w filmie rozwiąż poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/REjjNTg5WnYrs
Film nawiązujący do treści materiału - dotyczy wpływu ciśnienia na stan równowagi chemicznej oraz warunków, które muszą być spełnione.
dwa H indeks dolny, dwa, koniec indeksu dolnego, S indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, trzy O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa S O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, dwa H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego
jeśli zostanie zwiększone ciśnienie panujące w układzie : Możliwe odpowiedzi: 1. w prawo, 2. w lewo, 3. nie przesunie się, 4. nie można tego określić dla tej reakcji
N indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego
jeśli zostanie zwiększone ciśnienie panujące w układzie : Możliwe odpowiedzi: 1. przesunie się w kierunku tworzenia produktów, 2. przesunie się w kierunku substratów, 3. nie zmieni się położenie stanu równowagi, 4. nie można tego określić dla tej reakcji
dwa C O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa C O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego
podwyższenie ciśnienia panującego w układzie : Możliwe odpowiedzi: 1. spowoduje wzrost wydajności reakcji, 2. spowoduje spadek wydajności reakcji, 3. nie wpłynie na wydajność reakcji, 4. spowoduje przesunięcie położenia stanu równowagi w kierunku produktów