Wpływ stężenia reagentów na stan równowagi
Reguła przekory a stężenie reagenta
Jednym z wyzwań przemysłu chemicznego jest osiągnięcie wysokiej wydajności produktów.
W związku z tym, zadaniem chemików jest manipulowanie warunkami reakcji w taki sposób, aby równowaga reakcjirównowaga reakcji była przesunięta w stronę tworzenia produktów. Do tego celu wykorzystywana jest reguła przekory, a jednym z czynników, który ułatwia powstawanie produktów, jest zmiana stężenia reagentów reakcji.
Czy manipulowanie stężeniem reagentów zawsze zwiększa wydajność reakcji?
Załóżmy, że zachodzi reakcja odwracalnareakcja odwracalna substancji A z substancją B, w wyniku której powstaje związek AB:
W stanie równowagi wyrażenie na stałą równowagistałą równowagi (KIndeks dolny cc) przyjmuje postać:
![Ilustracja przedstawia wzór: K C = [ A B ] [ A ] ⋅ [ B ] . AB znajduje się w czerwonym kole, A w zielonym, B w niebieskim. Koła są tej samej wielkości. Legenda: czerwone koło to stężenie związku AB w stanie równowagi. Zielone koło to stężenie substancji A w stanie równowagi. Niebieskie koło oznacza stężenie substancji B w stanie równowagi.](https://static.zpe.gov.pl/portal/f/res-minimized/RAYxfys89Wn9w/1616760049/1PH5y8s8uLboKn2rvVLMVjTKBiWyMCxz.png)
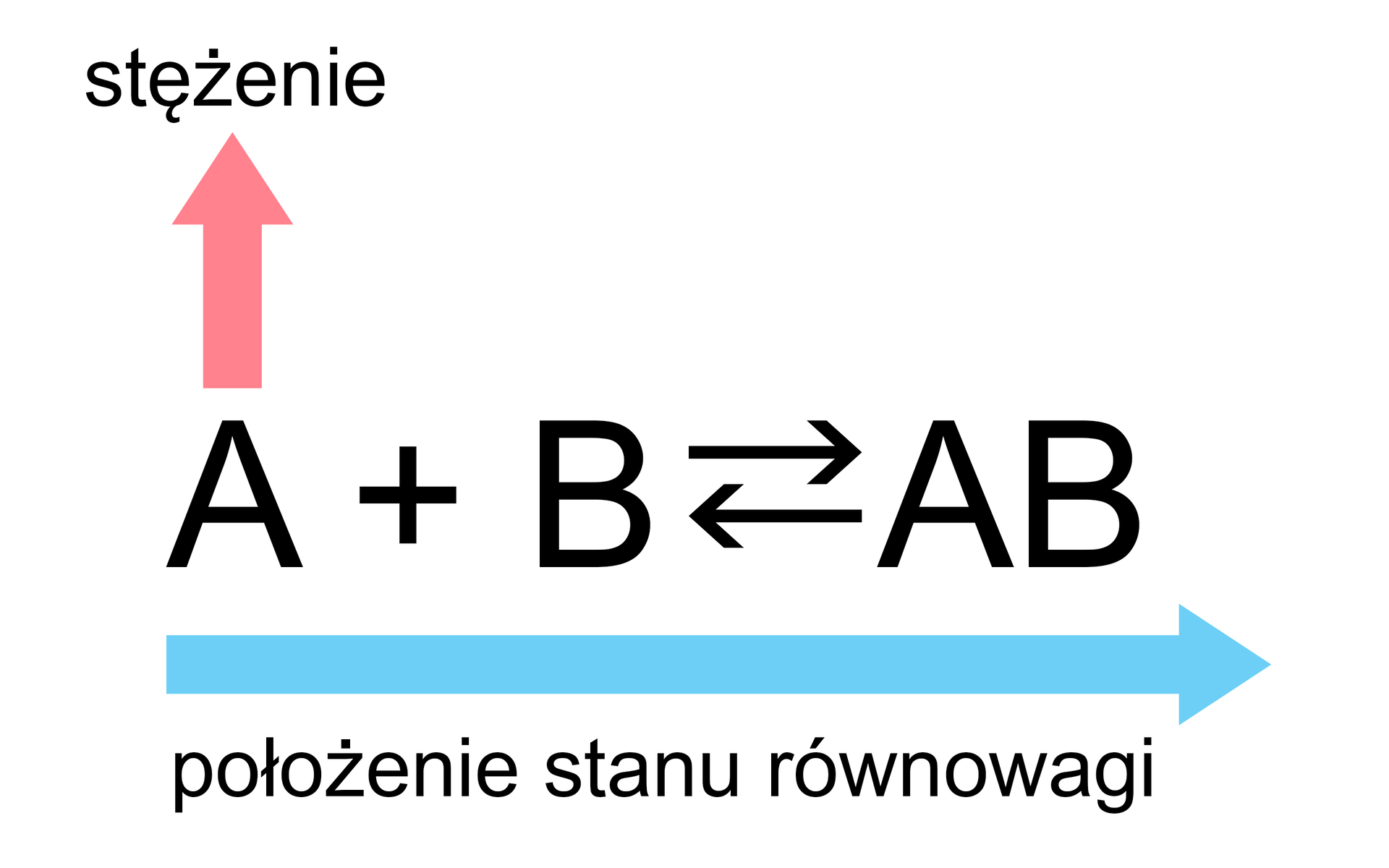
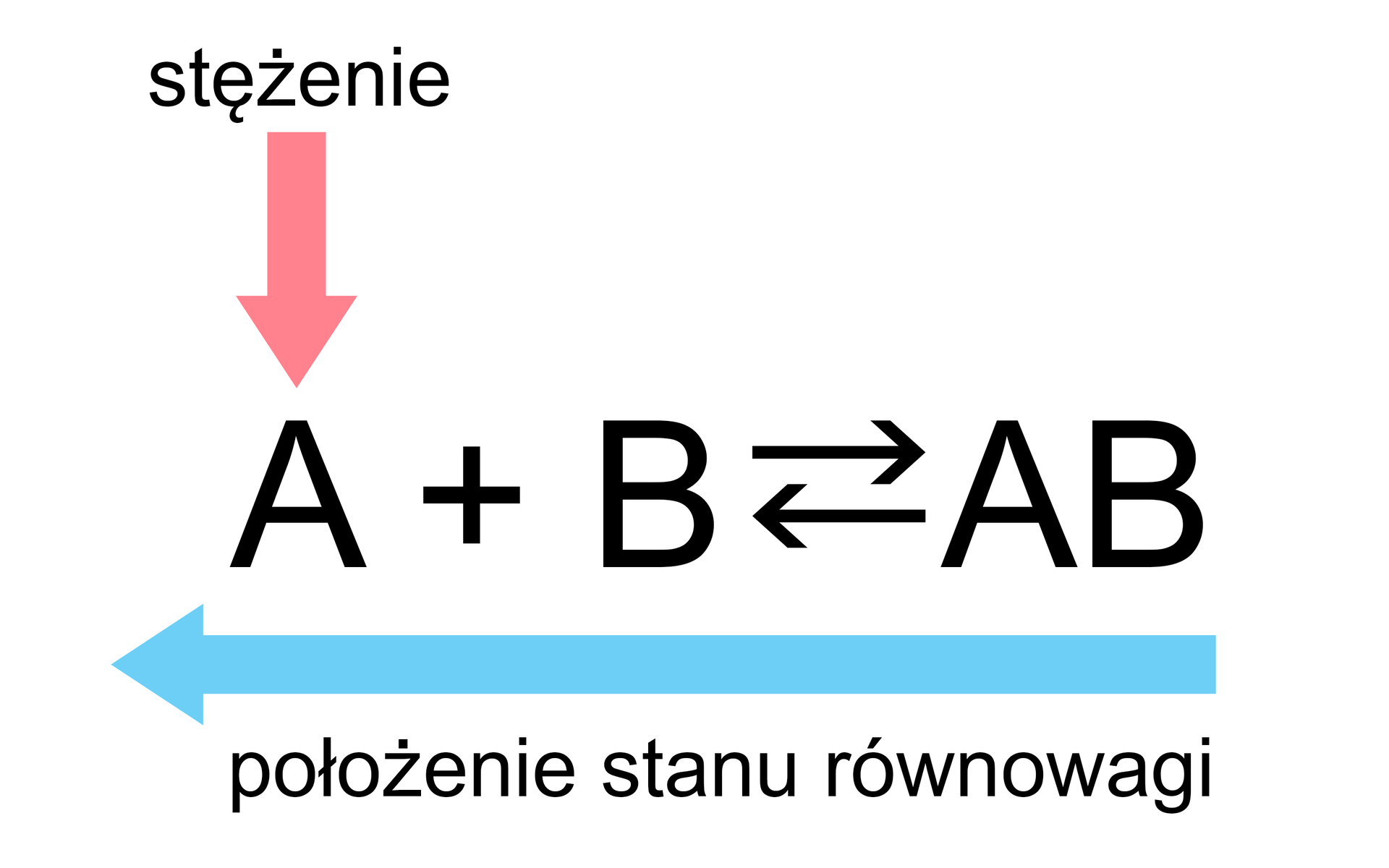
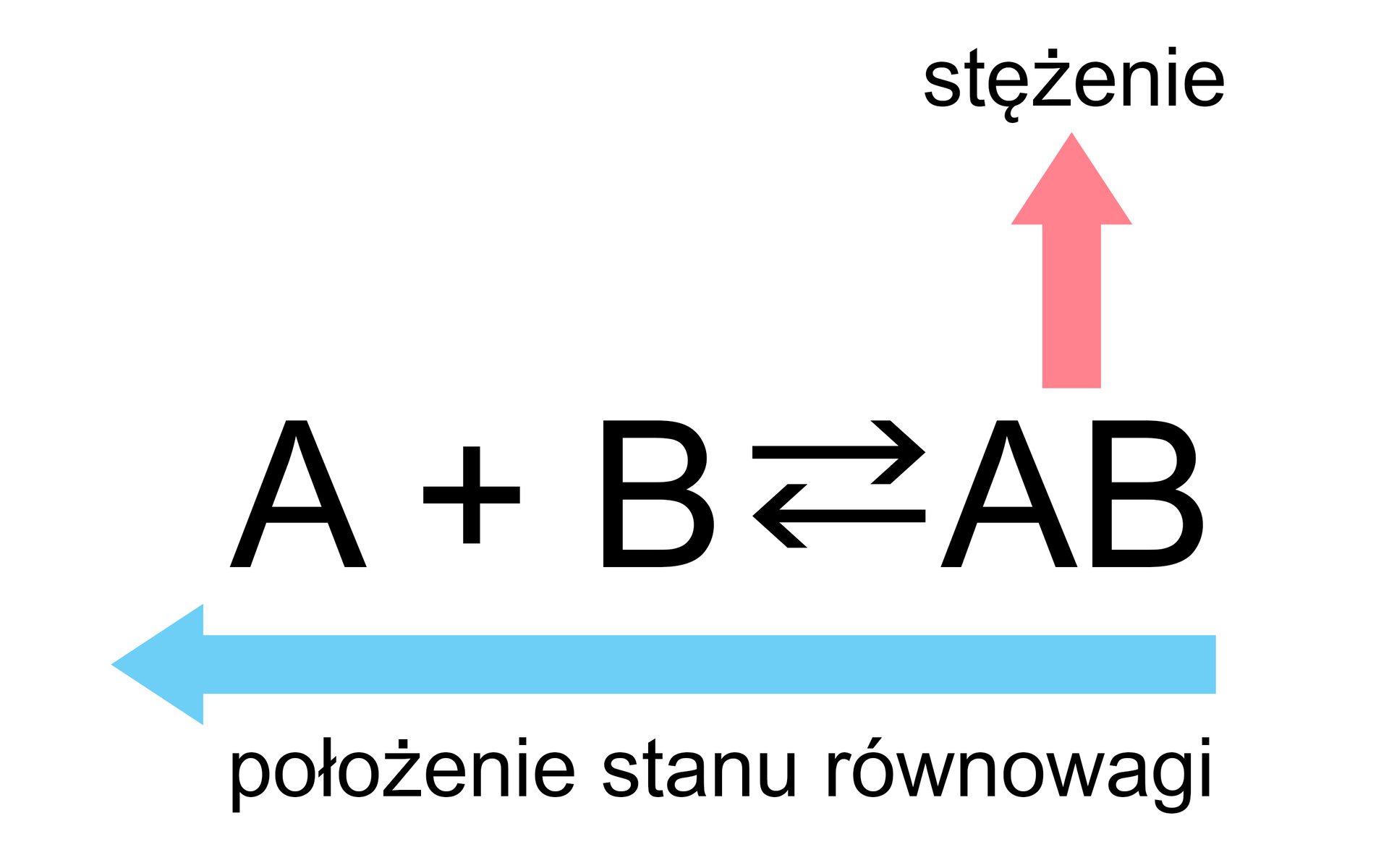
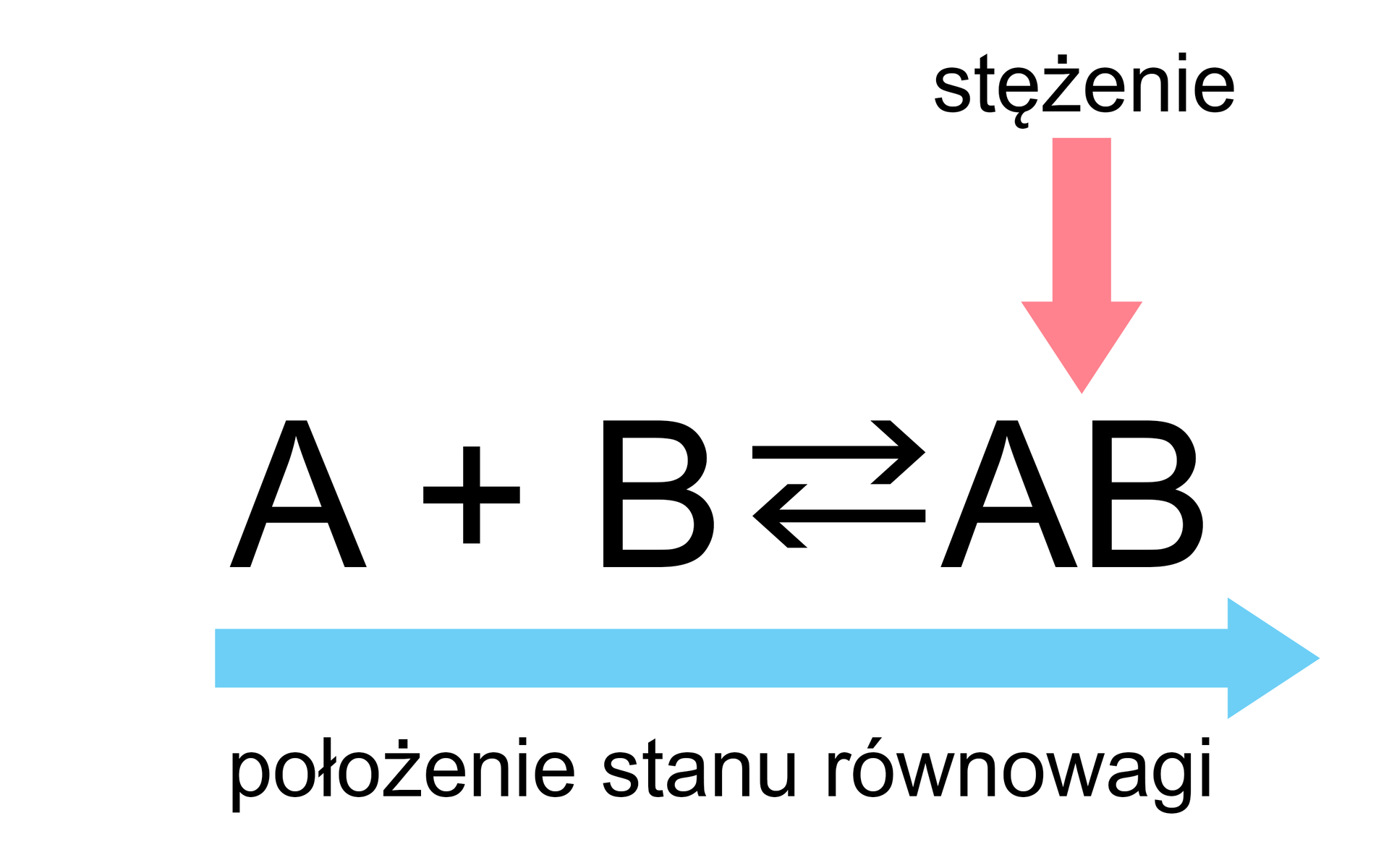
Zmiana położenia stanu równowagi powyższej reakcji może nastąpić poprzez:
Reguła przekory Le Chateliera-Brauna jest przydatnym przewodnikiem do identyfikacji tego, co dzieje się z układem podczas zmian warunków reakcji, będącej w stanie równowagi.
Jak pokazują powyższe przypadki, położenie stanu równowagi można przesuwać „w lewo” lub „w prawo”. Kiedy równowaga reakcji zostaje zaburzona, zainicjowane przemiany trwają tak długo, dopóki nie ustali się „nowy” stan równowagi, a szybkość reakcji, która biegnie w przeciwnych kierunkach, osiągnie tę samą wartość.
Równowaga, osiągnięta przez układ, ustala się przy nowych stężeniach. Co istotne, wartość stałej równowagi KIndeks dolny cc (w stałej temperaturze) nie ulega zmianie.
Uzupełnij tabelę, obrazującą wpływ stężenia reagentów na stan równowagi reakcji opisanej równaniem:
Czy wiesz, w którą stronę przesunie się położenie stanu równowagi chemicznej reakcji, jeśli zostanie zwiększone stężenie jednego z reagentów? Zapoznaj się z filmem samouczkiem. Przeanalizuj, jak rozwiązać przykładowe zadania związane z tematem lekcji, a następnie wykonaj ćwiczenia testowe zamieszczone pod filmem.

Film dostępny pod adresem /preview/resource/RxIxBCpkfKPRM
Film nawiązujący do treści materiału - dotyczy stężenia reagentów i jego wpływu na stan równowagi reakcji.
cztery H C l indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, dwa C l indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego Możliwe odpowiedzi: 1. spowoduje wzrost wydajności reakcji, 2. spowoduje spadek wydajności reakcji, 3. nie wpływa na wydajność tej reakcji, 4. spowoduje wzrost stężenia produktów
dwa N O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
Wybierz czynnik, który spowoduje wzrost wydajności tej reakcji : Możliwe odpowiedzi: 1. wzrost temperatury panującej w układzie, 2. spadek ciśnienia panującego w układzie, 3. usunięcie z mieszaniny reakcyjnej części tlenku azotu(IV), 4. wprowadzenie do układu katalizatora
trzy H indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, N indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa N H indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego, DELTA H, mniejszy niż, zero
Wprowadzenie do układu dodatkowej ilości wodoru : Możliwe odpowiedzi: 1. spowoduje przesunięcie się położenia stanu równowagi w prawo, 2. spowoduje przesunięcie się położenia stanu równowagi w lewo, 3. nie wpływa na położenie stanu równowagi, 4. zmniejsza wydajność tej reakcji
Jak wpłynie wzrost stężenia tlenu w układzie ? Możliwe odpowiedzi: 1. nie wpływa na ilość produktów, 2. spowoduje wzrost ilości produktów, 3. spowoduje spadek ilości produktów, 4. nie można określić jak ta zmiana wpłynie na ilość produktów tej reakcji
cztery N H indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, pięć O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe cztery N O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, sześć H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego
Który z wymienionych czynników spowoduje przesunięcie się położenia stanu równowagi w kierunku produktów? Możliwe odpowiedzi: 1. wzrost stężenia tlenu w układzie, 2. spadek stężenia tlenu w układzie, 3. wprowadzenie katalizatora do układu, 4. wprowadzenie inhibitora do układu
dwa H indeks dolny, dwa, koniec indeksu dolnego, S indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, trzy O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, strzałki równowagowe dwa S O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, dwa H indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, nawias g zamknięcie nawiasu, koniec indeksu dolnego
jeśli w układzie będącym w stanie równowagi usuniemy część pary wodnej. Możliwe odpowiedzi: 1. nie zmieni się, 2. nie można określić wpływu tego czynnika na wydajność tej reakcji, 3. zmaleje, 4. wzrośnie
![Ilustracja przedstawia wzór: K C = [ A B ] [ A ] ⋅ [ B ] . AB znajduje się w czerwonym kole, A w zielonym, B w niebieskim. Koło zielone jest większe od pozostałych.](https://static.zpe.gov.pl/portal/f/res-minimized/R1DlaSpMYLlO9/1616760049/2GgFMAWN1Iea4eBejtfclcPtbdE4rPPK.png)
![Ilustracja przedstawia wzór:
K
C
=
[
A
B
]
[
A
]
⋅
[
B
]
. AB znajduje się w czerwonym kole, A w zielonym, B w niebieskim. Koło zielone jest dużo mniejsze od pozostałych.](https://static.zpe.gov.pl/portal/f/res-minimized/R14DhN2RkqCcf/1616760050/240bXzDCpO3pMNXYGoKDCdmJwiRk6ElA.png)
![Ilustracja przedstawia wzór:
K
C
=
[
A
B
]
[
A
]
⋅
[
B
]
. AB znajduje się w czerwonym owalu, A w zielonym kole, B w zielonym kole.](https://static.zpe.gov.pl/portal/f/res-minimized/Rhfdt7yMUJEp0/1616760050/1b0bGfdvNv6MmAsrl59SsaYq0iyCMKjO.png)
![Ilustracja przedstawia wzór:
K
C
=
[
A
B
]
[
A
]
⋅
[
B
]
. AB znajduje się w czerwonym kole, A w zielonym, B w niebieskim. Czerwone koło jest dużo mniejsze od pozostałych kół.](https://static.zpe.gov.pl/portal/f/res-minimized/RYMUcNRWtJJY9/1616760050/ADuwQffEZfVSXHtjfzyxkryjAJTf7qGk.png)