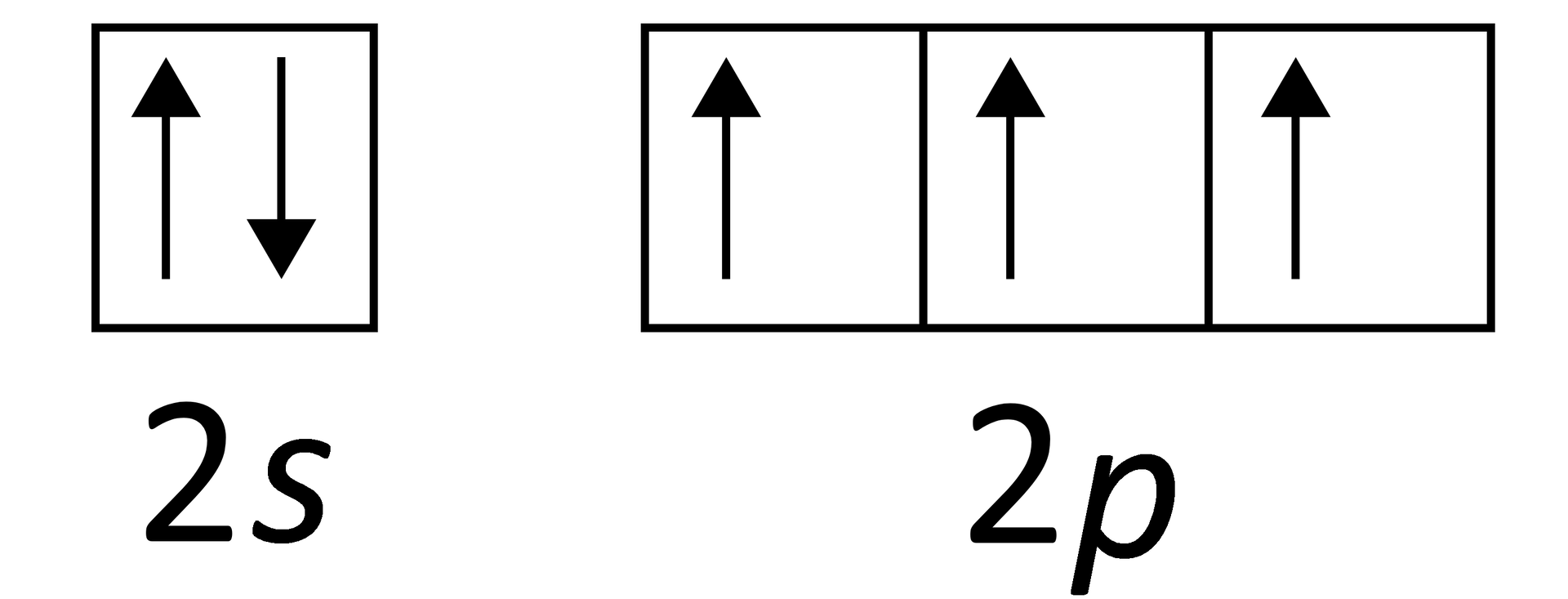
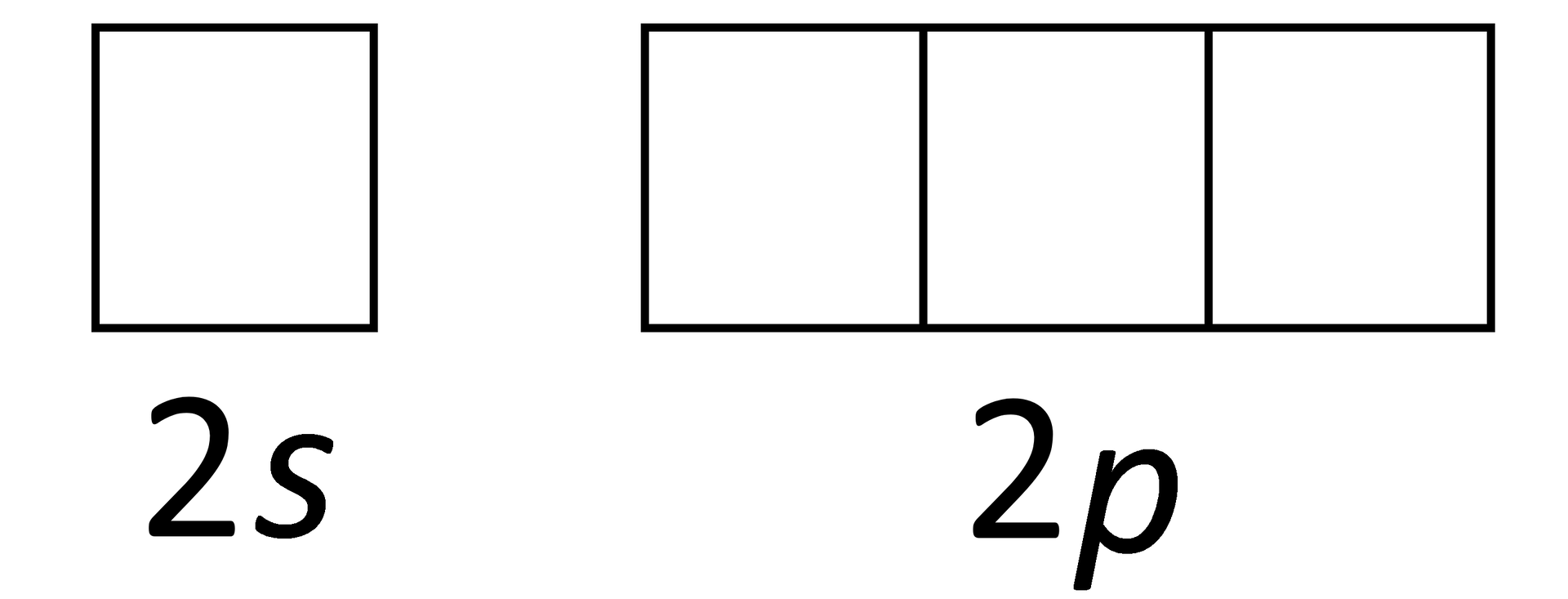
Jak obliczyć stopień utlenienia cząstki nieorganicznej?
Położenie w układzie okresowym a stopień utlenienia
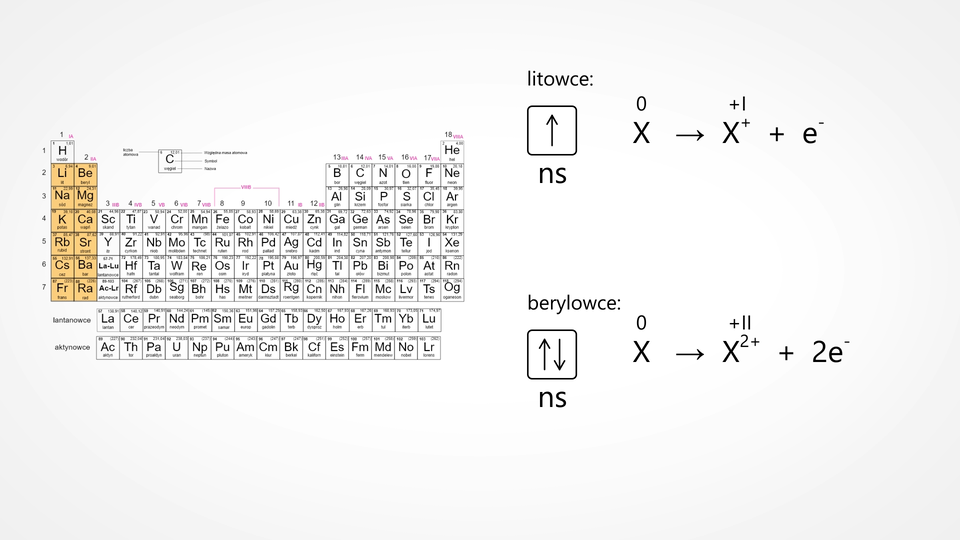
Pierwiastki, w zależności od położenia w układzie okresowym pierwiastków, mogą przyjmować różne stopnie utlenieniastopnie utlenienia (zapisywane cyframi rzymskimi).
Atomy pierwiastków dążą do trwałej konfiguracji, co objawia się zazwyczaj przez uzyskanie oktetu lub dubletu elektronowego (poza gazami szlachetnymi, które mają ją wypełnioną całkowicie). Aby przewidzieć możliwe maksymalne oraz minimalne stopnie utlenienia pierwiastka, należy:
określić charakter pierwiastka w związkach – czy jest to metal, czy niemetal; metale przyjmują dodatnie stopnie utlenienia, w przypadku niemetali mogą one przyjmować dodatnie lub ujemne wartości stopnia utlenienia;
określić liczbę elektronów atomu danego pierwiastka oraz liczbę elektronów walencyjnych;
określić, w jaki sposób atom będzie dążył do trwałej konfiguracji, a więc do oktetu lub dubletu elektronowego; na tej podstawie można przewidzieć, jaką liczbę elektronów powinien przyjąć, oddać lub uwspólnić atom w czasie tworzenia związku chemicznego, tak aby osiągnąć wspomniany oktet lub dublet.
Reguły określania stopnia utlenienia
Aby przypisać stopień utlenienia pierwiastka chemicznego w związku lub w jonie, korzysta się z poniższych reguł.
Pierwiastki w stanie wolnym (bez względu na liczbę wiązań występujących między atomami pierwiastka w cząsteczce) występują na zerowym stopniu utlenienia.
Litowce w związkach chemicznych występują na +I stopniu utlenienia
Berylowce w związkach chemicznych występują na +II stopniu utlenienia
Fluor w związkach chemicznych występuje zawsze na -I stopniu utlenienia.
Wodór
W połączeniach z niemetalami występuje na +I stopniu utlenienia.
W wodorkach metali występuje na -I stopniu utlenienia.
Tlen
W tlenkach, kwasach nieorganicznych i ich solach występuje na stopniu utlenienia: -II;
W nadtlenkach występuje na stopniu utlenienia:-I;
W ponadtlenkach występuje na stopniu utlenienia: -½;
We fluorku tlenu występuje na stopniu utlenienia: +I lub +II.
Stopień utlenienia pierwiastka w jonie prostym jest równy ładunkowi tego jonu.
Suma stopni utlenienia wszystkich atomów w cząsteczce obojętnej równa jest zero, a w jonie złożonym równa jest jego ładunkowi.
Aby więc określić stopień utlenienia pierwiastka w związkach chemicznych lub jonach, należy kierować się powyższymi regułami, które w prosty sposób nam to ułatwią.
Zapoznaj się z filmem pt. „Jak przewidzieć typowe stopnie utlenienia pierwiastka?”, a następnie rozwiąż ćwiczenia sprawdzające.
Film dostępny pod adresem /preview/resource/RJA8tXFoGTiyk
Film nawiązujący do treści materiału dotyczącej przewidywania stopni utlenienia pierwiastków.
Atom pierwiastka X może przyjmować stopnie utlenienia od wartości 0 do wartości +IV, a atom pierwiastka Y może przyjmować stopnie utlenienia od wartości -IV do wartości +IV. Do jakich grup układu okresowego pierwiastków chemicznych należą pierwiastki X i Y?
Zapoznaj się z zamieszczonym samouczkiem i na jego podstawie wykonaj poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/RJJ2656E2XpMQ
Film dotyczy obliczania stopni utlenienia w jonach i cząsteczkach.
Poniżej przedstawiono wzór strukturalny oraz model cząsteczki izocyjanianu chlorosulfonylu, bardzo niebezpiecznej i silnie reaktywnej substancji o wzorze .
Poniżej przedstawiono wzór strukturalny oraz model cząsteczki izocyjanianu chlorosulfonylu, bardzo niebezpiecznej i silnie reaktywnej substancji o wzorze .


Uzupełnij poniższą tabelę, wpisując stopnie utlenienia atomów wskazanych pierwiastków w wymienionych związkach.