Elektroliza stopionych tlenków, soli i wodorotlenków
Jeżeli elektrolizie poddaje się stopione elektrolity (np. tlenki, wodorotlenki, sole), to w takich warunkach wszystkie metale ulegają redukcji na katodzie (niezależnie od wartości ich potencjału standardowego).
Elektroliza stopionych tlenków
Przykładem procesu, w którym wykorzystuje się elektrolizę stopionego tlenku, jest otrzymywanie glinu poprzez proces Halla-Héroulta, opracowanego w roku. Tlenek glinu(), otrzymany z boksytu, rozkładany jest elektrolitycznie na metaliczny glin oraz gazowy tlen. Proces ten zachodzi w sposób ciągły i rozpoczyna się od etapu rozpuszczenia tlenku glinu w krioliciekriolicie, który wypełnia wannę elektrolityczną. Temperatura procesu utrzymywana jest na poziomie –. Powstający w tym procesie glin oddzielany jest od elektrolitu i sukcesywnie usuwany z komory elektrolizera. Uzyskany metal ma większą gęstość od elektrolitu, więc osiada na dnie wanny elektrolitycznej. Z kolei wydzielający się tlen reaguje z grafitową okładziną anody, tworząc tlenek węgla(), który, wydzielając się intensywnie, powoduje mieszanie się elektrolitu i staje się nośnikiem dla gazowych produktów ubocznych.

Wtórna reakcja na anodzie:
Elektroliza stopionych soli
Stopione sole należą do przewodników elektrolitycznych – dobrze przewodzą prąd. Podczas elektrolizy, na anodzie i katodzie wydzielają się produkty ich rozkładu, podobnie jak w przypadku elektrolizy roztworów wodnych. Wówczas z chlorku ołowiu() otrzymuje się chlor i ołów, z chlorku sodu – chlor i sód, a z azotanu() sodu – sód, tlen oraz tlenki azotu.
Metoda stapiania soli stosowana jest wtedy, gdy nie ma możliwości przeprowadzenia elektrolizy wodnych roztworów tych soli (zdarza się, że produkty elektrolizy wodnej reagują z wodą).
Przykładem tego typu elektrolizy jest stapianie chlorku sodu ().
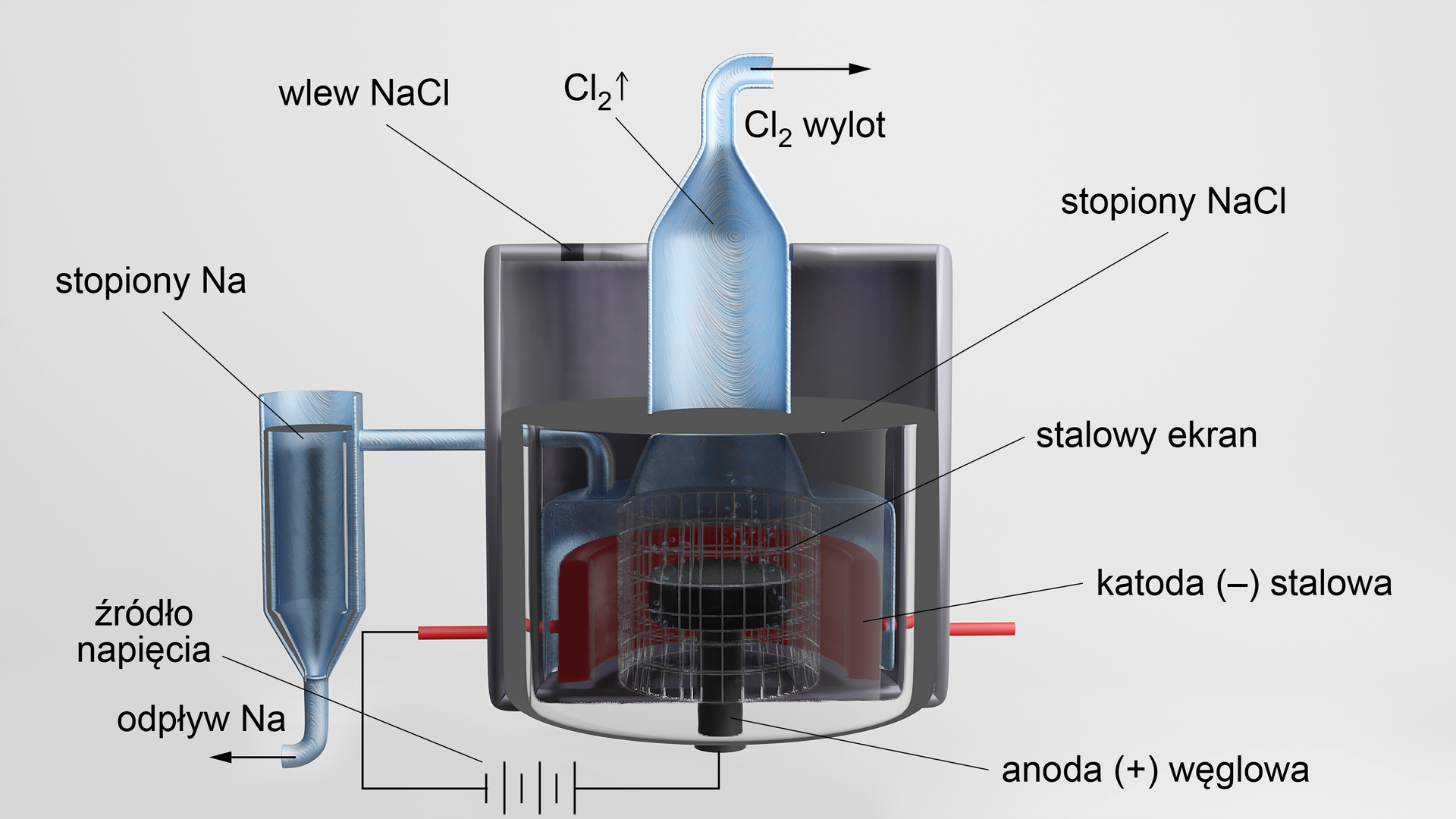
Naturalne solanki, woda morska, karnalit czy dolomit są źródłem chlorku magnezu. Po przeróbce chemicznej tych surowców otrzymuje się uwodniony chlorek magnezu, który jest surowcem do elektrolizy. Chlorek magnezu jest stapiany w temperaturze . W efekcie, na katodzie otrzymywany jest ciekły magnez, natomiast na anodzie wydziela się taka sama ilość chloru.
Elektroliza stopionego chlorku cynku
Umieść w tyglutyglu około bezwodnego chlorku cynku. Następnie ustaw tygiel nad palnikiem i zacznij go ogrzewać aż do stopienia soli (). Kolejnym krokiem jest umieszczenie dwóch elektrod grafitowych, połączonych płaską baterią (), w stopionej soli. Poczekaj kilka minut i opisz obserwację.
Uwaga! Doświadczenie należy przeprowadzać pod wyciągiem.
Podczas przeprowadzania elektrolizy opisanej w doświadczeniu możemy zaobserwować, że nad tyglem pojawia się gaz o charakterystycznym zapachu chloru, a na jednej z elektrod gromadzi się ciało stałe o wyglądzie odmiennym od stopionej soli. Te obserwacje wskazują na zajście elektrolizy stopionej soli.
Elektroliza stopionych wodorotlenków
Przemysłową metodą otrzymywania metalicznego sodu jest proces Castnera, prowadzony w drodze elektrolizy stopionego wodorotlenku sodu w temperaturze około .

W procesie tym metaliczny sód wytwarza się na katodzie. Ze względu na to, że jego gęstość jest mniejsza od stopionego wodorotlenku sodu, wędruje ku górze i gromadzi się w kolektorze.
Reakcje elektrochemiczne tego procesu przedstawiono poniżej.
Reakcja uboczna:
Przeprowadź elektrolizę stopionej soli chlorku sodu (), stopionego tlenku glinu () oraz stopionego wodorotlenku sodu (), a następnie wykonaj ćwiczenia pod symulacją.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D8B29MHPF
Zapoznaj się z poniższymi opisami elektrolizy stopionej soli chlorku sodu , stopionego tlenku glinu oraz stopionego wodorotlenku sodu , a następnie wykonaj ćwiczenia.
Doświadczenie : Elektroliza stopionego chlorku sodu
Układ złożony ze stalowej katody oraz grafitowej anody, zanurzony w stałym chlorku sodu . W układzie ma miejsce dysocjacja termiczna chlorku sodu na skutek ogrzewania. Zamknięcie obwodu i przyłożenie napięcia powoduje przepływ elektronów od anody do katody. Na anodzie ma miejsce proces utlenienia – powstają pęcherzyki gazu, chloru, a aniony chlorkowe poruszają się w kierunku anody, a na katodzie ma miejsce proces redukcji, kationy sodowe poruszają się w kierunku katody, wydziela się metaliczny sód.
Doświadczenie : Elektroliza stopionego tlenku glinu
Układ złożony ze stalowej katody oraz grafitowej anody, zanurzony w stałym tlenku glinu . W układzie ma miejsce dysocjacja termiczna tlenku glinu na skutek ogrzewania. Zamknięcie obwodu i przyłożenie napięcia powoduje przepływ elektronów od anody do katody. Na anodzie ma miejsce proces utlenienia – powstają pęcherzyki gazu, czyli tlenu. Na katodzie natomiast ma miejsce proces redukcji – kationy glinu poruszają się w kierunku katody i wydziela się metaliczny glin.
Doświadczenie : Elektroliza stopionego wodorotlenku sodu
Układ złożony ze stalowej katody oraz grafitowej anody, zanurzony w stałym wodorotlenku sodu . W układzie ma miejsce dysocjacja termiczna wodorotlenku sodu na skutek ogrzewania. Zamknięcie obwodu i przyłożenie napięcia powoduje przepływ elektronów od anody do katody. Na anodzie ma miejsce proces utlenienia – powstają pęcherzyki gazu, czyli tlenu. Na katodzie z kolei ma miejsce proces redukcji, wydziela się metaliczny sód oraz wodór.
Zapisz równania reakcji mających miejsce podczas elektrolizy chlorku sodu, z zaznaczeniem, gdzie te procesy zachodzą. Następnie zapisz równanie sumaryczne reakcji.
Zapisz równania reakcji mających miejsce podczas elektrolizy tlenku glinu, z zaznaczeniem, gdzie te procesy zachodzą. Następnie zapisz równanie sumaryczne reakcji.